22-23高三下·河南洛阳·开学考试
名校
解题方法
1 . 我国政府承诺二氧化碳排放在2030年前达到峰值,2060年前实现碳中和,彰显作为大国的担当和责任。 催化重整对温室气体的减排具有重要意义,其反应为
催化重整对温室气体的减排具有重要意义,其反应为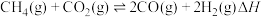 。回答下列问题:
。回答下列问题:
(1)已知:①
②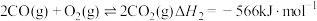
③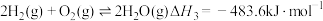
则
___________  。
。
(2)恒容密闭容器中可逆反应 达到平衡状态的标志是___________(填序号)。
达到平衡状态的标志是___________(填序号)。
(3)容器容积为1L,控制 和
和 初始投料量分别为2mol和3mol,发生反应:
初始投料量分别为2mol和3mol,发生反应: ,甲烷的平衡转化率与温度、压强的关系如图甲所示。
,甲烷的平衡转化率与温度、压强的关系如图甲所示。
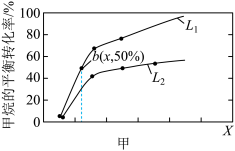
则 代表
代表___________ (填“温度”或“压强”):
___________  (填“大于”或“小于”),并请说出理由:
(填“大于”或“小于”),并请说出理由:___________ ; 点反应的平衡常数为
点反应的平衡常数为___________ 。
(4)500℃下,将 和
和 的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得
的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得 的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
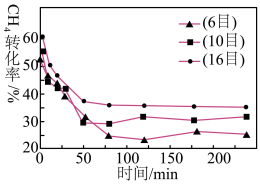
由图乙可知,75min后 转化率与炭催化剂目数的关系为
转化率与炭催化剂目数的关系为___________ ,原因是___________ 。
(5)①温度为 时,
时,
实验测得: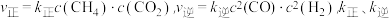 为速率常数。
为速率常数。 时,
时, =
=___________ (以 表示)。
表示)。
②当温度改变为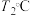 时,
时,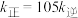 ,则
,则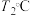 时平衡压强
时平衡压强___________  时平衡压强(填“>”“<”或“=”),理由是
时平衡压强(填“>”“<”或“=”),理由是___________ 。
 催化重整对温室气体的减排具有重要意义,其反应为
催化重整对温室气体的减排具有重要意义,其反应为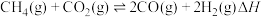 。回答下列问题:
。回答下列问题:(1)已知:①

②
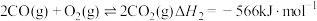
③
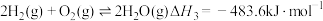
则

 。
。(2)恒容密闭容器中可逆反应
 达到平衡状态的标志是___________(填序号)。
达到平衡状态的标志是___________(填序号)。A.单位时间内生成1mol 的同时消耗2molCO 的同时消耗2molCO |
| B.混合气体的密度不再改变 |
C.反应速率 |
| D.混合气体的平均相对分子质量不再改变 |
 和
和 初始投料量分别为2mol和3mol,发生反应:
初始投料量分别为2mol和3mol,发生反应: ,甲烷的平衡转化率与温度、压强的关系如图甲所示。
,甲烷的平衡转化率与温度、压强的关系如图甲所示。
则
 代表
代表
 (填“大于”或“小于”),并请说出理由:
(填“大于”或“小于”),并请说出理由: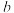 点反应的平衡常数为
点反应的平衡常数为(4)500℃下,将
 和
和 的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得
的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得 的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
由图乙可知,75min后
 转化率与炭催化剂目数的关系为
转化率与炭催化剂目数的关系为(5)①温度为
 时,
时,
实验测得:
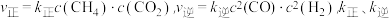 为速率常数。
为速率常数。 时,
时, =
= 表示)。
表示)。②当温度改变为
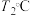 时,
时,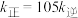 ,则
,则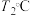 时平衡压强
时平衡压强 时平衡压强(填“>”“<”或“=”),理由是
时平衡压强(填“>”“<”或“=”),理由是
您最近一年使用:0次
2023-02-07更新
|
351次组卷
|
3卷引用:广东省广州市2022届高三一模考试(原理综合题)
名校
2 . 合成氨工业对国民经济和社会发展具有重要的意义,其原理为:
 ,在不同温度、压强和相同催化剂条件下,将
,在不同温度、压强和相同催化剂条件下,将 和
和 充入恒容密闭容器中反应,平衡后混合物中氨的体积分数如图所示。下列说法不正确的是
充入恒容密闭容器中反应,平衡后混合物中氨的体积分数如图所示。下列说法不正确的是


 ,在不同温度、压强和相同催化剂条件下,将
,在不同温度、压强和相同催化剂条件下,将 和
和 充入恒容密闭容器中反应,平衡后混合物中氨的体积分数如图所示。下列说法不正确的是
充入恒容密闭容器中反应,平衡后混合物中氨的体积分数如图所示。下列说法不正确的是
A.反应焓变: | B.压强: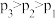 |
| C.M、N两点对应的平衡常数相等 | D.M、N两点 的平衡转化率均为80% 的平衡转化率均为80% |
您最近一年使用:0次
3 . 变化观念与平衡思想是化学学科核心素养之一。下列实验事实不能用平衡移动原理解释的是
| A.由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 |
| B.工业合成氨过程中及时分离出氨气,有利于提高原料转化率 |
| C.通常在硫酸铁或硫酸亚铁溶液中加入少许稀硫酸,抑制其水解 |
| D.久置的氯水黄绿色会褪去 |
您最近一年使用:0次
4 . 下列实验中,操作、现象及结论都正确且有因果关系的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向盛有2 mL 1 mol/L  溶液的甲、乙两试管中分别滴入2滴酚酞,将甲试管加热 溶液的甲、乙两试管中分别滴入2滴酚酞,将甲试管加热 | 甲试管溶液的红色更深 | 升温,促进 溶液向水解方向移动 溶液向水解方向移动 |
| B | 用pH试纸测定同浓度 和NaClO溶液的pH 和NaClO溶液的pH | NaClO溶液的pH比较大 |  酸性比HClO强 酸性比HClO强 |
| C | 压缩装有 和 和 混合气体的注射器 混合气体的注射器 | 压缩后气体颜色比压缩前要浅 | 加压,平衡向气体分子数减小方向移动 |
| D | 向盛有2 mL 0.1 mol/L  溶液中滴入2滴0.1 mol/L NaCl溶液,再滴入2滴0.1 mol/L KI溶液,振荡 溶液中滴入2滴0.1 mol/L NaCl溶液,再滴入2滴0.1 mol/L KI溶液,振荡 | 先有白色沉淀,后变为黄色 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 向密闭容器中充入S2Cl2、Cl2和SCl2,发生反应 ,S2Cl2与SCl2的初始消耗速率(v)与温度(T)的关系如图所示(图中A、B点处于平衡状态),下列说法不正确的是
,S2Cl2与SCl2的初始消耗速率(v)与温度(T)的关系如图所示(图中A、B点处于平衡状态),下列说法不正确的是

 ,S2Cl2与SCl2的初始消耗速率(v)与温度(T)的关系如图所示(图中A、B点处于平衡状态),下列说法不正确的是
,S2Cl2与SCl2的初始消耗速率(v)与温度(T)的关系如图所示(图中A、B点处于平衡状态),下列说法不正确的是
| A.a为v(SCl2)随温度的变化曲线 |
| B.该反应的ΔH<0 |
| C.200℃下反应一段时间,S2Cl2的物质的量增多 |
| D.反应达到平衡后向体系中充入氦气,平衡不移动 |
您最近一年使用:0次
名校
解题方法
6 . 向相同体积的甲、乙两容器中,甲容器中充入1molSO2和1 molO2,乙容器中充入2mol SO2和2 molO2且保持体积不变,在相同温度下,下列叙述中错误的是
| A.化学反应速率:乙>甲 | B.平衡时SO2的体积分数:乙>甲 |
| C.平衡时SO2的转化率:乙>甲 | D.平衡时O2的浓度:乙>甲 |
您最近一年使用:0次
名校
解题方法
7 . 向两个体积可变的密闭容器中均充入1 mol的 和2 mol的
和2 mol的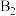 ,发生反应
,发生反应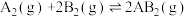
 。维持两个容器的压强分别为
。维持两个容器的压强分别为 和
和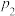 ,在不同温度下达到平衡,测得平衡时
,在不同温度下达到平衡,测得平衡时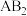 的体积分数随温度的变化如图所示。下列叙述正确的是
的体积分数随温度的变化如图所示。下列叙述正确的是
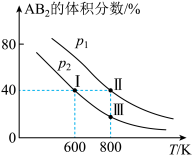
已知:图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上;
 和2 mol的
和2 mol的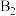 ,发生反应
,发生反应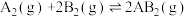
 。维持两个容器的压强分别为
。维持两个容器的压强分别为 和
和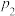 ,在不同温度下达到平衡,测得平衡时
,在不同温度下达到平衡,测得平衡时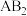 的体积分数随温度的变化如图所示。下列叙述正确的是
的体积分数随温度的变化如图所示。下列叙述正确的是
已知:图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上;
A.由图像可知, , , |
B.点Ⅰ时 的平衡转化率为40% 的平衡转化率为40% |
| C.点Ⅱ和点Ⅲ所对应的反应平衡常数相等 |
| D.将点Ⅱ所对应的容器冷却到600 K,可变成点Ⅰ |
您最近一年使用:0次
2022-12-12更新
|
239次组卷
|
2卷引用:广东省梅州市大埔县虎山中学2023届高三下学期6月模拟化学试题
名校
8 . 下列事实不能用平衡移动原理解释的是
| A.氯水在光照下颜色变浅,最终变为无色 |
| B.夏天打开啤酒瓶,有很多气泡冒出 |
| C.工业上合成氨时将温度控制在400-500度 |
| D.实验室用排饱和食盐水的方法收集Cl2 |
您最近一年使用:0次
2022-12-12更新
|
158次组卷
|
2卷引用:广东省广州市东涌中学2022-2023学年高二上学期期中考试化学试题
9 . 下列陈述Ⅰ和陈述Ⅱ均正确且有因果关系的是
| 选项 | 选项I | 选项II |
| A | Si-O键键能比Si-H键高 |  的熔沸点比 的熔沸点比 高 高 |
| B | Cl的非金属性比Si强 |  溶液中滴加盐酸产生白色凝胶 溶液中滴加盐酸产生白色凝胶 |
| C | 生铁中含有碳元素而纯铁中不含 | 生铁比纯铁熔点更低,硬度更大 |
| D | 增大压强, 平衡正移 平衡正移 | 压缩 和 和 混合气体体积,红棕色变深 混合气体体积,红棕色变深 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 某温度下,反应 CH2=CH2(g)+H2O(g)⇌CH3CH2OH(g)在密闭容器中达到平衡。下列说法正确的是
| A.加压,υ正增大,υ逆减小,平衡正向移动 |
| B.加入催化剂,CH2=CH2的平衡转化率增大 |
| C.再充入一定量CH2=CH2,CH2=CH2的平衡转化率增大 |
| D.分离出CH3CH2OH(g),υ逆减小,平衡正向移动 |
您最近一年使用:0次



