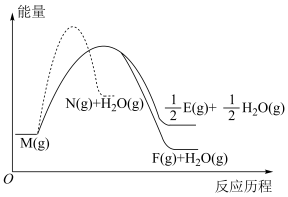
1 . 某1L恒容密闭容器发生反应: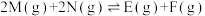
 。向容器中通入0.2molM和nmolN发生上述反应,测得M的平衡转化率与投料比
。向容器中通入0.2molM和nmolN发生上述反应,测得M的平衡转化率与投料比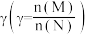 以及温度的关系如图。下列说法正确的是
以及温度的关系如图。下列说法正确的是
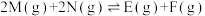
 。向容器中通入0.2molM和nmolN发生上述反应,测得M的平衡转化率与投料比
。向容器中通入0.2molM和nmolN发生上述反应,测得M的平衡转化率与投料比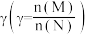 以及温度的关系如图。下列说法正确的是
以及温度的关系如图。下列说法正确的是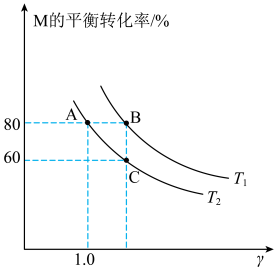
A. |
B. 时,C点的平衡常数值为2500 时,C点的平衡常数值为2500 |
C.当 时,反应达到平衡 时,反应达到平衡 |
| D.其它条件不变,增大压强,可使B点移向C点 |
您最近一年使用:0次
名校
2 . 下列实验装置能够达到实验目的的是
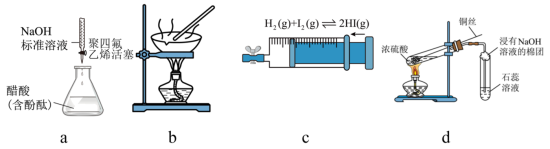
| A.图a测定醋酸的浓度 |
| B.图b由MgCl2溶液制取无水MgCl2 |
| C.图c探究压强对平衡的影响 |
| D.图d检验二氧化硫的漂白性 |
您最近一年使用:0次
2024-04-22更新
|
244次组卷
|
2卷引用:2024届广东省深圳市外国语学校高三下学期第九次模拟考试化学试题
解题方法
3 . H2O2俗称双氧水,是常用的绿色氧化剂,在生产和生活中发挥重要的作用。
(1)富勒烯C60颗粒对H2O2液相氧化:SO2具有明显的促进效果,该反应机理和能量变化如下:
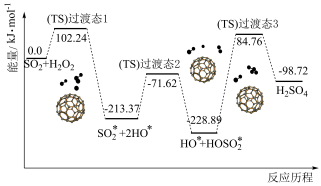
①H2O2液相氧化:SO2生成H2SO4的热化学方程式为________ 。
②图示历程包含________ 个基元反应,写出决速步骤的化学方程式________________ 。
③C60间的作用力是________ 。
(2) H2O2可用于工业源氮氧化物(NOx)的催化氧化,H2O2去除NO的反应存在平衡:
(i)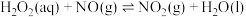
(ii)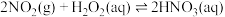
(iii)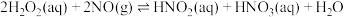
(iv)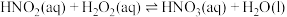
①上述反应体系在一定条件下建立平衡后,下列说法正确的有________ (填序号)。
A.其他条件不变时,温度越高,NO的转化率越大
B.加入催化剂,c(HNO3)与c(HNO2)比值保持不变
C.恒温恒压下,充入Ar,平衡(i)、(ii)向正反应方向移动
D.增大H2O2浓度,反应(i)、(ii)、(iii)、(iv)正反应速率都增加
②一定范围内,催化剂光热协同辅助H2O2降解NO的去除率变化如图甲所示,NO去除率最佳的反应条件为________ 。
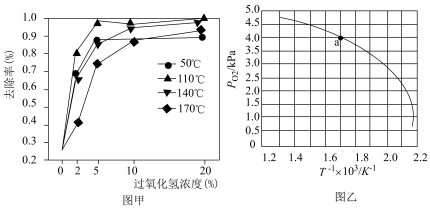
(3)过碳酸钠(2Na2CO3∙3H2O2)又称固体过氧化氢,是碳酸钠和过氧化氢的加成复合物。将2Na2CO3∙3H2O2置入真空的刚性容器中,升高温度发生分解反应:
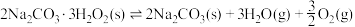 平衡时
平衡时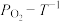 的关系如上图乙所示。a点时,该反应的平衡总压=
的关系如上图乙所示。a点时,该反应的平衡总压=________ kPa,平衡常数Kp=________ 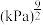 (列出算式),Kp随温度升高而
(列出算式),Kp随温度升高而________ (填“增大”、“减少”或“不变”)。
(1)富勒烯C60颗粒对H2O2液相氧化:SO2具有明显的促进效果,该反应机理和能量变化如下:

①H2O2液相氧化:SO2生成H2SO4的热化学方程式为
②图示历程包含
③C60间的作用力是
(2) H2O2可用于工业源氮氧化物(NOx)的催化氧化,H2O2去除NO的反应存在平衡:
(i)
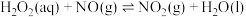
(ii)
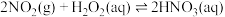
(iii)
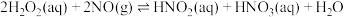
(iv)
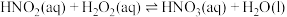
①上述反应体系在一定条件下建立平衡后,下列说法正确的有
A.其他条件不变时,温度越高,NO的转化率越大
B.加入催化剂,c(HNO3)与c(HNO2)比值保持不变
C.恒温恒压下,充入Ar,平衡(i)、(ii)向正反应方向移动
D.增大H2O2浓度,反应(i)、(ii)、(iii)、(iv)正反应速率都增加
②一定范围内,催化剂光热协同辅助H2O2降解NO的去除率变化如图甲所示,NO去除率最佳的反应条件为

(3)过碳酸钠(2Na2CO3∙3H2O2)又称固体过氧化氢,是碳酸钠和过氧化氢的加成复合物。将2Na2CO3∙3H2O2置入真空的刚性容器中,升高温度发生分解反应:
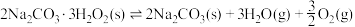 平衡时
平衡时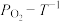 的关系如上图乙所示。a点时,该反应的平衡总压=
的关系如上图乙所示。a点时,该反应的平衡总压=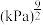 (列出算式),Kp随温度升高而
(列出算式),Kp随温度升高而
您最近一年使用:0次
4 . 化学无处不在,下列有关说法正确的是
| A.淀粉、纤维素、油脂均属于天然高分子 |
| B.炒菜后铁锅不及时清理容易生锈,因为潮湿环境中铁锅发生析氢腐蚀 |
| C.打开汽水瓶盖有大量气泡冒出,可用勒夏特列原理解释 |
| D.向鸡蛋清溶液中加入食盐浓溶液有白色沉淀析出,因为食盐能使蛋白质变性 |
您最近一年使用:0次
5 . 在一密闭容器中,物质 发生三个脱水的竞争反应:①
发生三个脱水的竞争反应:①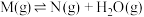

②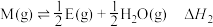 ③
③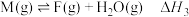 反应历程如图所示。相同条件下,下列说法正确的是
反应历程如图所示。相同条件下,下列说法正确的是
 发生三个脱水的竞争反应:①
发生三个脱水的竞争反应:①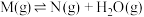

②
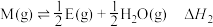 ③
③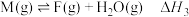 反应历程如图所示。相同条件下,下列说法正确的是
反应历程如图所示。相同条件下,下列说法正确的是
| A.由图可知,物质M比物质N稳定 |
| B.反应①比反应②和③更快达到化学平衡 |
C.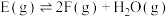 的反应热 的反应热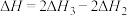 |
| D.平衡后压缩容器,物质E的物质的量不变 |
您最近一年使用:0次
6 . 氮的化合物在生产生活中广泛存在。
(1)①氯胺(NH2Cl)的电子式为___________ 。可通过反应NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g)制备氯胺,已知部分化学键的键能如表所示,则上述反应的ΔH_________ kJ/mol。
②NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为___________ 。
(2)用焦炭还原NO的反应为:2NO(g)+C(s) N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
①该正反应为______ (填“放热”或“吸热”)反应。
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=_________ mol/(L·min)。
(3)用焦炭还原NO2的反应为2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C(s)发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C(s)发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
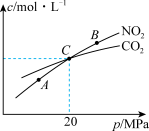
①A、B两点的浓度平衡常数关系:KA_______ KB(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最低的是___________ (填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp=_________ MPa(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)①氯胺(NH2Cl)的电子式为
| 键能/(kJ·mol-1) | 391 | 243 | 191 | 431 |
| 化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
(2)用焦炭还原NO的反应为:2NO(g)+C(s)
 N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器,400℃)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)‘(乙容器,400℃)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器,T℃)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=
(3)用焦炭还原NO2的反应为2NO2(g)+2C(s)
 N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C(s)发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C(s)发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
①A、B两点的浓度平衡常数关系:KA
②A、B、C三点中NO2的转化率最低的是
③计算C点时该反应的压强平衡常数Kp=
您最近一年使用:0次
名校
解题方法
7 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验淀粉水解是否完全 | 取少量淀粉于锥形瓶中,以固液比1∶10加入稀硫酸,牛皮纸封口,在120℃下水解30min,取适量水解液于试管中,加入足量NaOH溶液后加入碘水 | 无明显现象,说明淀粉水解完全 |
| B | 验证CH2=CHCHO分子中的碳碳双键 | 取样与适量溴水混合,充分反应,观察现象 | 溴水褪色,说明样品分子中含有碳碳双键 |
| C | 验证压强对平衡移动的影响 | 压缩装有NO2和N2O4混合气体(已达平衡)的容器 | 气体颜色先变深后稍变浅,平衡向生成N2O4的方向移动 |
| D | 检验干燥氯气的漂白性 | 将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片 | 有色鲜花褪色,干燥氯气具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-29更新
|
347次组卷
|
3卷引用:广东省广州大学附属中学2023-2024学年高三上学期期末化学试题
广东省广州大学附属中学2023-2024学年高三上学期期末化学试题辽宁省大连市第八中学2022-2023学年高三上学期12月月考化学试题(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
2023·山东青岛·三模
解题方法
8 . 已知反应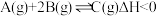 。在体积可变的密闭容器中,按
。在体积可变的密闭容器中,按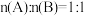 充入反应物进行反应,A的平衡转化率与温度、压强关系如图所示。下列说法正确的是
充入反应物进行反应,A的平衡转化率与温度、压强关系如图所示。下列说法正确的是
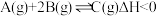 。在体积可变的密闭容器中,按
。在体积可变的密闭容器中,按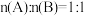 充入反应物进行反应,A的平衡转化率与温度、压强关系如图所示。下列说法正确的是
充入反应物进行反应,A的平衡转化率与温度、压强关系如图所示。下列说法正确的是
A.温度: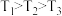 |
B.平均摩尔质量: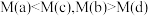 |
C.a点的分压平衡常数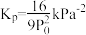 |
D.d点: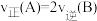 |
您最近一年使用:0次
2023-05-27更新
|
1028次组卷
|
5卷引用:选择题11-16
(已下线)选择题11-16山东省青岛市2023届高三第三次适应性检测化学试题考点巩固卷08 化学反应速率与化学平衡(3大考点45题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)第28讲化化学平衡的移动及反应进行的方向(已下线)提升练05 化学平衡常数的计算-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
解题方法
9 . 纳米二氧化钛催化剂可用于工业上合成甲醇: ,按
,按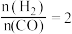 投料比将
投料比将 与
与 充入
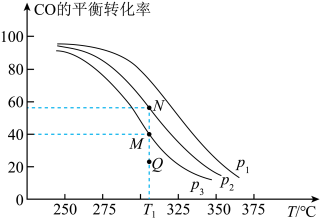
充入 恒容密闭容器中,在一定条件下发生反应,测得
恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
 ,按
,按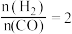 投料比将
投料比将 与
与 充入
充入 恒容密闭容器中,在一定条件下发生反应,测得
恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
A. |
B.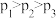 |
C.N点 转化率、平衡常数均大于M点 转化率、平衡常数均大于M点 |
D. 、 、 压强下,Q点对应的 压强下,Q点对应的 |
您最近一年使用:0次
2023-04-27更新
|
471次组卷
|
3卷引用:广东省部分学校2023届高三下学期4月大联考化学试题
名校
解题方法
10 . 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)⇌2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:

已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法错误的是

已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法错误的是
| A.该反应△H>0 |
| B.550℃时,充入惰性气体将使v正>v逆 |
| C.650℃时,反应达平衡后CO2的转化率为25.0% |
| D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.0p总 |
您最近一年使用:0次
2023-04-17更新
|
736次组卷
|
4卷引用:广东省江门市2023届高三下学期第一次模拟考试化学试题



