名校
解题方法
1 . 在恒温恒容下,在一容器充入2molSO2和1molO2发生反应:2SO2(g)+O2(g)⇌2SO3(g),达到平衡后,SO3的体积分数为p%。在恒温恒容下再充入2molSO2和1molO2,再次达到平衡后,SO3的体积分数为
| A.小于p% | B.等于p% | C.大于p% | D.无法判断 |
您最近一年使用:0次
名校
2 . 在一密闭容器中,反应aM(g) bN(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,N的浓度变为原来的60%。下列有关判断正确的是
bN(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,N的浓度变为原来的60%。下列有关判断正确的是
 bN(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,N的浓度变为原来的60%。下列有关判断正确的是
bN(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,N的浓度变为原来的60%。下列有关判断正确的是| A.平衡向逆反应方向移动 | B.反应的化学平衡常数变大 |
| C.物质M的转化率变小 | D.a、b的大小关系是:a < b |
您最近一年使用:0次
名校
3 . Ⅰ.在硫酸工业中,通过下列反应使SO2氧化成SO3:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1。
2SO3(g) ΔH=-196.6 kJ·mol-1。
下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
已知:反应条件为催化剂、加热;催化剂是V2O5,在400~500 ℃时催化剂效果最好
(1)一定温度下,在容积不变的密闭容器中发生上述反应,能说明反应达到平衡状态的是_______
(2)分析表格数据,为了使SO2尽可能多地转化为SO3,应选择______ ℃、______ Mpa下进行实验。
(3)在实际生产中,选定的温度为400~500 ℃,原因是___
(4)在实际生产中,采用的压强为常压,原因是______
(5)在实际生产中,通入过量的空气,原因是_____
(6)尾气中SO2必须回收,原因是______
Ⅱ.乙酸甲酯(CH3COOCH3)与氢气制备乙醇主要发生如下反应:CH3COOCH3(g)+2H2(g) CH3OH(g)+CH3CH2OH(g) ,一定温度、1.01 MPa下,在恒容容器中以n(CH3COOCH3)∶n(H2)=1∶10的投料比进行反应,乙酸甲酯转化率与气体总压强的关系如图所示:
CH3OH(g)+CH3CH2OH(g) ,一定温度、1.01 MPa下,在恒容容器中以n(CH3COOCH3)∶n(H2)=1∶10的投料比进行反应,乙酸甲酯转化率与气体总压强的关系如图所示:

已知:对于气相反应,某组分的平衡分压=总压×平衡时某组分的物质的量分数
(7)A点时,CH3COOCH3(g)的平衡分压为_____ ,CH3CH2OH(g)的体积分数为_____ %(保留一位小数)。
(8)此温度下,该反应的化学平衡常数Kp=_____ MPa-1(用平衡分压代替平衡浓度计算,列出计算式,不要求计算结果)。
 2SO3(g) ΔH=-196.6 kJ·mol-1。
2SO3(g) ΔH=-196.6 kJ·mol-1。下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
| 温度/℃ | 平衡时SO2的转化率/% | ||||
| 0.1 MPa | 0.5 MPa | 1 MPa | 5 MPa | 10 MPa | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
(1)一定温度下,在容积不变的密闭容器中发生上述反应,能说明反应达到平衡状态的是_______
| A.SO2的体积分数不再变化 | B.混合物的密度不再变化 |
| C.v(SO2)=2v(O2) | D.气体的压强不再变化 |
(3)在实际生产中,选定的温度为400~500 ℃,原因是
(4)在实际生产中,采用的压强为常压,原因是
(5)在实际生产中,通入过量的空气,原因是
(6)尾气中SO2必须回收,原因是
Ⅱ.乙酸甲酯(CH3COOCH3)与氢气制备乙醇主要发生如下反应:CH3COOCH3(g)+2H2(g)
 CH3OH(g)+CH3CH2OH(g) ,一定温度、1.01 MPa下,在恒容容器中以n(CH3COOCH3)∶n(H2)=1∶10的投料比进行反应,乙酸甲酯转化率与气体总压强的关系如图所示:
CH3OH(g)+CH3CH2OH(g) ,一定温度、1.01 MPa下,在恒容容器中以n(CH3COOCH3)∶n(H2)=1∶10的投料比进行反应,乙酸甲酯转化率与气体总压强的关系如图所示:
已知:对于气相反应,某组分的平衡分压=总压×平衡时某组分的物质的量分数
(7)A点时,CH3COOCH3(g)的平衡分压为
(8)此温度下,该反应的化学平衡常数Kp=
您最近一年使用:0次
名校
4 . 下列说法正确的是
A.恒温恒压,N2+3H2 2NH3达平衡时,各物质的物质的量均为1mol。再充3molN2,平衡正向移动 2NH3达平衡时,各物质的物质的量均为1mol。再充3molN2,平衡正向移动 |
| B.常温下,pH=3的醋酸与pH=3的盐酸体积比1:2混合后,混合溶液的pH=3 |
C.一定温度下的密闭容器中,发生反应2Cu2O(s)+O2(g) 4CuO(s),达平衡时压强为P0,将容器体积减小至原来的一半,达到新的平衡时气体压强为P,则P0<P<2P0 4CuO(s),达平衡时压强为P0,将容器体积减小至原来的一半,达到新的平衡时气体压强为P,则P0<P<2P0 |
D.恒温恒体积的容器,对反应2NO2(g) N2O4(g),在一定条件下达到平衡。若增加NO2的物质的量,可使再次平衡时 N2O4(g),在一定条件下达到平衡。若增加NO2的物质的量,可使再次平衡时 的值增大 的值增大 |
您最近一年使用:0次
名校
解题方法
5 . 乙烯气相水化法制备乙醇: 。乙烯的平衡转化率随温度、压强的变化关系如下图(起始时,
。乙烯的平衡转化率随温度、压强的变化关系如下图(起始时,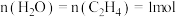 )。
)。
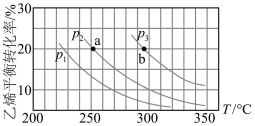
下列分析不正确的是
 。乙烯的平衡转化率随温度、压强的变化关系如下图(起始时,
。乙烯的平衡转化率随温度、压强的变化关系如下图(起始时,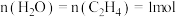 )。
)。
下列分析不正确的是
A.乙烯气相直接水化反应的 |
B.图中压强的大小关系为: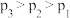 |
| C.图中a、b两点对应的化学平衡常数相等 |
D.达到平衡状态a、b所需要的时间: |
您最近一年使用:0次
名校
6 . 已知反应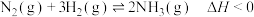 ,平衡时
,平衡时 的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是
的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是

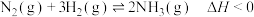 ,平衡时
,平衡时 的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是
的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是
A.平衡常数值: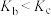 |
B. 温度下,若由a点达到 温度下,若由a点达到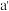 ,可以采取减小压强的方法 ,可以采取减小压强的方法 |
C.d点: |
D.从b点变为 点,增加 点,增加 的物质的量 的物质的量 |
您最近一年使用:0次
7 . 下列叙述中,不能用勒夏特列原理解释的是
A.合成氨工业的反应: ,增大压强有利于氨的合成 ,增大压强有利于氨的合成 |
| B.向双氧水中加入二氧化锰有利于氧气生成 |
| C.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| D.用饱和食盐水吸收氯气中的HCl |
您最近一年使用:0次
名校
8 . 由下列实验事实所得出的结论正确的是
| 选项 | 实验事实 | 结论 |
| A | 某温度下,向容积可变的密闭容器中加入足量CaCO3,发生反应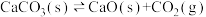 ,并达到平衡,将容器容积增大为原来的2倍 ,并达到平衡,将容器容积增大为原来的2倍 | 当体系再次达到平衡时,气体密度不变 |
| B | 恒温恒容条件下, ,增加 ,增加 的物质的量 的物质的量 | H2O的平衡转化率提高,且增大其反应速率 |
| C | 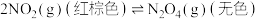  ,在反应达到平衡后,对平衡体系采取缩小容积、增大压强的措施, ,在反应达到平衡后,对平衡体系采取缩小容积、增大压强的措施, | 因为平衡向正反应方向移动,故体系颜色变浅 |
| D | 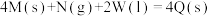 常温下,自发进行 常温下,自发进行 | 则ΔH>0 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
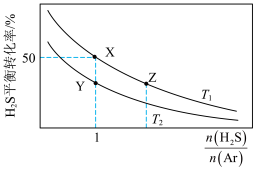
9 .  分解的热化学方程式为
分解的热化学方程式为
 。向体积为1L的恒容密闭容器中加入
。向体积为1L的恒容密闭容器中加入 的混合气体(Ar不参与反应),测得不同温度
的混合气体(Ar不参与反应),测得不同温度 时
时 的平衡转化率随
的平衡转化率随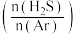 比值的变化如图所示。下列说法正确的是
比值的变化如图所示。下列说法正确的是
 分解的热化学方程式为
分解的热化学方程式为
 。向体积为1L的恒容密闭容器中加入
。向体积为1L的恒容密闭容器中加入 的混合气体(Ar不参与反应),测得不同温度
的混合气体(Ar不参与反应),测得不同温度 时
时 的平衡转化率随
的平衡转化率随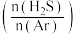 比值的变化如图所示。下列说法正确的是
比值的变化如图所示。下列说法正确的是
A.该反应的 |
B.平衡常数 |
C. 温度下,当 温度下,当 ,到达平衡时, ,到达平衡时, 的体积分数为 的体积分数为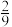 |
D.维持Y点时 不变,向容器中充入Ar, 不变,向容器中充入Ar, 的平衡转化率减小 的平衡转化率减小 |
您最近一年使用:0次
2023-12-11更新
|
376次组卷
|
17卷引用:广东省广州市第三中学、第四中学、培正中学2023-2024学年高二上学期期中考试化学试题
广东省广州市第三中学、第四中学、培正中学2023-2024学年高二上学期期中考试化学试题湖北省石首市2021-2022学年高二上学期期中考试化学试题江西省南昌市第一中学2022-2023学年高二上学期11月期中考试化学试题河北省保定市六校联考2023-2024学年高二上学期11月期中考试化学试题江苏省如皋中学2021-2022学年高三上学期第一次阶段考试化学试题黑龙江省佳木斯市第一中学2021-2022学年高三上学期第五次调研考试化学试题2021年北京高考化学试题变式题11-19(已下线)专题25 关于化学平衡的计算-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)北京市怀柔区2021-2022学年高二上学期期末考试化学试题重庆市天星桥中学2021-2022学年高二上学期第一次月考化学试题山西省太原市第五中学校2022-2023学年高二上学期10月月考化学试题湖北省武汉外国语学校2022-2023学年高二上学期第五次阶段性测试化学试题江苏省南通市通州区金沙中学2021-2022学年高二上学期第二次调研考试化学试题湖北省沙市中学2022-2023学年高二上学期12月月考化学试题(已下线)选择题11-14陕西省安康市2023-2024学年高二上学期期末考试化学试题四川省成都市教育科学研究院附属中学2023-2024学年高二上学期10月月考化学试题
名校
10 . 已知:A(g)+2B(g) 3C(s)+3D(g) △H<0。若在容积可变的密闭容器中进行反应,下列对图像的分析中不正确的是
3C(s)+3D(g) △H<0。若在容积可变的密闭容器中进行反应,下列对图像的分析中不正确的是
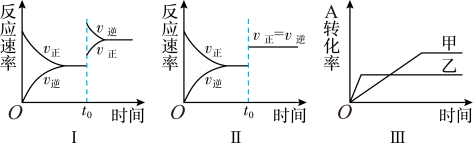
 3C(s)+3D(g) △H<0。若在容积可变的密闭容器中进行反应,下列对图像的分析中不正确的是
3C(s)+3D(g) △H<0。若在容积可变的密闭容器中进行反应,下列对图像的分析中不正确的是
| A.图I研究的是t0时升高温度对反应速率的影响 |
| B.图II可能是t0时使用催化剂对反应速率的影响 |
| C.图III研究的是温度对化学平衡的影响,且乙的温度较高 |
| D.图III研究的是压强对化学平衡的影响,且乙的压强较大 |
您最近一年使用:0次
2023-10-17更新
|
324次组卷
|
2卷引用:广东省广州市第三中学、第四中学、培正中学2023-2024学年高二上学期期中考试化学试题



