名校
解题方法
1 . 在一密闭容器中,反应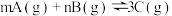 达到平衡时,测得
达到平衡时,测得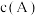 为
为 在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得
在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得 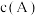 为
为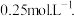 下列判断中不正确的是
下列判断中不正确的是
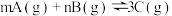 达到平衡时,测得
达到平衡时,测得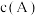 为
为 在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得
在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得 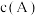 为
为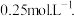 下列判断中不正确的是
下列判断中不正确的是| A.物质B的质量分数减小 | B.平衡时逆反应速率减小 |
C.化学计量数: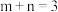 | D.物质C的体积分数不变 |
您最近一年使用:0次
2020-01-17更新
|
226次组卷
|
5卷引用:重庆市南岸区2019-2020学年高二上学期期末学业质量调研抽测化学试题
2 . 下列不能能用勒夏特烈原理解释的是( )
| A.对2HI⇌H2+I2平衡体系增加压强使颜色变深 |
| B.在溴水中存在如下平衡:Br2+H2O⇌HBr+HBrO,当加入NaOH溶液后颜色变浅 |
| C.反应2NO+2CO⇌2CO2+N2正反应放热,升高温度使平衡向逆方向移动 |
| D.合成氨反应:N2+3H2⇌2NH3正反应放热,为使氨的产率提高,理论上应采取低温高压的措施 |
您最近一年使用:0次
解题方法
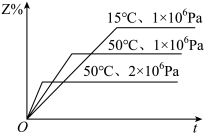
3 . 在密闭容器中进行反应:X(g)+Y(g) Z(g)+2W。如图所示,其中Z%是Z的体积分数,t是时间,下列关于该反应的分析正确的是
Z(g)+2W。如图所示,其中Z%是Z的体积分数,t是时间,下列关于该反应的分析正确的是
 Z(g)+2W。如图所示,其中Z%是Z的体积分数,t是时间,下列关于该反应的分析正确的是
Z(g)+2W。如图所示,其中Z%是Z的体积分数,t是时间,下列关于该反应的分析正确的是
| A.正反应吸热,W为气体 |
| B.正反应吸热,W为固体或纯液体 |
| C.正反应放热,W为气体 |
| D.正反应放热,W为固体或纯液体 |
您最近一年使用:0次
4 . 反应:aX(g)+bY(g) cZ(g),达到平衡时测得X气体的浓度为3mol/L,在恒温下将该容器体积扩大一倍,再次达到平衡时,测得X气体的浓度为1.4mol/L,则下列叙述不正确的是
cZ(g),达到平衡时测得X气体的浓度为3mol/L,在恒温下将该容器体积扩大一倍,再次达到平衡时,测得X气体的浓度为1.4mol/L,则下列叙述不正确的是
 cZ(g),达到平衡时测得X气体的浓度为3mol/L,在恒温下将该容器体积扩大一倍,再次达到平衡时,测得X气体的浓度为1.4mol/L,则下列叙述不正确的是
cZ(g),达到平衡时测得X气体的浓度为3mol/L,在恒温下将该容器体积扩大一倍,再次达到平衡时,测得X气体的浓度为1.4mol/L,则下列叙述不正确的是| A.a+b<c | B.平衡向生成Z的方向移动 |
| C.Z的体积分数降低 | D.Y的转化率升高 |
您最近一年使用:0次
名校
5 . 在密闭容器中的一定量混合气体发生反应xM (g)+yN(g) zP(g)。平衡时测得M的浓度为0.80 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0.50 mol/L。下列有关判断正确的是
zP(g)。平衡时测得M的浓度为0.80 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0.50 mol/L。下列有关判断正确的是
 zP(g)。平衡时测得M的浓度为0.80 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0.50 mol/L。下列有关判断正确的是
zP(g)。平衡时测得M的浓度为0.80 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0.50 mol/L。下列有关判断正确的是| A.x + y < z | B.平衡向正反应方向移动 |
| C.N的转化率降低 | D.混合气体的密度不变 |
您最近一年使用:0次
2019-10-23更新
|
115次组卷
|
3卷引用:重庆文理学院附属中学校2022-2023学年高二上学期第一次月考化学试题
名校
6 . 下列事实中,不能用 勒夏特列原理解释的是
①Fe(SCN)3溶液中加入固体KSCN后颜色变深②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 ③实验室常用排饱和食盐水的方法收集氯气 ④棕红色NO2加压后颜色先变深后变浅 ⑤加入催化剂有利于合成氨的反应 ⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深 ⑦500℃时比室温更有利于合成氨的反应 ⑧将混合气体中的氨液化有利于合成氨反应
①Fe(SCN)3溶液中加入固体KSCN后颜色变深②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 ③实验室常用排饱和食盐水的方法收集氯气 ④棕红色NO2加压后颜色先变深后变浅 ⑤加入催化剂有利于合成氨的反应 ⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深 ⑦500℃时比室温更有利于合成氨的反应 ⑧将混合气体中的氨液化有利于合成氨反应
| A.①②⑥⑧ | B.①③⑤⑦ | C.②⑤⑥⑦ | D.②③⑦⑧ |
您最近一年使用:0次
2019-10-12更新
|
601次组卷
|
14卷引用:三峡名校联盟2021-2022学年高二上学期联考化学试题
三峡名校联盟2021-2022学年高二上学期联考化学试题甘肃省兰州市第一中学2019-2020学年高二9月月考化学试题浙江省东阳中学2019-2020学年高二上学期期中考试化学试题浙江省金华市江南中学高二上学期12月月考化学试题江西省高安中学2019-2020学年高二上学期期末考试化学(B卷)试题(已下线)【浙江新东方】44.(已下线)【浙江新东方】97浙江省宁波市咸祥中学2021-2022学年高二上学期期中考试化学试题天津市实验中学滨海学校2021-2022学年高二上学期期中质量监测化学试题浙江省玉环市玉城中学2022-2023学年高二上学期第一次月考化学试题 广东省广州市第一中学2022-2023学年高二上学期期末考试化学试题甘肃省武威、张掖两地2022-2023学年高二上学期11月期中考试化学试题辽宁省沈阳市第十五中学2023-2024学年高二上学期10月月考化学试题广东省化州市第一中学2023-2024学年高二上学期12月质量检测化学试卷
7 . 处理、回收CO是环境科学家研究的热点课题。
(1)CO用于处理犬气污染物N2O所发生的反应为:N2O(g)+CO(g) CO2(g)+N2(g)ΔH,几种物质的相对能量如下:
CO2(g)+N2(g)ΔH,几种物质的相对能量如下:
①ΔH=______ kJ·mol-1;改变下列“量”,一定会引起ΔH发生变化的是____ 填代号)
A.反应物浓度B.催化剂C.化学计量数
②有人提出上述反应可以用Fe作催化剂。其总反应分两步进行:第一步:Fe+N2O=FeO+N2,第二步:______ (写化学方程式)。第二步反应不影响总反应达到平衡所用时间,由此推知,第二步反应活化能____ 第一步反应活化能(填“大于”、“小于”或等于”)。
(2)在实验室,采用I2O5测定空气中CO的含量。在密闭容器中充入足量的I2O5粉末和一定量的CO,发生反应:I2O5(g)+5CO(g) 5CO2(g)+I2(s)。测得CO的转化率如图1所示。
5CO2(g)+I2(s)。测得CO的转化率如图1所示。
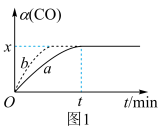
①相对曲线a,曲线b仅改变一个条件,改变的条件可能是______ 。
②在此温度下,该可逆反应的平衡常数K=_____ (用含x的代数式表示)。
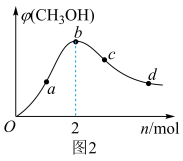
(3)工业上,用CO和H2合成CH3OH。在1L恒容密闭容器中充入1 mol CO(g)和n mol H2,在250℃发生反应:CO(g)+2H2(g) CH3OH(g),测得混合气体中CH3OH的体积分数与H2的物质的量的关系如图2所示。在a、b、c、d点中,CO的平衡转化率最大的点是
CH3OH(g),测得混合气体中CH3OH的体积分数与H2的物质的量的关系如图2所示。在a、b、c、d点中,CO的平衡转化率最大的点是___ 。
(4)CO-空气碱性燃料电池(用KOH作电解质),当恰好完全生成KHCO3时停止放电。写出此时负极的电极反应式:______ 。
(1)CO用于处理犬气污染物N2O所发生的反应为:N2O(g)+CO(g)
 CO2(g)+N2(g)ΔH,几种物质的相对能量如下:
CO2(g)+N2(g)ΔH,几种物质的相对能量如下:| 物质 | N2O(g) | CO(g) | CO2(g) | N2(g) |
| 相对能量kJ·mol-1 | 475.5 | 283 | 0 | 393.5 |
①ΔH=
A.反应物浓度B.催化剂C.化学计量数
②有人提出上述反应可以用Fe作催化剂。其总反应分两步进行:第一步:Fe+N2O=FeO+N2,第二步:
(2)在实验室,采用I2O5测定空气中CO的含量。在密闭容器中充入足量的I2O5粉末和一定量的CO,发生反应:I2O5(g)+5CO(g)
 5CO2(g)+I2(s)。测得CO的转化率如图1所示。
5CO2(g)+I2(s)。测得CO的转化率如图1所示。
①相对曲线a,曲线b仅改变一个条件,改变的条件可能是
②在此温度下,该可逆反应的平衡常数K=
(3)工业上,用CO和H2合成CH3OH。在1L恒容密闭容器中充入1 mol CO(g)和n mol H2,在250℃发生反应:CO(g)+2H2(g)
 CH3OH(g),测得混合气体中CH3OH的体积分数与H2的物质的量的关系如图2所示。在a、b、c、d点中,CO的平衡转化率最大的点是
CH3OH(g),测得混合气体中CH3OH的体积分数与H2的物质的量的关系如图2所示。在a、b、c、d点中,CO的平衡转化率最大的点是
(4)CO-空气碱性燃料电池(用KOH作电解质),当恰好完全生成KHCO3时停止放电。写出此时负极的电极反应式:
您最近一年使用:0次
2019-09-15更新
|
319次组卷
|
2卷引用:重庆市第一中学2020届高三上学期摸底考试理科综合化学试题
解题方法
8 . 甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)⇌CH3OH(g)△H1
②CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)⇌CO(g)+H2O(g)△H3
回答下列问题:
(1)已知△H1=﹣99kJ·mol﹣1,已知△H2=﹣58kJ·mol﹣1,则△H3=______ kJ·mol﹣1。
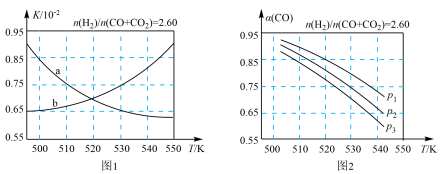
(2)反应①的化学平衡常数K的表达式为______ ;图1中能正确反映平衡常数K随温度变化关系的曲线为________ (填曲线标记字母)。
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率(a)与温度和压强的关系如图2所示。a(CO)值随温度升高而________ (填“增大”或“减小”)图2中的压强由大到小为________ 。
①CO(g)+2H2(g)⇌CH3OH(g)△H1
②CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)⇌CO(g)+H2O(g)△H3
回答下列问题:
(1)已知△H1=﹣99kJ·mol﹣1,已知△H2=﹣58kJ·mol﹣1,则△H3=
(2)反应①的化学平衡常数K的表达式为
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率(a)与温度和压强的关系如图2所示。a(CO)值随温度升高而

您最近一年使用:0次
2019-06-14更新
|
242次组卷
|
2卷引用:重庆市第三十中学2018-2019学年高二下学期期中考试化学试题
名校
9 . 将1 mol N2、3 mol H2放入恒温恒容的密闭容器中,在一定温度下发生如下反应并达到平衡:N2(g)+3H2(g)⇌2NH3(g)。在t0时刻,再往容器中充入2 mol NH3,一定时间后重新达到平衡。能正确表征上述过程的图象是
A. | B.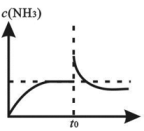 |
C. | D.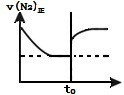 |
您最近一年使用:0次
2019-01-28更新
|
200次组卷
|
3卷引用:重庆市暨华中学校2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
10 . 氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为:N2(g)+3H2(g) 2NH3(g) △H
2NH3(g) △H
(1)已知破坏1mol共价键需要的能量如表所示
则△H=__________ 。
(2)在恒温、恒压容器中,按体积比1:3加入N2和H2进行合成氨反应,达到平衡后,再向容器中充入适量氨气,达到新平衡时,c(H2)将__________ (填“增大”、“减小”、或“不变”,后同);若在恒温、恒容条件下c(N2)/c(NH3)将________ 。
(3)在不同温度、压强和使用相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol 时,平衡混合物中氨的体积分数(φ)如图所示。_______ ,原因是___________________ 。
②若在250℃、p1条件下,反应达到平衡时的容器体积为1L,则该条件下合成氨的平衡常数K=____ (结果保留两位小数)。
(4)H2NCOONH4是工业由氨气合成尿素的中间产物。在一定温度下、体积不变的密闭容器中发生反应H2NCOONH4(s) 2NH3(g)+CO2(g),能说明该反应达到平衡状态的是
2NH3(g)+CO2(g),能说明该反应达到平衡状态的是_____ (填序号)
①每生成34g NH3的同时消耗44g CO2 ②混合气体的密度保持不变
③NH3的体积分数保持不变 ④混合气体的平均相对分子质量不变 ⑤c(NH3):c(CO2)=2:1
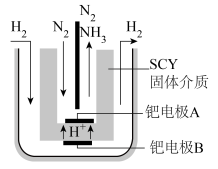
(5)科学家发现,N2和H2组成的原电池合成氨与工业合成氨相比具有效率高,条件易达到等优点。其装置如图所示、写出该原电池的电极反应:________________ 、_____________ ,若N2来自于空气,当电极B到A间通过2molH+时理论上需要标况下空气的体积为_________ (结果保留两位小数)。
 2NH3(g) △H
2NH3(g) △H(1)已知破坏1mol共价键需要的能量如表所示
| H-H | N-H | N-N | N≡N |
| 435.5kJ | 390.8kJ | 163kJ | 945.8kJ |
(2)在恒温、恒压容器中,按体积比1:3加入N2和H2进行合成氨反应,达到平衡后,再向容器中充入适量氨气,达到新平衡时,c(H2)将
(3)在不同温度、压强和使用相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol 时,平衡混合物中氨的体积分数(φ)如图所示。
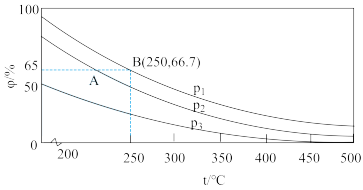
②若在250℃、p1条件下,反应达到平衡时的容器体积为1L,则该条件下合成氨的平衡常数K=
(4)H2NCOONH4是工业由氨气合成尿素的中间产物。在一定温度下、体积不变的密闭容器中发生反应H2NCOONH4(s)
 2NH3(g)+CO2(g),能说明该反应达到平衡状态的是
2NH3(g)+CO2(g),能说明该反应达到平衡状态的是①每生成34g NH3的同时消耗44g CO2 ②混合气体的密度保持不变
③NH3的体积分数保持不变 ④混合气体的平均相对分子质量不变 ⑤c(NH3):c(CO2)=2:1
(5)科学家发现,N2和H2组成的原电池合成氨与工业合成氨相比具有效率高,条件易达到等优点。其装置如图所示、写出该原电池的电极反应:
您最近一年使用:0次
2018-06-06更新
|
572次组卷
|
4卷引用:重庆市綦江中学2018届高三高考适应性考试化学试题



