1 . 在密闭容器中进行如下反应: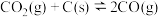
 ,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
(1)增加 的量,则平衡
的量,则平衡___________ (填“逆移”“正移”或“不移”,下同),
___________ (填“增大”“减小”或“不变”,下同)。
(2)恒温条件,增大反应容器的容积,则平衡___________ ,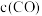
___________ (填“增大”“减小”或“不变”,下同)
(3)保持反应容器的容积和温度不变,通入He气,则平衡___________ ,
___________ 。
(4)保持反应容器的压强不变,通入Ar气,则平衡___________ ,
___________ 。
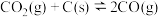
 ,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。(1)增加
 的量,则平衡
的量,则平衡
(2)恒温条件,增大反应容器的容积,则平衡
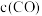
(3)保持反应容器的容积和温度不变,通入He气,则平衡

(4)保持反应容器的压强不变,通入Ar气,则平衡

您最近一年使用:0次
名校
解题方法
2 . 处理再利用 有多种方法。
有多种方法。
(1)碱法脱硫:
用 溶液吸收
溶液吸收 。已知:氢硫酸和碳酸的电离常数如表。
。已知:氢硫酸和碳酸的电离常数如表。
①用化学用语表示 溶液显碱性的原因:
溶液显碱性的原因:_______ 。
②用过量的 溶液吸收
溶液吸收 的离子方程式是
的离子方程式是_______ 。
(2)热分解法脱硫
在密闭容器中发生反应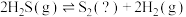 。其他条件不变时,
。其他条件不变时, 的平衡转化率随温度和压强的变化如图。
的平衡转化率随温度和压强的变化如图。
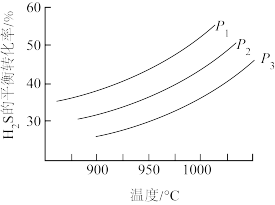
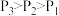 ,反应中
,反应中
_______ (填“是”或“不是”)气态,理由是_______ 。
(3)间接电解法脱硫
间接电解法脱硫过程的示意图如图。
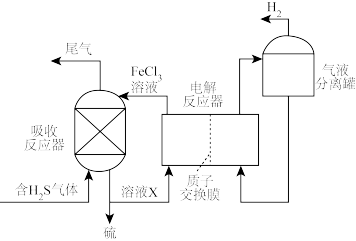
①溶液X的主要溶质是_______ 。
②简述在电解反应器中 溶液再生的原理:
溶液再生的原理:_______ 。
 有多种方法。
有多种方法。(1)碱法脱硫:
用
 溶液吸收
溶液吸收 。已知:氢硫酸和碳酸的电离常数如表。
。已知:氢硫酸和碳酸的电离常数如表。 |  | |
 | 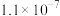 | 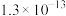 |
 | 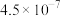 | 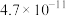 |
 溶液显碱性的原因:
溶液显碱性的原因:②用过量的
 溶液吸收
溶液吸收 的离子方程式是
的离子方程式是(2)热分解法脱硫
在密闭容器中发生反应
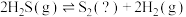 。其他条件不变时,
。其他条件不变时, 的平衡转化率随温度和压强的变化如图。
的平衡转化率随温度和压强的变化如图。
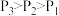 ,反应中
,反应中
(3)间接电解法脱硫
间接电解法脱硫过程的示意图如图。

①溶液X的主要溶质是
②简述在电解反应器中
 溶液再生的原理:
溶液再生的原理:
您最近一年使用:0次
2023-10-15更新
|
94次组卷
|
2卷引用:北京市第一○一中学2023-2024学年高三上学期10月月考化学试题
3 . 回答下列问题。
(1)某学习小组同学研究过氧化氢溶液与氢碘酸反应,查到一组室温下的实验数据,如下表所示:
回答下列问题:
①过氧化氢与氢碘酸反应的化学方程式为___________ 。
②该反应的速率方程可表示为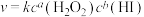 ,对比表中数据可知a=
,对比表中数据可知a=___________ ,b=___________ 。
③该小组同学将实验④的温度升高,发现加热到一定温度下,溶液出现棕黄色所需时间变长,可能的原因是___________ 。
(2)工业上用CH4催化还原NO2可以消除氮氧化物的污染,反应原理为:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH=-867.0 kJ·mol-1。一定比例的甲烷和二氧化氮的混合气在装有催化剂的反应器中反应一段时间。体系中二氧化氮的转化率和催化剂的催化活性与温度的关系如图所示。
N2(g)+CO2(g)+2H2O(g) ΔH=-867.0 kJ·mol-1。一定比例的甲烷和二氧化氮的混合气在装有催化剂的反应器中反应一段时间。体系中二氧化氮的转化率和催化剂的催化活性与温度的关系如图所示。
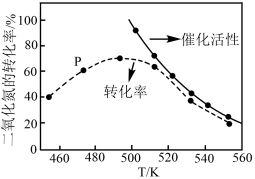
①温度为470K时,图中P点___________ (填“处于”或“不处于”)平衡状态。判断理由是___________ 。490K之后,二氧化氮的转化率随温度升高而减小的原因可能是___________ 。
A.催化剂的活性降低 B.平衡常数变大 C.反应活化能增大
②为提高反应中的二氧化氮的转化率,有人提出可以采取在恒压条件下充入稀有气体,解释其原因:___________ 。
(1)某学习小组同学研究过氧化氢溶液与氢碘酸反应,查到一组室温下的实验数据,如下表所示:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(H2O2) mol/L | 0.1 | 0.1 | 0.1 | 0.2 | 0.3 |
| c(HI) mol/L | 0.1 | 0.2 | 0.3 | 0.1 | 0.1 |
| 从混合至溶液出现棕黄色的时间/s | 13 | 6.5 | 4.3 | 6.6 | 4.4 |
①过氧化氢与氢碘酸反应的化学方程式为
②该反应的速率方程可表示为
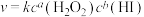 ,对比表中数据可知a=
,对比表中数据可知a=③该小组同学将实验④的温度升高,发现加热到一定温度下,溶液出现棕黄色所需时间变长,可能的原因是
(2)工业上用CH4催化还原NO2可以消除氮氧化物的污染,反应原理为:CH4(g)+2NO2(g)
 N2(g)+CO2(g)+2H2O(g) ΔH=-867.0 kJ·mol-1。一定比例的甲烷和二氧化氮的混合气在装有催化剂的反应器中反应一段时间。体系中二氧化氮的转化率和催化剂的催化活性与温度的关系如图所示。
N2(g)+CO2(g)+2H2O(g) ΔH=-867.0 kJ·mol-1。一定比例的甲烷和二氧化氮的混合气在装有催化剂的反应器中反应一段时间。体系中二氧化氮的转化率和催化剂的催化活性与温度的关系如图所示。
①温度为470K时,图中P点
A.催化剂的活性降低 B.平衡常数变大 C.反应活化能增大
②为提高反应中的二氧化氮的转化率,有人提出可以采取在恒压条件下充入稀有气体,解释其原因:
您最近一年使用:0次
2023-10-10更新
|
168次组卷
|
2卷引用:黑龙江省双鸭山市第一中学2023-2024学年高二上学期10月月考化学试题
23-24高二上·全国·课时练习
4 . 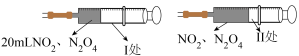
注射器活塞往里推到Ⅱ处时,为什么管内气体的颜色先变深又逐渐变浅________ ?由此得出的实验结论是什么________ ?

注射器活塞往里推到Ⅱ处时,为什么管内气体的颜色先变深又逐渐变浅
您最近一年使用:0次
23-24高二上·全国·课时练习
5 . 改变压强平衡一定移动吗________ ?
您最近一年使用:0次
23-24高二上·全国·课时练习
6 . 对于反应:FeCl3(aq)+3KSCN(aq) Fe(SCN)3(aq)+3KCl(aq)增大体系的压强,平衡是否发生移动
Fe(SCN)3(aq)+3KCl(aq)增大体系的压强,平衡是否发生移动________ ?为什么________ ?
 Fe(SCN)3(aq)+3KCl(aq)增大体系的压强,平衡是否发生移动
Fe(SCN)3(aq)+3KCl(aq)增大体系的压强,平衡是否发生移动
您最近一年使用:0次
23-24高二上·全国·课时练习
7 . 对于反应H2(g)+I2(g) 2HI(g),增大压强,平衡是否发生移动
2HI(g),增大压强,平衡是否发生移动________ ?为什么________ ?
 2HI(g),增大压强,平衡是否发生移动
2HI(g),增大压强,平衡是否发生移动
您最近一年使用:0次
23-24高二上·全国·课时练习
8 . 注射器活塞往外拉到Ⅲ处时,为什么管内气体的颜色先变浅又逐渐变深________ ?由此得出的实验结论是什么________ ?
您最近一年使用:0次
名校
9 . 乙酸制氢具有重要意义,同时可能发生的反应如下:
热裂解反应: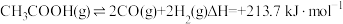
脱羧基反应:
完成下列问题:
(1)乙酸制氢时选择___________ (填“高压”或“常压”)有利于提高转化率。
(2)乙酸制直时温度与气体产率关系如图所示。
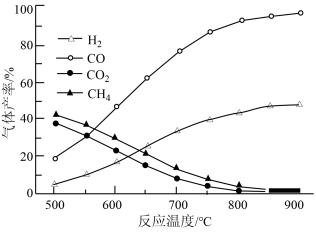
约650℃之前,脱羧基反应活化能低,速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随若温度升高,热裂解反应速率加快,且___________ 。
(3)保持其他条件不变,在乙酸气中掺杂一定量水蒸气,氢气产率显著提高而CO的产率下降,请分析原因:___________ 。
热裂解反应:
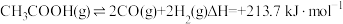
脱羧基反应:

完成下列问题:
(1)乙酸制氢时选择
(2)乙酸制直时温度与气体产率关系如图所示。

约650℃之前,脱羧基反应活化能低,速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随若温度升高,热裂解反应速率加快,且
(3)保持其他条件不变,在乙酸气中掺杂一定量水蒸气,氢气产率显著提高而CO的产率下降,请分析原因:
您最近一年使用:0次
10 . 甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇。发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) ΔH1=-99 kJ·mol-1
CH3OH(g) ΔH1=-99 kJ·mol-1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol-1
CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol-1
③CO2(g)+H2(g) CO(g)+H2O(g) ΔH3=+41 kJ·mol-1
CO(g)+H2O(g) ΔH3=+41 kJ·mol-1
回答下列问题:
(1)反应①的化学平衡常数K的表达式为___________ ;图1中能正确反映平衡常数K随温度变化关系的曲线为___________ (填曲线标记字母),其判断理由是___________ 。

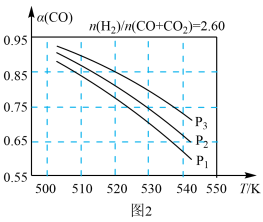
(2)合成气组成 =2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而
=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而___________ (填“增大”或“减小”),其原因是___________ ;图2中的压强由大到小为___________ ,其判断理由是___________ 。
①CO(g)+2H2(g)
 CH3OH(g) ΔH1=-99 kJ·mol-1
CH3OH(g) ΔH1=-99 kJ·mol-1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol-1
CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol-1③CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH3=+41 kJ·mol-1
CO(g)+H2O(g) ΔH3=+41 kJ·mol-1回答下列问题:
(1)反应①的化学平衡常数K的表达式为

(2)合成气组成
 =2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而
=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而
您最近一年使用:0次



