解题方法
1 . 下列图中的实验装置或操作表述合理的是
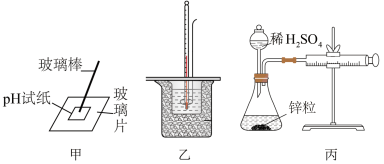



A.图甲:测定 溶液的 溶液的 |
B.图乙:测定稀盐酸和 溶液反应的中和热 溶液反应的中和热 |
C.图丙:测定锌粒与稀 反应的速率 反应的速率 |
| D.图丁:注射器活塞由Ⅱ推至Ⅰ处管内气体颜色变浅 |
您最近一年使用:0次
名校
2 . 反应
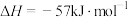 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是
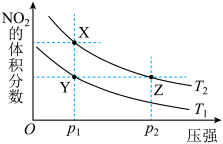

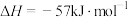 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是
A. | B.X、Y两点的反应速率:X>Y |
| C.X、Z两点气体的颜色:X比Z浅 | D.X、Z两点气体的平均相对分子质量:X>Z |
您最近一年使用:0次
2023-02-10更新
|
505次组卷
|
6卷引用:湖南省长沙市湖南师范大学附属中学2022-2023学年高二上学期期末考试化学试题
3 . 一定温度和压强下,在两个容积均为1L的密闭容器中,充入一定量的A和B,发生反应: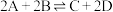 。相关反应数据如下表所示(已知在
。相关反应数据如下表所示(已知在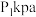 、
、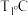 下,A、B、C、D都是气态)
下,A、B、C、D都是气态)
下列说法正确的是
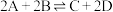 。相关反应数据如下表所示(已知在
。相关反应数据如下表所示(已知在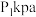 、
、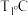 下,A、B、C、D都是气态)
下,A、B、C、D都是气态)| 容器编号 | 压强 | 温度 | 起始物质的量/mol | 10s时物质的量/mol | |
| A | B | C | |||
| Ⅰ | 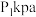 | 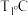 | 0.2 | 0.2 | 0.05 |
| Ⅱ | 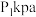 | 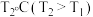 | 0.2 | 0.2 | 0.05 |
| Ⅲ |  | 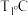 | 0.2 | 0.2 | 0.05 |
A.该反应的 |
| B.在容器Ⅲ中,A、B中至少有一种呈非气态 |
| C.10s时,容器Ⅱ中的反应一定处于平衡状态 |
D.若起始时,向容器II中充入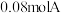 、 、 、 、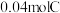 和 和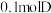 ,反应将向正反应方向进行 ,反应将向正反应方向进行 |
您最近一年使用:0次
4 . 二氧化碳催化加氢制甲醇,可减少CO2排放,并合成清洁能源。其反应可表示为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物
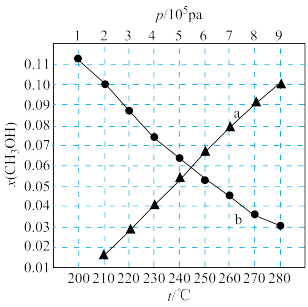
CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物 =3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
=3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
 CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物
CH3OH(g)+H2O(g) △H=-49kJ•mol-1,反应在起始物 =3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
=3时,在不同条件下达到平衡。设体系中甲醇的物质的量分数为χ(CH3OH),在t=250℃下的χ(CH3OH)~p、在p=5×105Pa下的χ(CH3OH)~t如图所示。下列说法不正确的是
A.该反应的平衡常数表达式为K=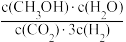 |
| B.图中对应等温过程的曲线是a |
| C.当χ(CH3OH)=0.10时,CO2的平衡转化率为33.3% |
| D.当χ(CH3OH)=0.10时,反应条件可能为2×105Pa、210℃或9×105Pa、280℃ |
您最近一年使用:0次
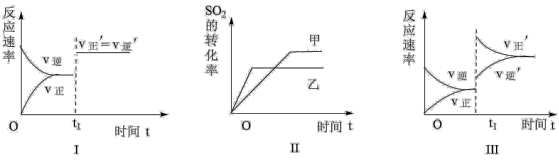
5 . 在容积不变的密闭容器中存在如下反应2SO2(g)+O2(g) 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
| A.图I表示的是t1时刻加入催化剂后对反应速率的影响 |
| B.图II表示的是压强对化学平衡的影响,且乙的压强较高 |
| C.图II表示的是温度对化学平衡的影响,且乙的温度较高 |
| D.图III表示的是t1时刻增大O2的浓度对反应速率的影响 |
您最近一年使用:0次
2022-10-25更新
|
142次组卷
|
4卷引用:湖南省张家界市2021-2022学年高二下学期期末考试化学试题
名校
6 . 在恒容密闭容器中通入CH4与CO2,使其物质的量浓度均为1.0mol•L-1,在一定条件下发生反应:CO2(g)+CH4(g) 2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图所示。下列说法一定正确的是
2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图所示。下列说法一定正确的是

 2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图所示。下列说法一定正确的是
2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图所示。下列说法一定正确的是
| A.a点时CH4的转化率为80% |
| B.压强力p1、p2、p3由小到大的顺序为p3<p2<p1 |
C.压强为p2时,b点处 正< 正< 逆 逆 |
| D.该反应的△H>0 |
您最近一年使用:0次
名校
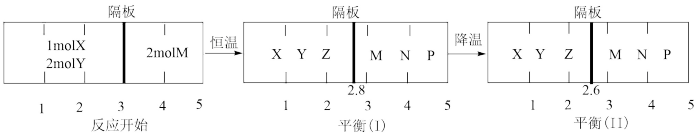
7 . 可逆反应① 、②
、② 分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
下列说法正确的是
 、②
、② 分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
下列说法正确的是
| A.反应①的正反应是吸热反应 |
| B.达平衡(I)时体系的压强与反应开始时体系的压强之比为10:11 |
| C.达平衡(I)时,X的转化率为5/11 |
| D.在平衡(I)和平衡(Ⅱ)中M的物质的量分数相等 |
您最近一年使用:0次
名校
8 . 一定温度下,在容积恒为1L的容器中通入一定量N2O4,发生反应N2O4(g) 2NO2(g) ΔH>0,体系中各组分浓度随时间(t)的变化如下表。
2NO2(g) ΔH>0,体系中各组分浓度随时间(t)的变化如下表。
下列说法正确的是
 2NO2(g) ΔH>0,体系中各组分浓度随时间(t)的变化如下表。
2NO2(g) ΔH>0,体系中各组分浓度随时间(t)的变化如下表。| t/s | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/(mol/L) | 0.100 | 0.062 | 0.048 | 0.040 | 0.040 |
| c(NO2)/(mol/L) | 0 | 0.076 | 0.104 | 0.120 | 0.120 |
| A.0~60s,N2O4的平均反应速率为v=0.06mol/(L·min) |
| B.升高温度,反应的化学平衡常数值减小 |
| C.80s时,再充入NO2、N2O4各0.12mol,平衡不移动 |
| D.若压缩容器使压强增大,达新平衡后混合气颜色比原平衡时浅 |
您最近一年使用:0次
名校
9 . 下列图示与对应叙述相符的是
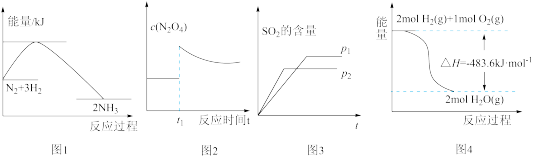

| A.图1反应达平衡后,升高温度,平衡常数K值减小 |
B.图2表示平衡2NO2(g) N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 |
C.图3表示可逆反应“2SO2+O2 2SO3”中SO2的含量与压强的关系,且P2>P1 2SO3”中SO2的含量与压强的关系,且P2>P1 |
| D.图4表示H2与O2发生反应过程中的能量变化,则H2的燃烧热ΔH=-241.8kJ•mol-1 |
您最近一年使用:0次
2022-09-27更新
|
328次组卷
|
3卷引用:湖南省邵阳市第二中学2022-2023学年高二上学期期中考试化学试题
10 . 对于平衡体系mA(g)+nB(g) pC(g)+qD(g) △H<0。下列结论正确的是
pC(g)+qD(g) △H<0。下列结论正确的是
 pC(g)+qD(g) △H<0。下列结论正确的是
pC(g)+qD(g) △H<0。下列结论正确的是| A.若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n>p+q |
| B.若m+n=p+q,则向含有amol气体的平衡体系中再加入amol的B,达到新平衡时气体的总物质的量等于2amol |
| C.若平衡时,A.B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| D.温度升高时,K值增大 |
您最近一年使用:0次



