名校
解题方法
1 . 二甲醚( )既是一种有机燃料,又是一种重要的有机化工原料。利用
)既是一种有机燃料,又是一种重要的有机化工原料。利用 催化氢化制备二甲醚的反应原理如下:
催化氢化制备二甲醚的反应原理如下:
Ⅰ.

Ⅱ.

Ⅲ.

下表是几种物质的标准生成热(由对应稳定单质生成1mol某种物质的焓变叫做该物质的标准生成热)。
回答下列问题:
(1)
___________ ;反应Ⅱ的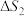
___________ (填“>”“=”或“<”)0。
(2) ℃下,向1L刚性密闭容器中投入2mol
℃下,向1L刚性密闭容器中投入2mol  ,只发生反应Ⅲ,t s时达到平衡,此时
,只发生反应Ⅲ,t s时达到平衡,此时 的转化率为
的转化率为 。
。
①下列叙述能说明反应Ⅲ已经达到平衡的是___________ (填选项字母)。
a.混合气体密度不再发生变化 b.容器内压强不再发生变化
c. 的消耗速率等于
的消耗速率等于 的消耗速率 d.
的消耗速率 d. 的体积分数不再发生变化
的体积分数不再发生变化
②若向该容器中再加入2mol ,重新达到平衡时所需时间
,重新达到平衡时所需时间___________ (填“>”“=”或“<”)t s,此时 的体积分数为
的体积分数为___________ (用含 的代数式表示)。
的代数式表示)。
③在催化剂条件下反应Ⅲ的反应过程如下图所示,“*”表示吸附在催化剂上。___________ (填“第一步”或“第二步”),判断的理由是__________________ 。
(3) ℃下,向压强恒定为p kPa的某密闭容器中按1∶3投入
℃下,向压强恒定为p kPa的某密闭容器中按1∶3投入 和
和 发生上述反应,平衡时
发生上述反应,平衡时 的转化率为60%,
的转化率为60%, (g)的体积分数为25%。则平衡时
(g)的体积分数为25%。则平衡时 的体积分数为
的体积分数为___________ (保留3位有效数字);该温度下反应Ⅰ的压强平衡常数
___________ (用含p的代数式表示) 。
。
 )既是一种有机燃料,又是一种重要的有机化工原料。利用
)既是一种有机燃料,又是一种重要的有机化工原料。利用 催化氢化制备二甲醚的反应原理如下:
催化氢化制备二甲醚的反应原理如下:Ⅰ.


Ⅱ.


Ⅲ.


下表是几种物质的标准生成热(由对应稳定单质生成1mol某种物质的焓变叫做该物质的标准生成热)。
| 物质 |  (g) (g) |  (g) (g) |  (g) (g) |  (g) (g) |
标准生成热/( ) ) | 0 | -201.3 | -241.3 | -184.3 |
(1)

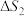
(2)
 ℃下,向1L刚性密闭容器中投入2mol
℃下,向1L刚性密闭容器中投入2mol  ,只发生反应Ⅲ,t s时达到平衡,此时
,只发生反应Ⅲ,t s时达到平衡,此时 的转化率为
的转化率为 。
。①下列叙述能说明反应Ⅲ已经达到平衡的是
a.混合气体密度不再发生变化 b.容器内压强不再发生变化
c.
 的消耗速率等于
的消耗速率等于 的消耗速率 d.
的消耗速率 d. 的体积分数不再发生变化
的体积分数不再发生变化②若向该容器中再加入2mol
 ,重新达到平衡时所需时间
,重新达到平衡时所需时间 的体积分数为
的体积分数为 的代数式表示)。
的代数式表示)。③在催化剂条件下反应Ⅲ的反应过程如下图所示,“*”表示吸附在催化剂上。
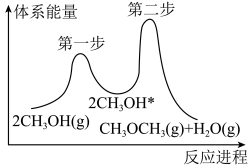
(3)
 ℃下,向压强恒定为p kPa的某密闭容器中按1∶3投入
℃下,向压强恒定为p kPa的某密闭容器中按1∶3投入 和
和 发生上述反应,平衡时
发生上述反应,平衡时 的转化率为60%,
的转化率为60%, (g)的体积分数为25%。则平衡时
(g)的体积分数为25%。则平衡时 的体积分数为
的体积分数为
 。
。
您最近一年使用:0次
7日内更新
|
193次组卷
|
2卷引用:河北省张家口市尚义县第一中学等校2023-2024学年高三下学期4月模拟测试化学试题
2 . 烯丙醇是生产甘油、医药、农药、香料和化妆品的中间体。已知烯丙醇与水在一定条件下发生加成反应的原理如下:
Ⅰ:CH2=CHCH2OH(g)+H2O(g) HOCH2CH2CH2OH(g) △H1 △S1
HOCH2CH2CH2OH(g) △H1 △S1
Ⅱ:CH2=CHCH2OH(g)+H2O(g) CH3CH(OH)CH2OH(g) △H2
CH3CH(OH)CH2OH(g) △H2
已知:相关物质在298K时的标准摩尔生成焓(101kPa时,该温度下由最稳定单质生成1 mol某纯物质的焓变)如下表所示:
(1)△H2=_______ kJ/mol;反应CH2=CHCH2OH(g)+H2O(g) HOCH2CH2CH2OH(l)的熵变为△S1',则△S1
HOCH2CH2CH2OH(l)的熵变为△S1',则△S1_______ △S1' (填“>”“=”或“<”)。
(2)若向绝热恒容容器中加入CH2=CHCH2OH(g)和H2O(g),发生反应Ⅰ和Ⅱ,下列事实不能说明体系达到平衡状态的是_______(填选项字母)。
(3)已知:反应的压强平衡常数(K)满足方程Kp=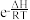 +C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为
+C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为_______ 和_______ 。
①该温度下,反应Ⅱ的压强平衡常数K=_______ 。
②若其他条件不变,初始时不充入He(g),而是按1:1的体积比充入CH2=CHCH2OH(g)和H2O(g),达到新平衡时,H2O(g)的转化率将_______ (填“增大”“减小”或“不变”),解释其原因为_______ 。
(5)烯丙醇的电氧化过程有重要应用。其在阳极放电时,同时存在三种电极反应(烯丙醇→丙烯酸、烯丙醇→丙烯醛、烯丙醇→丙二酸),各反应决速步骤的活化能如下表所示。
①该条件下,相同时间内,阳极产物中含量最多的为_______ 。
②碱性条件下,烯丙醇在电极上生成丙烯醛(CH2=CHCHO)的电极反应式为_______ 。
Ⅰ:CH2=CHCH2OH(g)+H2O(g)
 HOCH2CH2CH2OH(g) △H1 △S1
HOCH2CH2CH2OH(g) △H1 △S1Ⅱ:CH2=CHCH2OH(g)+H2O(g)
 CH3CH(OH)CH2OH(g) △H2
CH3CH(OH)CH2OH(g) △H2 已知:相关物质在298K时的标准摩尔生成焓(101kPa时,该温度下由最稳定单质生成1 mol某纯物质的焓变)如下表所示:
| 物质 | CH2=CHCH2OH(g) | H2O(g) | HOCH2CH2CH2OH(g) | CH3CH(OH)CH2OH(g) |
| 标准摩尔生成焓/(kJ/mol) | -171.8 | -241.8 | -464.9 | -485.7 |
(1)△H2=
 HOCH2CH2CH2OH(l)的熵变为△S1',则△S1
HOCH2CH2CH2OH(l)的熵变为△S1',则△S1(2)若向绝热恒容容器中加入CH2=CHCH2OH(g)和H2O(g),发生反应Ⅰ和Ⅱ,下列事实不能说明体系达到平衡状态的是_______(填选项字母)。
| A.容器内气体的压强不变 | B.容器内温度不变 |
| C.容器内气体的密度不变 | D.容器内气体的平均相对分子质量不变 |
(3)已知:反应的压强平衡常数(K)满足方程Kp=
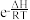 +C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为
+C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为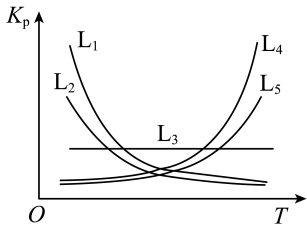
①该温度下,反应Ⅱ的压强平衡常数K=
②若其他条件不变,初始时不充入He(g),而是按1:1的体积比充入CH2=CHCH2OH(g)和H2O(g),达到新平衡时,H2O(g)的转化率将
(5)烯丙醇的电氧化过程有重要应用。其在阳极放电时,同时存在三种电极反应(烯丙醇→丙烯酸、烯丙醇→丙烯醛、烯丙醇→丙二酸),各反应决速步骤的活化能如下表所示。
| 反应 | 烯丙醇→丙烯酸 | 烯丙醇→丙烯醛 | 烯丙醇→丙二酸 |
| 活化能(单位:eV) | 8.6a | 2.5 a | 13.7a |
②碱性条件下,烯丙醇在电极上生成丙烯醛(CH2=CHCHO)的电极反应式为
您最近一年使用:0次
名校
解题方法
3 . 下列说法正确的是
| A.冰在室温下自动融化成水是熵增的过程 |
| B.能够自发进行的反应一定是放热反应 |
| C.能够自发进行的反应一定是熵增的过程 |
| D.△H<0的反应均是自发进行的反应 |
您最近一年使用:0次
解题方法
4 . 关于熵变和焓变的理解,下列说法正确的是
| A.绝热体系中,自发过程向着熵增方向进行 |
B.水凝结成冰的过程中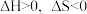 |
C.反应能否自发进行与温度有关,一般高温时 的影响为主 的影响为主 |
| D.能够自发进行的反应一定是放热的反应 |
您最近一年使用:0次
2023-12-23更新
|
125次组卷
|
2卷引用:河北省保定市高碑店市崇德实验中学2023-2024学年高三上学期1月考试化学试题
名校
5 . 下列说法正确的是
A.稀氨水中存在平衡NH3•H2O NH NH +OH-,若要使平衡逆向移动且c(OH-)增大,可加入NH4Cl固体 +OH-,若要使平衡逆向移动且c(OH-)增大,可加入NH4Cl固体 |
| B.某固体化合物M不导电,但熔融时能完全电离,则M一定是强电解质 |
| C.熵值增大的反应都能自发进行 |
D.溶液中存在平衡FeCl3+3KSCN Fe(SCN)3+3KCl,平衡时加入KCl固体时,平衡逆向移动 Fe(SCN)3+3KCl,平衡时加入KCl固体时,平衡逆向移动 |
您最近一年使用:0次
名校
6 . 下列说法中,正确的是
A. 晶体与 晶体与 晶体的反应吸热,因此该反应在室温下是非自发反应 晶体的反应吸热,因此该反应在室温下是非自发反应 |
B.某反应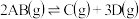 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的 |
| C.活化分子之间的碰撞一定是有效碰撞 |
D.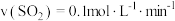 表示在 表示在 时, 时, 的浓度为 的浓度为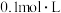 |
您最近一年使用:0次
解题方法
7 . 下列变化过程中, 的是
的是
 的是
的是| A.液氨汽化 |
| B.硫酸钾溶于水 |
C. 和 和 反应生成 反应生成 |
D.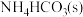 分解生成 分解生成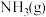 、 、 和 和 |
您最近一年使用:0次
2023-10-11更新
|
193次组卷
|
3卷引用:河北省部分学校2023-2024学年高二上学期10月联考化学试题
8 . 下列诗词中,包含 、
、 的化学变化的是
的化学变化的是
 、
、 的化学变化的是
的化学变化的是| A.日照香炉生紫烟,遥看瀑布挂前川 |
| B.美人首饰侯王印,尽是沙中浪底来 |
| C.日暮北风吹雨去,数峰清瘦出云来 |
| D.千锤万凿出深山,烈火焚烧若等闲 |
您最近一年使用:0次
2023-10-08更新
|
281次组卷
|
5卷引用:河北省泊头市第一中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
9 . 化学反应进行的方向是一个比较复杂的问题。下列有关说法正确的是
A.反应 的 的 |
B. 或 或 的反应一定能自发进行 的反应一定能自发进行 |
C.  在不同状态时的熵值: 在不同状态时的熵值: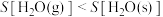 |
D.反应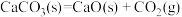  能否自发进行与温度有关 能否自发进行与温度有关 |
您最近一年使用:0次
2023-10-03更新
|
56次组卷
|
2卷引用:河北省邢台市五岳联盟2023-2024学年高二上学期第一次月考化学试题
名校
10 . 下列说法正确的是
| A.冰在室温下能自动融化成水,这是熵增的过程 |
| B.吸热反应一定不能自发进行 |
| C.非自发反应一定不能实现 |
D. , , 的反应,低温能自发进行 的反应,低温能自发进行 |
您最近一年使用:0次



