名校
1 . 下列实验操作、现象及结论均正确的是
| 操作 | 现象 | 结论 | |
| A | 向5mL0.1mol/L的AgNO3溶液中先滴加2mL0.1mol/L的NaCl溶液,再加入几滴0.1 mol/L的KI溶液 | 先生成白色沉淀,后转化为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 在蓝色CuCl2溶液中存在如下平衡:[Cu(H2O)4]2+(蓝色)+4Cl- [CuCl4]2-(黄色)+4H2O ΔH>0,加热该溶液 [CuCl4]2-(黄色)+4H2O ΔH>0,加热该溶液 | 溶液由蓝色转变为黄绿色 | 对于该反应,升高温度,平衡正向移动 |
| C | 用pH试纸分别测定相同浓度的CH3COONa溶液和NaClO溶液的pH | 测定CH3COONa溶液试纸颜色变化更深 | CH3COONa溶液水解程度更大 |
| D | 用pH计分别测定SO2和CO2饱和溶液的pH | SO2饱和溶液的pH小 | 酸性:H2SO3>H2CO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 乙酸,也叫醋酸,是我国应用最早、使用最多的酸味剂,同时也是一种重要的化工原料。请回答下列问题:
(1)可以使0.1
 的电离程度增大的是
的电离程度增大的是________ (填字母)。
A.加入少量0.1 的稀盐酸 B.加热该
的稀盐酸 B.加热该 溶液
溶液
C.加入少量纯 D.加水稀释至0.01
D.加水稀释至0.01
E.加入少量氯化钠晶体 F.加入少量0.1 的NaOH溶液
的NaOH溶液
(2)体积均为10mL、pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程的pH变化如图所示。

则相同条件下酸HX的电离平衡常数___________ (填“大于”“等于”或“小于”,下同)醋酸的电离平衡常数;在体积、pH均相同的 与一元酸HX中加入足量的锌,生成的氢气在相同条件下的体积大小关系:
与一元酸HX中加入足量的锌,生成的氢气在相同条件下的体积大小关系:
___________ HX。
(3)已知25℃时,两种酸的电离平衡常数如下表。
①在相同条件下,试比较 、
、 和
和 的酸性从强到弱顺序为
的酸性从强到弱顺序为___________ 。
②向 溶液中加入足量
溶液中加入足量 溶液,反应的离子方程式为
溶液,反应的离子方程式为___________ 。
(1)可以使0.1

 的电离程度增大的是
的电离程度增大的是A.加入少量0.1
 的稀盐酸 B.加热该
的稀盐酸 B.加热该 溶液
溶液C.加入少量纯
 D.加水稀释至0.01
D.加水稀释至0.01
E.加入少量氯化钠晶体 F.加入少量0.1
 的NaOH溶液
的NaOH溶液(2)体积均为10mL、pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程的pH变化如图所示。

则相同条件下酸HX的电离平衡常数
 与一元酸HX中加入足量的锌,生成的氢气在相同条件下的体积大小关系:
与一元酸HX中加入足量的锌,生成的氢气在相同条件下的体积大小关系:
(3)已知25℃时,两种酸的电离平衡常数如下表。
 |  | |
 | 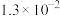 | 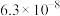 |
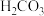 | 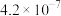 | 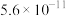 |
 、
、 和
和 的酸性从强到弱顺序为
的酸性从强到弱顺序为②向
 溶液中加入足量
溶液中加入足量 溶液,反应的离子方程式为
溶液,反应的离子方程式为
您最近一年使用:0次
名校
3 . 25℃时,下列各组离子在指定条件下一定不能大量共存的是
A.含有大量Fe3+的溶液中:H+、Na+、Cl-、NO |
B.能使酚酞变红的溶液中:Na+、Mg2+、HCO 、Cl- 、Cl- |
C.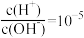 的溶液中:Na+、K+、OH-、NO 的溶液中:Na+、K+、OH-、NO |
D.pH<7的溶液中:Al3+、Ca2+、NO 、Cl- 、Cl- |
您最近一年使用:0次
2023-12-05更新
|
177次组卷
|
3卷引用:辽宁省抚顺市六校2023-2024学年高二上学期期中考试化学试题
名校
4 . 下列操作会使水的电离平衡向电离方向移动,且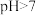 的是
的是
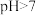 的是
的是| A.将纯水加热到80℃ | B.向水中加入少量的 |
C.向水中加入少量的 固体 固体 | D.向水中加入少量的 固体 固体 |
您最近一年使用:0次
2023-11-23更新
|
346次组卷
|
4卷引用:辽宁省辽东南协作校2023-2024学年高二上学期12月月考化学(A卷)试题
5 . 浓度均为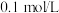 、体积均为
、体积均为 的
的 和
和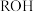 溶液,分别加水稀释至体积为V,
溶液,分别加水稀释至体积为V, 随
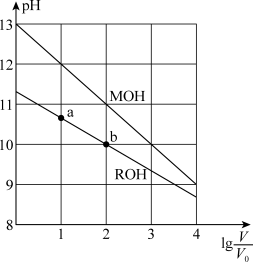
随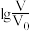 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
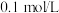 、体积均为
、体积均为 的
的 和
和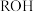 溶液,分别加水稀释至体积为V,
溶液,分别加水稀释至体积为V, 随
随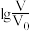 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
A. 的碱性弱于 的碱性弱于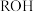 的碱性 的碱性 |
B.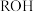 的电离程度:b点小于a点 的电离程度:b点小于a点 |
C.若两溶液无限稀释,则它们的 相等 相等 |
D.当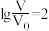 时,若两溶液同时升高温度,则 时,若两溶液同时升高温度,则 增大 增大 |
您最近一年使用:0次
2023-11-08更新
|
647次组卷
|
3卷引用:辽宁省县级重点高中协作体2023-2024学年高二上学期期中考试化学试题
名校
6 . 下列对生产、生活中事实的解释正确的是
| 选项 | 事实 | 解释 |
| A | 常温下,浓硫酸可以用铁罐储存 | 常温下,浓硫酸与铁不反应 |
| B | NO2、N2O4平衡混合气加压后气体颜色加深 | 加压后平衡向生成NO2的方向移动 |
| C | 合成氨工业使用铁触媒作催化剂 | 催化剂既能加快反应速率,又能提高氢气的平衡转化率 |
| D | 将pH=12的NaOH溶液由25℃加热至100℃后,pH变为10 | 温度升高,水的离子积常数增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-13更新
|
351次组卷
|
2卷引用:辽宁省名校联盟2023-2024学年高二上学期10月份联合考试化学试题
7 . 下列说法正确的是
A. 是强电解质,故 是强电解质,故 的电离方程式为 的电离方程式为 |
B.室温下, 的 的 溶液的 溶液的 ,则 ,则 的电离方程式为 的电离方程式为 |
C. 是酸式盐,故其电离方程式为 是酸式盐,故其电离方程式为 |
D. 的饱和水溶液导电性很弱,故 的饱和水溶液导电性很弱,故 的电离方程式为 的电离方程式为 |
您最近一年使用:0次
名校
解题方法
8 . 已知:25 ℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25 ℃时,取10 mL 0.1 mol·L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1 000 mL,溶液pH数值范围为___________ ,溶液中
___________ (填“增大”“减小”“不变”或“不能确定”)。
②氨水(NH3·H2O溶液)电离平衡常数表达式Kb=___________ ,25 ℃时,氨水电离平衡常数约为___________ 。
(2)25 ℃时,现向10 mL 0.1 mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中
___________ (填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)纯水在100℃时pH=6,该温度下1 mol•L﹣1的NaOH溶液中,由水电离出的c(OH﹣)=______ mol•L﹣1。该温度下pH=11的NaOH溶液与pH=1的HCl溶液等体积混合,则混合后溶液的pH为______ 。
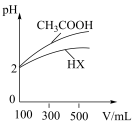
(4)体积均为100 mLpH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则相同温度时,HX的电离平衡常数___________ (填“大于”或“小于”或“等丁”)CH3COOH的电离平衡常数
(5)电离平衡常数是衡量弱电解质电离程度强弱的物理量。
已知:
则向NaCN溶液中通入少量的CO2,发生反应的化学方程式为___________ 。
(1)25 ℃时,取10 mL 0.1 mol·L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1 000 mL,溶液pH数值范围为

②氨水(NH3·H2O溶液)电离平衡常数表达式Kb=
(2)25 ℃时,现向10 mL 0.1 mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中

a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)纯水在100℃时pH=6,该温度下1 mol•L﹣1的NaOH溶液中,由水电离出的c(OH﹣)=
(4)体积均为100 mLpH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则相同温度时,HX的电离平衡常数

(5)电离平衡常数是衡量弱电解质电离程度强弱的物理量。
已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10﹣10 |
| CH3COOOH | K=1.8×10﹣5 |
| H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
您最近一年使用:0次
名校
9 . 常温下,在指定溶液中下列各组离子可能大量共存的是
A.滴加KSCN显红色的溶液: 、Cl-、K+、 、Cl-、K+、 |
| B.0.1mol·L−1KI溶液:Na+、K+、ClO−、OH− |
C.与铝粉反应放出H2的透明溶液:Cu2+、Na+、 、C1- 、C1- |
D. =10-12的溶液中:K+、 =10-12的溶液中:K+、 、Na+、C1- 、Na+、C1- |
您最近一年使用:0次
解题方法
10 . 下列实验操作或实验方案,能达到目的的是
选项 | 实验操作或实验方案 | 目的 |
A | 向有MnO2固体的圆底烧瓶中加入浓盐酸,产生的气体依次通过饱和食盐水和浓硫酸 | 制取并纯化氯气 |
B | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量BaCl2溶液 | 检验Na2SO3固体是否变质 |
C | 用湿润的淀粉碘化钾试纸检验某气体,试纸变蓝 | 证明该气体为Cl2 |
D | 将NaOH待测液滴在湿润的pH试纸上,与标准比色卡对照 | 测定NaOH溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



