1 . 下列溶液呈酸性的是
| A.NaCl溶液 | B.HCl溶液 | C.Ba(OH)2溶液 | D.NaOH溶液 |
您最近半年使用:0次
2 . 常温下,向一定质量的冰醋酸中加水稀释,溶液的导电能力变化如图。已知 ,
, 。下列说法正确的是
。下列说法正确的是
 ,
, 。下列说法正确的是
。下列说法正确的是
| A.a、b、c三点溶液的pH:b>a>c |
| B.a、b、c三点溶液中水的电离程度:a>b>c |
C.b→c过程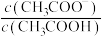 减小 减小 |
| D.向c点溶液中加入等浓度等体积的氮水,所得溶液呈中性 |
您最近半年使用:0次
名校
3 . 已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,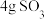 中含电子数为 中含电子数为 | B. 金属钠生成 金属钠生成 ,转移的电子数为 ,转移的电子数为 |
C. 的甲酸溶液中 的甲酸溶液中 数为 数为 | D.标准状况下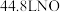 和 和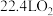 反应后的分子数为 反应后的分子数为 |
您最近半年使用:0次
4 . Ⅰ.太空很神秘,水的世界也深不可测,从水作溶剂、水分子运动到水的电离、水与活泼金属反应等等。结合书本知识,回答下列问题:
(1)标准状况下,0.01 的NaOH溶液的pH
的NaOH溶液的pH_______ (填“>”“<”或“=”,下同)12,该温度下,水的离子积常数
_______  。
。
(2)T℃下,水的离子积曲线如图所示。_______ (填字母)。
a.T℃小于25℃
b.A点溶液pH=8
c.B点溶液呈碱性
d.保持温度不变,加入少量的酸可以实现从B点到C点的变化
②该温度下,将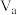 L pH=a NaOH溶液与
L pH=a NaOH溶液与 L
L 硫酸混合。
硫酸混合。
若所得混合溶液呈中性,且a=12,b=1,则
_______ ;若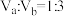 ,且a=11,b=3,则所得混合溶液的pH=
,且a=11,b=3,则所得混合溶液的pH=_______ 。
(3)现有以下五种电解质溶液,回答下列问题:
① ②NaOH ③
②NaOH ③ ④
④ ⑤
⑤
①浓度均为0.1 的五种溶液中导电能力最强的是
的五种溶液中导电能力最强的是_______ (填序号)。
②浓度均为0.1 的①②④三种溶液中由水电离出的氢离子浓度由大到小的排列顺序为
的①②④三种溶液中由水电离出的氢离子浓度由大到小的排列顺序为_______ (填序号)。
Ⅱ. 、
、 、
、 是中学化学中常见的物质,常温下,有关物质的电离常数如下表:
是中学化学中常见的物质,常温下,有关物质的电离常数如下表:
回答下列问题:
(4)常温下,下列事实能说明 是弱电解质的是
是弱电解质的是_______ (填写序号)
① 与水能以任意比互溶
与水能以任意比互溶
②0.1mol/L 溶液导电能力比0.1mol/L盐酸弱
溶液导电能力比0.1mol/L盐酸弱
③常温下pH=3的 溶液稀释十倍后pH<4
溶液稀释十倍后pH<4
④ 溶液能与
溶液能与 溶液反应放出
溶液反应放出
⑤向 溶液中加入
溶液中加入 固体,溶液pH增大
固体,溶液pH增大
⑥大小相同的锌片与同体积同浓度的盐酸和 反应,产生
反应,产生 的物质的量相同
的物质的量相同
(5)已知 ,则常温下
,则常温下
 溶液的pH=
溶液的pH=_______ 。用水缓慢稀释该氨水的过程中,溶液中随着水量的增加,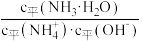
_______ 。(填“增大”“减小”或“不变”)
(1)标准状况下,0.01
 的NaOH溶液的pH
的NaOH溶液的pH
 。
。(2)T℃下,水的离子积曲线如图所示。
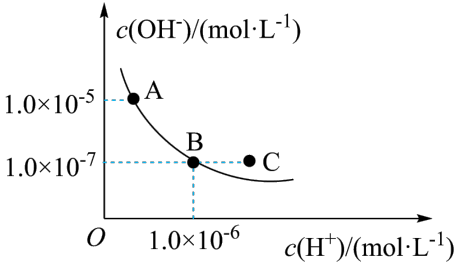
a.T℃小于25℃
b.A点溶液pH=8
c.B点溶液呈碱性
d.保持温度不变,加入少量的酸可以实现从B点到C点的变化
②该温度下,将
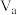 L pH=a NaOH溶液与
L pH=a NaOH溶液与 L
L 硫酸混合。
硫酸混合。若所得混合溶液呈中性,且a=12,b=1,则

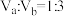 ,且a=11,b=3,则所得混合溶液的pH=
,且a=11,b=3,则所得混合溶液的pH=(3)现有以下五种电解质溶液,回答下列问题:
①
 ②NaOH ③
②NaOH ③ ④
④ ⑤
⑤
①浓度均为0.1
 的五种溶液中导电能力最强的是
的五种溶液中导电能力最强的是②浓度均为0.1
 的①②④三种溶液中由水电离出的氢离子浓度由大到小的排列顺序为
的①②④三种溶液中由水电离出的氢离子浓度由大到小的排列顺序为Ⅱ.
 、
、 、
、 是中学化学中常见的物质,常温下,有关物质的电离常数如下表:
是中学化学中常见的物质,常温下,有关物质的电离常数如下表:| 物质 |  |  |  |
| 电离常数 | 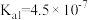 , ,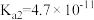 |  | 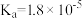 |
(4)常温下,下列事实能说明
 是弱电解质的是
是弱电解质的是①
 与水能以任意比互溶
与水能以任意比互溶②0.1mol/L
 溶液导电能力比0.1mol/L盐酸弱
溶液导电能力比0.1mol/L盐酸弱③常温下pH=3的
 溶液稀释十倍后pH<4
溶液稀释十倍后pH<4④
 溶液能与
溶液能与 溶液反应放出
溶液反应放出
⑤向
 溶液中加入
溶液中加入 固体,溶液pH增大
固体,溶液pH增大⑥大小相同的锌片与同体积同浓度的盐酸和
 反应,产生
反应,产生 的物质的量相同
的物质的量相同(5)已知
 ,则常温下
,则常温下
 溶液的pH=
溶液的pH=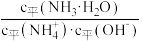
您最近半年使用:0次
5 . 下列物质呈碱性的是
物质 | 食醋 | 酱油 | 牛奶 | 肥皂水 |
| 2 | 5 | 7 | 10 |
| A.食醋 | B.酱油 | C.牛奶 | D.肥皂水 |
您最近半年使用:0次
解题方法
6 . 丙酸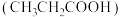 可用作食品防腐剂和防霉剂,能与水、乙醇等混溶。某同学为测定其电离常数做了如下实验:
可用作食品防腐剂和防霉剂,能与水、乙醇等混溶。某同学为测定其电离常数做了如下实验:
【实验一】配制丙酸溶液并用 溶液滴定测定丙酸的浓度。
溶液滴定测定丙酸的浓度。 丙酸溶液,用移液管移取
丙酸溶液,用移液管移取 丙酸溶液于锥形瓶中,加入几
丙酸溶液于锥形瓶中,加入几____________ 滴溶液作指示剂。
(2)取图中的滴定管____________ (填“a”或“b”),检查____________ 后,用蒸馏水洗涤,再用 的
的 标准溶液
标准溶液____________  次,完成后盛装好标准溶液,然后进行滴定,达到滴定终点时的操作和现象为
次,完成后盛装好标准溶液,然后进行滴定,达到滴定终点时的操作和现象为____________ 。
(3)重复滴定操作3次,每次消耗标准溶液的体积如下:
根据表中数据计算,所配丙酸溶液的物质的量浓度为____________  ;若读取滴定终点的数据时仰视读数,则造成所测丙酸溶液的浓度将
;若读取滴定终点的数据时仰视读数,则造成所测丙酸溶液的浓度将____________ (填“偏大”“偏小”或“无影响”)。
【实验二】常温下测定所配丙酸溶液的 。
。
(4)若用 试纸测定丙酸溶液的
试纸测定丙酸溶液的 ,写出简要操作:
,写出简要操作:____________ 。
(5)若用 计测得所配丙酸溶液的
计测得所配丙酸溶液的 为2.94,则常温下,丙酸的电离常数
为2.94,则常温下,丙酸的电离常数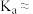
____________ 。
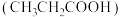 可用作食品防腐剂和防霉剂,能与水、乙醇等混溶。某同学为测定其电离常数做了如下实验:
可用作食品防腐剂和防霉剂,能与水、乙醇等混溶。某同学为测定其电离常数做了如下实验:【实验一】配制丙酸溶液并用
 溶液滴定测定丙酸的浓度。
溶液滴定测定丙酸的浓度。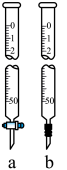
 丙酸溶液,用移液管移取
丙酸溶液,用移液管移取 丙酸溶液于锥形瓶中,加入几
丙酸溶液于锥形瓶中,加入几(2)取图中的滴定管
 的
的 标准溶液
标准溶液 次,完成后盛装好标准溶液,然后进行滴定,达到滴定终点时的操作和现象为
次,完成后盛装好标准溶液,然后进行滴定,达到滴定终点时的操作和现象为(3)重复滴定操作3次,每次消耗标准溶液的体积如下:
实验序号 | 1 | 2 | 3 |
消耗NaOH标准溶液的体积/mL | 24.98 | 25.00 | 25.02 |
 ;若读取滴定终点的数据时仰视读数,则造成所测丙酸溶液的浓度将
;若读取滴定终点的数据时仰视读数,则造成所测丙酸溶液的浓度将【实验二】常温下测定所配丙酸溶液的
 。
。(4)若用
 试纸测定丙酸溶液的
试纸测定丙酸溶液的 ,写出简要操作:
,写出简要操作:(5)若用
 计测得所配丙酸溶液的
计测得所配丙酸溶液的 为2.94,则常温下,丙酸的电离常数
为2.94,则常温下,丙酸的电离常数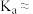
您最近半年使用:0次
7 . 常温下,下列离子组在指定溶液中能大量共存的是
A.使酚酞变红的溶液中: |
B.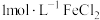 溶液中: 溶液中: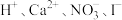 |
C.加入石蕊呈红色的溶液中: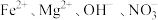 |
D. 的溶液中: 的溶液中: |
您最近半年使用:0次
8 . 在酸性环境中,纳米Fe/Ni复合材料去除污染水体的N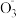 的反应过程(Ni不参与反应)如图所示,下列说法正确的是
的反应过程(Ni不参与反应)如图所示,下列说法正确的是
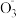 的反应过程(Ni不参与反应)如图所示,下列说法正确的是
的反应过程(Ni不参与反应)如图所示,下列说法正确的是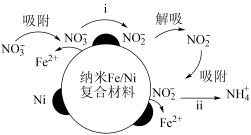
| A.反应步骤i中产生了气体 | B.反应步骤ⅱ不需要H+的参与 |
C.去除N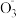 后的水体pH增大 后的水体pH增大 | D.处理过程中Fe/Ni复合材料作催化剂 |
您最近半年使用:0次
9 . 镀锌钢板广泛运用于汽车行业。当镀层质量不合格时,先利用强酸将镀件表面的镀锌层清洗,再检测其中含有的 、
、 、
、 等离子的浓度。
等离子的浓度。
(1)测定原理:EDTA(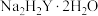 )可与
)可与 、
、 、
、 等多种金属离子形成络合物,如下表。其中
等多种金属离子形成络合物,如下表。其中 是乙二胺四乙酸根(
是乙二胺四乙酸根( )的简写。
)的简写。
①EDTA在水溶液中可看作“六元酸”的一种微粒可表示为___________ (用H、Y表示)。
②表中最稳定的金属络合物是___________ (填化学式)。
(2)测定过程:已知EDTA标准溶液滴定 的相关信息如下表:
的相关信息如下表:
可采用连续滴定法测定 、
、 、
、 的浓度,具体步骤如下:
的浓度,具体步骤如下:
I.先测定 (
( 、
、 不影响Fe3+的滴定):
不影响Fe3+的滴定):
请补充完整实验方案:
①按规定操作分别将0.01000 EDTA标准溶液和待测溶液[其中
EDTA标准溶液和待测溶液[其中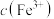 约为0.01
约为0.01 ]装入如图所示的滴定管中;
]装入如图所示的滴定管中;___________ 。(可选用的实验试剂有:磺基水杨酸、氨水溶液、盐酸溶液)
③实验测得 的浓度偏大,其原因可能是
的浓度偏大,其原因可能是___________ 。
II.再测定 :在
:在 的锥形瓶中继续加入适量过硫酸铵
的锥形瓶中继续加入适量过硫酸铵 ,轻微摇晃使
,轻微摇晃使 转化为
转化为 ,继续用EDTA标准溶液滴定到终点。写出
,继续用EDTA标准溶液滴定到终点。写出 转化为
转化为 的离子方程式:
的离子方程式:___________ 。
III.最后测定 :在
:在 的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用
的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用 标准溶液滴定到终点。
标准溶液滴定到终点。 不影响
不影响 滴定的原因是
滴定的原因是___________ 。
 、
、 、
、 等离子的浓度。
等离子的浓度。(1)测定原理:EDTA(
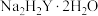 )可与
)可与 、
、 、
、 等多种金属离子形成络合物,如下表。其中
等多种金属离子形成络合物,如下表。其中 是乙二胺四乙酸根(
是乙二胺四乙酸根( )的简写。
)的简写。| 络合反应 | 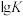 (K为平衡常数) |
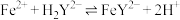 | 14.3 |
 | 16.5 |
 | 25.1 |
②表中最稳定的金属络合物是
(2)测定过程:已知EDTA标准溶液滴定
 的相关信息如下表:
的相关信息如下表:| 滴定对象 |  |
| 滴定时溶液pH范围 | 1.5~2.0 |
| 指示剂 | 磺基水杨酸 |
| 滴定终点现象 | 紫红色→亮黄色 |
 、
、 、
、 的浓度,具体步骤如下:
的浓度,具体步骤如下:I.先测定
 (
( 、
、 不影响Fe3+的滴定):
不影响Fe3+的滴定):请补充完整实验方案:
①按规定操作分别将0.01000
 EDTA标准溶液和待测溶液[其中
EDTA标准溶液和待测溶液[其中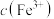 约为0.01
约为0.01 ]装入如图所示的滴定管中;
]装入如图所示的滴定管中;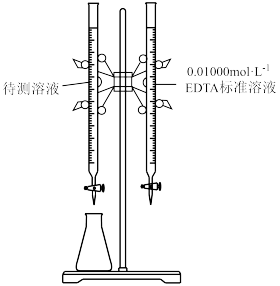
③实验测得
 的浓度偏大,其原因可能是
的浓度偏大,其原因可能是II.再测定
 :在
:在 的锥形瓶中继续加入适量过硫酸铵
的锥形瓶中继续加入适量过硫酸铵 ,轻微摇晃使
,轻微摇晃使 转化为
转化为 ,继续用EDTA标准溶液滴定到终点。写出
,继续用EDTA标准溶液滴定到终点。写出 转化为
转化为 的离子方程式:
的离子方程式:III.最后测定
 :在
:在 的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用
的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用 标准溶液滴定到终点。
标准溶液滴定到终点。 不影响
不影响 滴定的原因是
滴定的原因是
您最近半年使用:0次
名校
10 . 下列溶液一定呈中性的是
| A.pH=7的溶液 | B.等物质的量的强酸和强碱反应得到的溶液 |
C. 的溶液 的溶液 | D.使酚酞试液呈无色的溶液 |
您最近半年使用:0次



