常温下,向一定质量的冰醋酸中加水稀释,溶液的导电能力变化如图。已知 ,
, 。下列说法正确的是
。下列说法正确的是
 ,
, 。下列说法正确的是
。下列说法正确的是
| A.a、b、c三点溶液的pH:b>a>c |
| B.a、b、c三点溶液中水的电离程度:a>b>c |
C.b→c过程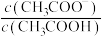 减小 减小 |
| D.向c点溶液中加入等浓度等体积的氮水,所得溶液呈中性 |
更新时间:2024-05-12 08:47:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】室温下,将( 固体溶于水配成100mL溶液,向溶液中加入下列物质有关结论正确的是
固体溶于水配成100mL溶液,向溶液中加入下列物质有关结论正确的是
 固体溶于水配成100mL溶液,向溶液中加入下列物质有关结论正确的是
固体溶于水配成100mL溶液,向溶液中加入下列物质有关结论正确的是| 加入的物质 | 结论 | |
| A |  | 反应结束后, |
| B |  固体 固体 | 反应完全后,溶液pH减小, 不变 不变 |
| C |  | 由水电离出的 不变 不变 |
| D |  | 溶液中 增大 增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】图为不同温度下水的电离平衡曲线,pOH=—lgc(OH—),下列说法错误的是


| A.D点溶液显酸性,E点溶液显碱性 |
| B.A点到B点可以通过降温来实现 |
| C.Kw的关系是:B<C<A=D=E |
| D.T1时,pH=2的硫酸与pH=12的NaOH溶液等体积混合后溶液呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,向体积均为V0 mL、pH均为3的两种难挥发性酸HX、HY溶液加入蒸馏水分别稀释至V mL,稀释后溶液的pH与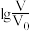 关系如图所示。忽略溶液体积变化,下列说法不正确的是
关系如图所示。忽略溶液体积变化,下列说法不正确的是

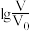 关系如图所示。忽略溶液体积变化,下列说法不正确的是
关系如图所示。忽略溶液体积变化,下列说法不正确的是
| A.HX溶液中不存在HX分子 |
B.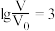 时微热两种溶液, 时微热两种溶液, 减小 减小 |
| C.a点溶液中的c(X-)大于b点溶液中的c(Y-) |
| D.常温下,0.1 mol/LHY溶液的pH=3,则Ka(HY)的数量级为10-5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某温度下,相同pH的两种弱酸HA和HB分别加水稀释,pH随溶液体积变化的曲线如图所示。下列判断正确的是( )
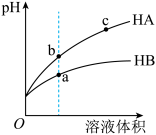
| A.酸性:HB> HA |
| B.结合H+的能力:B->A- |
| C.导电能力:c > b |
| D.与氢氧化钠完全反应时,消耗氢氧化钠体积Va<Vb |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,图象和实验结论表达均正确的是
| 实验① | 实验② | 实验③ | 实验④ |
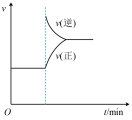
| 用0.10mol/L NaOH溶液滴定20mL 0.1mol/L的CH3COOH溶液 | 稀释初始pH相同的两种酸 | 向冰醋酸中逐渐加水后溶液导电能力的变化 | 验证FeCl3+3KSCN⇌Fe(SCN)3+3KCl平衡移动 |
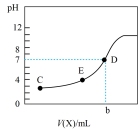 | 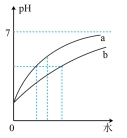 | 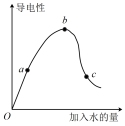 |  |
| A.实验①可用甲基橙作为指示剂 |
| B.实验②可推知,等体积等pH的两种酸和足量的金属镁反应,b产生的氢气更多 |
| C.实验③中分别向a、b、c三点对应的溶液加入NaOH溶液中和,完全中和时b点消耗的NaOH最多 |
| D.实验④是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图象 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下表中的实验操作能达到实验目的或能得出相应结论的是( )
| 选项 | 实验操作 | 实验目的或结论 |
| A | 室温下,将BaSO4投入饱和Na2CO3溶液中充分反应,向过滤后所得固体中加入足量盐酸,固体部分溶解且有无色无味气体产生 | 验证Ksp(BaSO4)<Ksp(BaCO3) |
| B | 将混有Ca(OH)2杂质的Mg(OH)2样品放入水中,搅拌,成浆状后,再加入饱和MgCl2溶液,充分搅拌后过滤,用蒸馏水洗净沉淀。 | 除去Mg(OH)2样品中Ca(OH)2杂质 |
| C | 向KNO3和KOH混合溶液中加入铝粉并加热,管口放湿润的红色石蕊试纸,试纸变为蓝色 | NO3-被氧化为NH3 |
| D | 室温下,用pH试纸测得:0.1mol/LNa2SO3溶液pH约为10,0.1mol/LNaHSO3溶液pH约为5 | HSO3-结合H+的能力比SO32-的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,0.1mol/L醋酸钠溶液的 。下列相关说法
。下列相关说法不正确 的是
 。下列相关说法
。下列相关说法A.醋酸钠溶液显碱性的原因是: |
B.常温下,醋酸钠溶液中: |
C.向10mL上述溶液中滴加5滴饱和 溶液, 溶液,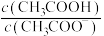 逐渐增大 逐渐增大 |
| D.在pH均为9的醋酸钠溶液和氨水中,水的电离程度:醋酸钠溶液>氨水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】室温下,通过下列实验探究0.1mol·L−1NaHCO3和0.1mol·L−1Na2CO3溶液的性质。
下列说法正确的是
| 实验1: | 用pH试纸测得0.1mol·L−1Na2CO3溶液pH约为12 |
| 实验2: | 两溶液中分别加入等体积的0.1mol·L−1CaCl2溶液,都产生白色沉淀 |
| 实验3: | 0.1mol·L−1NaHCO3与0.1mol·L−1Ba(OH)2溶液等体积混合,产生白色沉淀 |
| 实验4: | 向两溶液中不断滴加0.1mol·L−1HCl溶液,至不再产生气体 |
A.0.1mol·L−1Na2CO3溶液中存在c(OH-)=c(H+)+c( )+c(H2CO3) )+c(H2CO3) |
| B.实验2中CaCl2溶液滴入后,两试管中溶液pH均降低 |
C.实验3中的离子方程式为:Ba2++2OH-+2 =BaCO3↓+ =BaCO3↓+ +2H2O +2H2O |
D.实验4中完全反应后,两试管中溶液中都存在:c(H+)+c(Na+)=c(Cl-)+c(OH-)+c( )+c( )+c( ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】艾思考同学通过查阅资料发现,赖氨酸[H3N+(CH2)4CH(NH2)COO-,用HR表示]是人体必需氨基酸,其盐酸盐(H3RCl2)在水溶液中存在如下平衡:H3R2+ H2R+
H2R+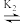 HR
HR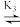 R-。向一定浓度的H3RCl2溶液中滴加NaOH溶液,溶液中H3R2+、H2R+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
R-。向一定浓度的H3RCl2溶液中滴加NaOH溶液,溶液中H3R2+、H2R+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)= ,下列表述
,下列表述正确 的是

 H2R+
H2R+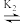 HR
HR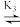 R-。向一定浓度的H3RCl2溶液中滴加NaOH溶液,溶液中H3R2+、H2R+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
R-。向一定浓度的H3RCl2溶液中滴加NaOH溶液,溶液中H3R2+、H2R+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)= ,下列表述
,下列表述
| A.曲线b对应的物质是HR |
B.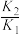 > >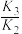 |
| C.M点,c(Cl-)+c(OH-)+c(R-)=2c(H2R+)+c(Na+)+c(H+) |
D.O点,pH=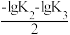 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下向一定浓度的 溶液中滴入盐酸,粒子浓度与混合溶液的pH变化的关系如图所示{已知:
溶液中滴入盐酸,粒子浓度与混合溶液的pH变化的关系如图所示{已知: 是二元弱酸,Y表示
是二元弱酸,Y表示 或
或 ,
, }:
}:
 溶液中滴入盐酸,粒子浓度与混合溶液的pH变化的关系如图所示{已知:
溶液中滴入盐酸,粒子浓度与混合溶液的pH变化的关系如图所示{已知: 是二元弱酸,Y表示
是二元弱酸,Y表示 或
或 ,
, }:
}:
A.曲线m表示 与pH的变化关系 与pH的变化关系 |
B. 数量级为 数量级为 |
C.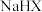 溶液显碱性 溶液显碱性 |
D.当 时,混合溶液中 时,混合溶液中 |
您最近一年使用:0次

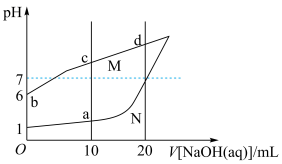

 为
为
 溶液滴定30.00mL等浓度的HA溶液,溶液中由水电离出的氢离子浓度的负对数[
溶液滴定30.00mL等浓度的HA溶液,溶液中由水电离出的氢离子浓度的负对数[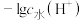 ]和溶液的pH与所加NaOH溶液体积的关系如图所示(其中虚线表示pH变化曲线),下列说法中正确的是
]和溶液的pH与所加NaOH溶液体积的关系如图所示(其中虚线表示pH变化曲线),下列说法中正确的是




