1 . 已知NA为阿伏加德罗常数的数值,下列有关说法中正确的是
| A.标准状况下,11.2LCHCl3中含有的C-Cl的数目为1.5NA |
| B.向FeI2溶液中通入适量Cl2,当有1molFe2+被氧化时,共转移电子的数目为NA |
| C.常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA |
| D.室温下,pH为13的NaOH和Ba(OH)2混合溶液中含OH-个数为0.1NA |
您最近一年使用:0次
名校
解题方法
2 . 重铬酸钾(K2Cr2O7)在实验室和工业上都有广泛应用,如用于制铬矾、制火柴、电镀、有机合成等。工业上。以铬铁矿[主要成分为Fe(CrO2)2,杂质主要为硅、铁、铝的氧化物]制备重铬酸钾的工艺流程如下图所示:
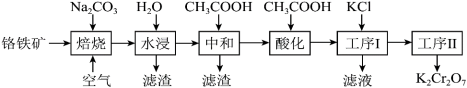
已知:①焙烧时Fe(CrO2)2中的Fe元素转化为NaFeO2,Cr元素转化为Na2CrO4。
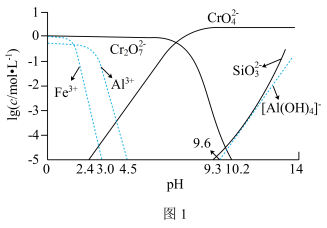
②矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图1所示。当溶液中可溶性组分浓度c≤10-5 mol·L-1时,可认为已除尽。
③有关物质的溶解度如图2所示。

回答下列问题:
(1)写出焙烧过程中发生的主要反应的化学方程式___________ 。
(2)水浸滤渣的主要成分是Fe(OH)3,写出生成此滤渣的化学方程式___________ 。
(3)中和步骤中理论pH的范围是___________ ,中和后滤渣的主要成分是___________ (填化学式)。
(4)酸化时加冰醋酸,简述不能用盐酸的可能原因是___________ 。
(5)工序1加入KCl后发生反应的离子方程式为___________ 。滤液经___________ (填操作名称)也可得到部分K2Cr2O7固体。经过工序2可得到更纯的K2Cr2O7固体,则工序2方法为___________ 。

已知:①焙烧时Fe(CrO2)2中的Fe元素转化为NaFeO2,Cr元素转化为Na2CrO4。
②矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图1所示。当溶液中可溶性组分浓度c≤10-5 mol·L-1时,可认为已除尽。
③有关物质的溶解度如图2所示。


回答下列问题:
(1)写出焙烧过程中发生的主要反应的化学方程式
(2)水浸滤渣的主要成分是Fe(OH)3,写出生成此滤渣的化学方程式
(3)中和步骤中理论pH的范围是
(4)酸化时加冰醋酸,简述不能用盐酸的可能原因是
(5)工序1加入KCl后发生反应的离子方程式为
您最近一年使用:0次
3 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.1mol 含有的共价键数为 含有的共价键数为 |
B.1L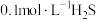 溶液中含有 溶液中含有 总数为 总数为 |
C.标准状况下,11.2L 含有的电子数大于 含有的电子数大于 |
D.向 盐酸溶液中通氨气至中性, 盐酸溶液中通氨气至中性, 的数目大于 的数目大于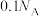 |
您最近一年使用:0次
名校
4 .  为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A. 的 的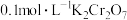 溶液中 溶液中 离子数为 离子数为 |
B.标准状况下,11.2L 与10.0gHF均含有 与10.0gHF均含有 个质子 个质子 |
C.常温下,将2.7g铝条投入足量浓硝酸中,转移 电子 电子 |
D.100mL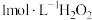 溶液中含有的 溶液中含有的 键数目为 键数目为 |
您最近一年使用:0次
5 . 常温下,下列各组离子在指定溶液中能大量共存的是
A.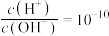 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.惰性电极电解饱和食盐水后的溶液中: 、 、 、 、 、 、 |
D.  溶液中: 溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
6 . 人们日常生产生活与化学有着紧密的联系。
(1)现有常温下pH=2的盐酸(甲)和pH=2的醋酸溶液(乙),请根据下列操作回答:
①常温下, 溶液加水稀释,下列数值一定变小的是
溶液加水稀释,下列数值一定变小的是___________ (填字母)。
A.c(H+) B. C.
C.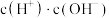 D.
D.
②取10mL乙溶液,加入少量无水CH3COONa固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的值将
的值将___________ (填“增大”“减小”或“无法确定”)。
③相同条件下,取等体积的甲、乙两溶液,分别与0.1mol/LNaOH溶液反应,消耗NaOH溶液的体积(甲)___________ (乙)(填“>”“<”或“=”)。
(2)已知水在25℃和100℃时,其电离平衡曲线如图所示:
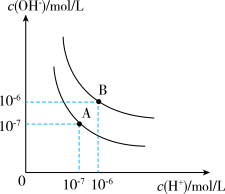
25℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为___________ 。
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
①CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为___________ 。
②同浓度的CH3COO-、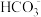 、
、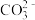 、ClO-结合H+的能力由强到弱的顺序为
、ClO-结合H+的能力由强到弱的顺序为___________ 。
③将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:___________ 。
④将SO2通入该氨水中,当c(OH-)降至 时,溶液中的
时,溶液中的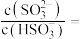
___________ 。
⑤下列微粒在溶液中不能大量共存的是___________ 。
A. 、
、 B.ClO-、
B.ClO-、 C.
C. 、
、 D.HClO、
D.HClO、
(1)现有常温下pH=2的盐酸(甲)和pH=2的醋酸溶液(乙),请根据下列操作回答:
①常温下,
 溶液加水稀释,下列数值一定变小的是
溶液加水稀释,下列数值一定变小的是A.c(H+) B.
 C.
C.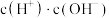 D.
D.
②取10mL乙溶液,加入少量无水CH3COONa固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
 的值将
的值将③相同条件下,取等体积的甲、乙两溶液,分别与0.1mol/LNaOH溶液反应,消耗NaOH溶液的体积(甲)
(2)已知水在25℃和100℃时,其电离平衡曲线如图所示:

25℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
| 弱电解质 | 电离常数(Ka) | |
| NH3·H2O | Kb=1.8×10-5 | |
| HClO | Kₐ=4.7×10-8 | |
| H2CO3 | Ka1=4.2×10-7 | Ka2=5.6×10-11 |
| H2SO3 | Ka1=1.54×10-2 | Ka2=1.02×10-7 |
| CH3COOH | Kₐ=1.7×10-5 | |
②同浓度的CH3COO-、
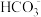 、
、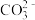 、ClO-结合H+的能力由强到弱的顺序为
、ClO-结合H+的能力由强到弱的顺序为③将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:
④将SO2通入该氨水中,当c(OH-)降至
 时,溶液中的
时,溶液中的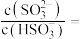
⑤下列微粒在溶液中不能大量共存的是
A.
 、
、 B.ClO-、
B.ClO-、 C.
C. 、
、 D.HClO、
D.HClO、
您最近一年使用:0次
7 . 正常体温下,人体动脉血液的 在
在 之间,之所以能够控制在该范围内,主要是因为血液中
之间,之所以能够控制在该范围内,主要是因为血液中 分子与
分子与 共存形成“缓冲溶液”[正常体温下
共存形成“缓冲溶液”[正常体温下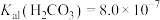 ,
,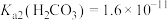 ],若血液
],若血液 超出正常范围,则可能导致酸中毒或碱中毒。
超出正常范围,则可能导致酸中毒或碱中毒。
(1)正常体温下,若某人动脉血 为
为 ,则属于
,则属于______ 中毒(选填“酸”或“碱”),他的血液中
______ 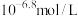 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
(2)已知: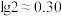 。正常体温下,某人动脉血液中
。正常体温下,某人动脉血液中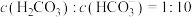 ,试通过计算判断属于酸中毒或碱中毒。
,试通过计算判断属于酸中毒或碱中毒。_____________________
 在
在 之间,之所以能够控制在该范围内,主要是因为血液中
之间,之所以能够控制在该范围内,主要是因为血液中 分子与
分子与 共存形成“缓冲溶液”[正常体温下
共存形成“缓冲溶液”[正常体温下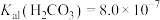 ,
,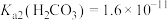 ],若血液
],若血液 超出正常范围,则可能导致酸中毒或碱中毒。
超出正常范围,则可能导致酸中毒或碱中毒。(1)正常体温下,若某人动脉血
 为
为 ,则属于
,则属于
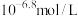 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。(2)已知:
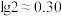 。正常体温下,某人动脉血液中
。正常体温下,某人动脉血液中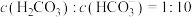 ,试通过计算判断属于酸中毒或碱中毒。
,试通过计算判断属于酸中毒或碱中毒。
您最近一年使用:0次
8 . 下列有关 试纸的说法正确的是
试纸的说法正确的是
 试纸的说法正确的是
试纸的说法正确的是A.对不同 的溶液显示不同的颜色 的溶液显示不同的颜色 |
B.精密 试纸测定范围是 试纸测定范围是 且为整数 且为整数 |
C.用广泛 试纸测“84”消毒液的 试纸测“84”消毒液的 |
D.测溶液酸性或碱性时, 试纸必须事先润湿 试纸必须事先润湿 |
您最近一年使用:0次
9 . 下列溶液因盐的水解而呈酸性的是
| A.柠檬水 | B.洁则灵 | C. 溶液 溶液 | D. 溶液 溶液 |
您最近一年使用:0次
10 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下, 的 的 含有电子数等于 含有电子数等于 |
B.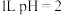 的 的 中含 中含 的数目为 的数目为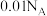 |
C.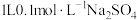 溶液中含有氧原子数为 溶液中含有氧原子数为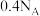 |
D.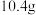 苯乙烯( 苯乙烯(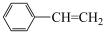 )中含有碳碳双键的数目为 )中含有碳碳双键的数目为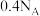 |
您最近一年使用:0次



