名校
1 . 关于下列各实验或装置的叙述中,正确的是
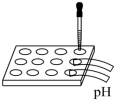 |  | 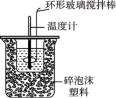 |  |
| A测定NaClO溶液的pH | B加热蒸干MgCl2溶液制备MgCl2固体 | C测定中和热 | D用酸性KMnO4溶液滴定FeSO4溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列实验误差分析不正确的是
A.用标准 溶液滴定 溶液滴定 溶液来测定其浓度,选择酚酞为指示剂 溶液来测定其浓度,选择酚酞为指示剂 |
| B.中和热测定实验中,用铜制环形搅拌器代替环形玻璃搅拌棒,所测放出的热量偏小 |
C.用润湿的 试纸测稀碱溶液的 试纸测稀碱溶液的 ,测定值偏小 ,测定值偏小 |
| D.用酸式滴定管盛放盐酸溶液,滴定前开始调节液面时,仰视读数,滴定后正常读数,最终会使所测液体体积偏低 |
您最近一年使用:0次
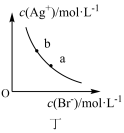
3 . 下列图示与对应的叙述相符的是
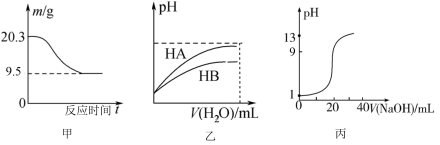


| A.图甲表示0.1molMgCl2·6H2O在空气中充分加热时固体质量随时间的变化 |
| B.图乙表示常温下,稀释等体积等pH的HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则酸性:HA<HB |
| C.图丙表示0.1mol·L-1NaOH溶液滴定20.00mL0.10mol·L-1醋酸溶液得到的滴定曲线 |
| D.图丁表示一定温度下,溴化银在水中的沉淀溶解平衡曲线,将a点溶液加入AgNO3固体可以得到b点代表的饱和溶液 |
您最近一年使用:0次
2022-04-03更新
|
241次组卷
|
2卷引用:四川省仁寿第一中学校南校区2023-2024学年高二上学期12月月考化学试题
名校
解题方法
4 . 水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)某温度(t℃)时,水的离子积为Kw=1×10-13,则该温度____ 25℃(选填“大于”、“小于”或“等于”),若将此温度下pH=11的苛性钠溶液aL与pH=1的稀硫酸bL混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两溶液的体积比:
①若所得混合液为中性,则a:b=____ ;此溶液中各种离子的浓度由大到小排列顺序是____ 。
②若所得混合液的pH=2,则a:b=____ 。
(2)25℃时,向水中加入一定量的碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为____ ,由水电离出的c(OH-)=____ mol·L-1。
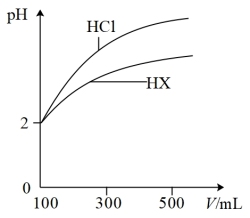
(3)体积均为100mL、pH均为2的盐酸与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX是____ (填“强酸”或“弱酸”)。
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
①25℃时,等物质的量浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,溶液的pH由大到小的顺序为____ (填化学式)。
②25℃时,在0.5mol/L的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的____ 倍。
(1)某温度(t℃)时,水的离子积为Kw=1×10-13,则该温度
①若所得混合液为中性,则a:b=
②若所得混合液的pH=2,则a:b=
(2)25℃时,向水中加入一定量的碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为
(3)体积均为100mL、pH均为2的盐酸与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX是

(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②25℃时,在0.5mol/L的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的
您最近一年使用:0次
名校
解题方法
5 . 下列有关实验操作的说法正确的是
| A.pH=3和pH=5的盐酸各10mL混合,所得溶液的pH=4 |
| B.中和反应反应热的测定实验中,将环形玻璃搅拌棒换成环形铁丝搅拌棒,不影响反应热的测定 |
| C.在配制FeCl3溶液时加入适量的盐酸是为了防止铁离子水解 |
| D.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 |
您最近一年使用:0次
2022-03-18更新
|
100次组卷
|
2卷引用:四川省遂宁市射洪中学2021-2022学年高二下学期第一次月考化学试题
名校
6 . 25℃,下列溶液等体积混合后pH>7的是
| A.pH=4的盐酸与pH=10的Ba(OH)2溶液 |
| B.pH=4的硝酸与pH=10的氨水溶液 |
| C.pH=2的醋酸与pH=12的NaOH溶液 |
| D.pH=2的硫酸与pH=12的KOH溶液 |
您最近一年使用:0次
2022-03-18更新
|
412次组卷
|
3卷引用:四川省遂宁市射洪中学2021-2022学年高二下学期第一次月考化学试题
名校
解题方法
7 . 下列指定反应的离子方程式正确的是
| A.向0.1 mol·L-1NaHA溶液(pH=1)中加入NaOH溶液: HA- +OH- =A2- +H2O |
B.乙醇与足量酸性重铬酸钾溶液: 3CH3CH2OH +2Cr2O +16H+=3CH3COOH +4Cr3++11H2O +16H+=3CH3COOH +4Cr3++11H2O |
C.Na2S2O3溶液与硝酸溶液混合: S2O +2H+=S↓+SO2↑+H2O +2H+=S↓+SO2↑+H2O |
| D.用纯碱溶液吸收海水提取溴时吹出的Br2: Br2 +2OH-=Br- + BrO- + H2O |
您最近一年使用:0次
2022-03-03更新
|
446次组卷
|
2卷引用:四川省成都市第四十九中学校2021-2022学年高三3月月考理综化学试题
名校
解题方法
8 . 常温下,下列各组离子在指定溶液中能大量共存的是
A.pH=1的溶液中:Fe2+、NO 、SO 、SO 、Na+ 、Na+ |
B.c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、CO 、Cl- 、Cl- |
C.c(H+)/c(OH-)=1012的溶液中:NH 、Al3+、NO 、Al3+、NO 、Cl- 、Cl- |
D.由水电离的c(H+)=1×10-14mol/L的溶液中:Ca2+、K+、Cl-、HCO |
您最近一年使用:0次
名校
解题方法
9 . 下列实验操作正确且能达到相应实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 用 试纸测定同温度同浓度 试纸测定同温度同浓度 溶液和 溶液和 溶液的 溶液的 | 酸性: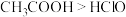 |
| B | 将 固体溶于适量浓盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的铁粉 固体溶于适量浓盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的铁粉 | 配制 溶液 溶液 |
| C | 将两个相同的 球分别放入热水和冰水里,热水中的 球分别放入热水和冰水里,热水中的 球红棕色加深,冰水中的变浅 球红棕色加深,冰水中的变浅 |  的 的 |
| D | 向 溶液中先滴入5滴 溶液中先滴入5滴 的 的 溶液,再滴入5滴 溶液,再滴入5滴 的 的 溶液 溶液 | 证明: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-22更新
|
332次组卷
|
4卷引用:四川省广安市2021-2022学年高二上学期期末考试化学试题
名校
10 . 下列实验操作规范且能达到实验目的的是
| 目的 | 操作 | |
| A | 测定醋酸钠溶液的pH | 用玻璃棒蘸 取溶液,点在湿润的pH试纸上 |
| B | 排除碱式滴定管尖嘴部分的气泡 | 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
| C | 由TiCl4制备TiO2∙xH2O | 在干燥的HCl气流中加热 |
| D | 研究催化剂对H2O2分解速率的影响 | 分别向两支试管中加入相同体积不同浓度的H2O2溶液,再向其中一支中加入少量MnO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-20更新
|
559次组卷
|
7卷引用:四川省仁寿第一中学校南校区2022—2023学年高二下学期3月月考化学试题



