名校
解题方法
1 . 常温下,甲乙两种溶液,已知甲溶液的 是乙溶液
是乙溶液 的2倍,则甲溶液的
的2倍,则甲溶液的 与乙溶液的
与乙溶液的 关系是
关系是
 是乙溶液
是乙溶液 的2倍,则甲溶液的
的2倍,则甲溶液的 与乙溶液的
与乙溶液的 关系是
关系是A. 倍 倍 | B. | C.100倍 | D.无法确定 |
您最近一年使用:0次
名校
解题方法
2 . 下列各组离子中,在给定条件下能够大量共存的是
A.通入足量 后的溶液中: 后的溶液中: 、 、 、 、 、 、 |
B.无色溶液中: 、 、 、 、 、 、 |
C.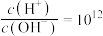 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.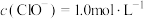 的溶液: 的溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
3 . 室温下,现有相同体积、 的氨水和
的氨水和 两种溶液:
两种溶液:
(1)溶液中水的电离程度:氨水_______  溶液。(填“
溶液。(填“ ”、“
”、“ ”或“
”或“ ”)
”)
(2)两种溶液分别加水稀释时的 变化曲线如图所示:
变化曲线如图所示: 点所在曲线对应的是
点所在曲线对应的是_______ (填溶液名称)
② 三点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积由大到小排序
三点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积由大到小排序_______ 。
 的氨水和
的氨水和 两种溶液:
两种溶液:(1)溶液中水的电离程度:氨水
 溶液。(填“
溶液。(填“ ”、“
”、“ ”或“
”或“ ”)
”)(2)两种溶液分别加水稀释时的
 变化曲线如图所示:
变化曲线如图所示: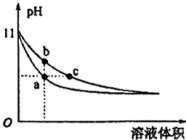
 点所在曲线对应的是
点所在曲线对应的是②
 三点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积由大到小排序
三点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积由大到小排序
您最近一年使用:0次
4 . 已知NA为阿伏加德罗常数的数值,下列有关说法中正确的是
| A.标准状况下,11.2LCHCl3中含有的C-Cl的数目为1.5NA |
| B.向FeI2溶液中通入适量Cl2,当有1molFe2+被氧化时,共转移电子的数目为NA |
| C.常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA |
| D.室温下,pH为13的NaOH和Ba(OH)2混合溶液中含OH-个数为0.1NA |
您最近一年使用:0次
解题方法
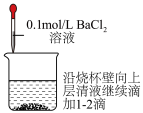
5 . 下列实验操作或装置能达到相应目的的是
|
|
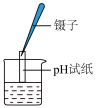
A.检验 是否沉淀完全 是否沉淀完全 | B.测定溶液的pH |
|
|
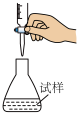
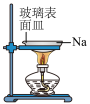
C.用酸性 溶液滴定 溶液滴定 溶液 溶液 | D.钠的燃烧 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024高三下·全国·专题练习
6 . 地球上没有垃圾,只有放错地方的资源。某化学兴趣小组对厨余垃圾中的鸡蛋壳进行再利用。主要实验步骤如下:
Ⅰ.鸡蛋壳预处理
将鸡蛋壳洗净干燥后研磨成粉,高温煅烧后加水得到石灰乳。
Ⅱ.制备葡萄糖酸钙
在石灰乳中边搅拌边缓缓加入葡萄糖酸溶液至pH为6~7,充分反应后过滤,将滤液蒸发浓缩、冷却结晶得到葡萄糖酸钙晶体。
Ⅲ.制备营养强化剂G
取3.00g葡萄糖酸钙晶体,用蒸馏水溶解,边搅拌边逐滴加入适量ZnSO4溶液,待反应完成后减压过滤;滤液转入烧杯中,加入适量95%乙醇,充分搅拌至晶体析出,减压过滤得到G的粗产物2.60g;将粗产物提纯后,得到G的晶体1.56g。
回答下列问题:
(1)步骤Ⅱ中用pH试纸测定溶液pH的操作方法是_______ 。
Ⅰ.鸡蛋壳预处理
将鸡蛋壳洗净干燥后研磨成粉,高温煅烧后加水得到石灰乳。
Ⅱ.制备葡萄糖酸钙
在石灰乳中边搅拌边缓缓加入葡萄糖酸溶液至pH为6~7,充分反应后过滤,将滤液蒸发浓缩、冷却结晶得到葡萄糖酸钙晶体。
Ⅲ.制备营养强化剂G
取3.00g葡萄糖酸钙晶体,用蒸馏水溶解,边搅拌边逐滴加入适量ZnSO4溶液,待反应完成后减压过滤;滤液转入烧杯中,加入适量95%乙醇,充分搅拌至晶体析出,减压过滤得到G的粗产物2.60g;将粗产物提纯后,得到G的晶体1.56g。
已知:①葡萄糖酸分子式为C6H12O7,结构简式为: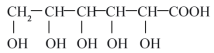
回答下列问题:
(1)步骤Ⅱ中用pH试纸测定溶液pH的操作方法是
您最近一年使用:0次
解题方法
7 . 2023年诺贝尔化学奖授予了三位科学家,以表彰他们为“发现和合成量子点”作出的贡献。一种含有新型量子点(简写为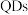 )的复合光催化剂利用太阳能高效制氢的原理如图所示。
)的复合光催化剂利用太阳能高效制氢的原理如图所示。
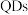 )的复合光催化剂利用太阳能高效制氢的原理如图所示。
)的复合光催化剂利用太阳能高效制氢的原理如图所示。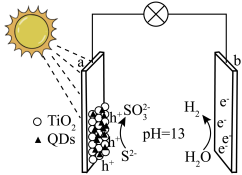
| A.电子由电极b沿导线流向电极a |
B.电极a的电极反应式为:S2-+3H2O-6e-= +6H+ +6H+ |
C.标准状况下,当电路转移2mol电子时电极 生成11.2L 生成11.2L |
D.电池的总反应方程式为:S2-+3H2O  +3H2↑ +3H2↑ |
您最近一年使用:0次
2024-04-15更新
|
249次组卷
|
2卷引用:2024届贵州省高三下学期二模化学试题
名校
解题方法
8 . 下列实验操作、现象和得出的结论都正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 用pH试纸测同温同浓度的KClO3和NaClO溶液的pH,NaClO溶液pH值大 | 溶液的碱性:NaClO>KClO3 |
| B | 向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置,溶液分层,上层几乎无色,下层紫红色 | 非金属性:Cl>Br>I |
| C | 将Na[Al(OH)4](或写为NaAlO2)溶液加入NaHCO3溶液中,有白色沉淀生成 | 结合H+能力: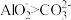 |
| D | 向两支盛有KI3溶液的试管中分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀生成 | KI3溶液中存在平衡: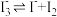 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 重铬酸钾(K2Cr2O7)在实验室和工业上都有广泛应用,如用于制铬矾、制火柴、电镀、有机合成等。工业上。以铬铁矿[主要成分为Fe(CrO2)2,杂质主要为硅、铁、铝的氧化物]制备重铬酸钾的工艺流程如下图所示:
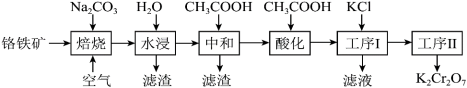
已知:①焙烧时Fe(CrO2)2中的Fe元素转化为NaFeO2,Cr元素转化为Na2CrO4。
②矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图1所示。当溶液中可溶性组分浓度c≤10-5 mol·L-1时,可认为已除尽。
③有关物质的溶解度如图2所示。
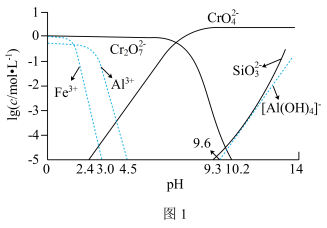

回答下列问题:
(1)写出焙烧过程中发生的主要反应的化学方程式___________ 。
(2)水浸滤渣的主要成分是Fe(OH)3,写出生成此滤渣的化学方程式___________ 。
(3)中和步骤中理论pH的范围是___________ ,中和后滤渣的主要成分是___________ (填化学式)。
(4)酸化时加冰醋酸,简述不能用盐酸的可能原因是___________ 。
(5)工序1加入KCl后发生反应的离子方程式为___________ 。滤液经___________ (填操作名称)也可得到部分K2Cr2O7固体。经过工序2可得到更纯的K2Cr2O7固体,则工序2方法为___________ 。

已知:①焙烧时Fe(CrO2)2中的Fe元素转化为NaFeO2,Cr元素转化为Na2CrO4。
②矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图1所示。当溶液中可溶性组分浓度c≤10-5 mol·L-1时,可认为已除尽。
③有关物质的溶解度如图2所示。


回答下列问题:
(1)写出焙烧过程中发生的主要反应的化学方程式
(2)水浸滤渣的主要成分是Fe(OH)3,写出生成此滤渣的化学方程式
(3)中和步骤中理论pH的范围是
(4)酸化时加冰醋酸,简述不能用盐酸的可能原因是
(5)工序1加入KCl后发生反应的离子方程式为
您最近一年使用:0次
解题方法
10 . 碳酸氢铵在食品工业中常用于制作蓬松的面点和糕点。室温下,通过下列实验来探究 的性质:
的性质:
实验1:测得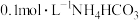 溶液的
溶液的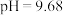
实验2:向浓度为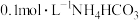 溶液中加入足量
溶液中加入足量 ,有刺激性气味气体产生
,有刺激性气味气体产生
实验3:浓度均为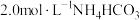 溶液和
溶液和 溶液等体积混合,有晶体析出,过滤
溶液等体积混合,有晶体析出,过滤
下列说法正确的是
 的性质:
的性质:实验1:测得
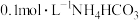 溶液的
溶液的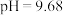
实验2:向浓度为
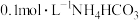 溶液中加入足量
溶液中加入足量 ,有刺激性气味气体产生
,有刺激性气味气体产生实验3:浓度均为
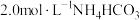 溶液和
溶液和 溶液等体积混合,有晶体析出,过滤
溶液等体积混合,有晶体析出,过滤下列说法正确的是
A.实验1可以用 试纸进行测定 试纸进行测定 |
B.由实验1可得: |
C.实验2中发生反应的离子方程式: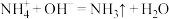 |
D.实验3中析出的晶体为 |
您最近一年使用:0次