名校
解题方法
1 . 室温下,某二元弱酸(用H2A表示)的 、
、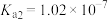 ,NH3⋅H2O的
,NH3⋅H2O的 ,通过下列实验探究NH4HA溶液的性质。
,通过下列实验探究NH4HA溶液的性质。
下列有关说法正确的是
 、
、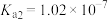 ,NH3⋅H2O的
,NH3⋅H2O的 ,通过下列实验探究NH4HA溶液的性质。
,通过下列实验探究NH4HA溶液的性质。| 实验 | 实验操作 |
| 1 | 用pH试纸测定0.1mol·L-1NH4HA溶液的pH,测得pH约为4.5 |
| 2 | 将0.1mol·L-1NH4HA溶液和0.1mol·L-1NaOH溶液等体积混合,无气体产生 |
| 3 | 向实验2所得溶液中继续滴加一定量0.1mol·L-1NaOH溶液,加热,使产生的气体完全逸出 |
| 4 | 将等体积0.1mol·L-1NH4HA溶液与0.05mol·L-1ZnSO4溶液混合,产生ZnA沉淀 |
A.由实验1可知,0.1mol⋅L-1NH4HA溶液中由水电离出的 |
B.实验2所得溶液中存在: |
C.实验3所得溶液中一定含有Na2A,故反应过程中一定有: |
D.由实验4可知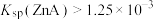 |
您最近半年使用:0次
名校
解题方法
2 . NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;请回答下列问题:______ 。(请用离子方程式加文字进行描述)
(2)相同条件下,0.1mol•L﹣1NH4Al(SO4)2中c(NH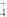 )
)______ (填“等于”、“大于”或“小于”)0.1mol•L﹣1 NH4HCO3中c( )。
)。
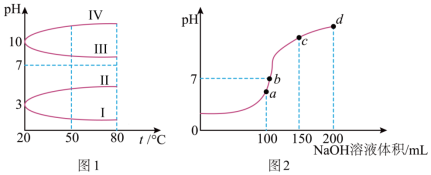
(3)如图1是0.1mol•L﹣1电解质溶液的pH随温度变化的图像
①其中符合0.1mol•L﹣1NH4Al(SO4)2的pH随温度变化的曲线是______ (填写序号)。
②20℃时,0.1mol•L﹣1NH4Al(SO4)2中2c( )﹣c(
)﹣c( )﹣3c(Al3+)=
)﹣3c(Al3+)= ______ mol•L﹣1(用数字表达式写出精确结果)。
(4)室温时,向100mL 0.1mol•L﹣1 NH4HSO4溶液中滴加0.1mol•L﹣1 NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2所示:试分析图2中a、b、c、d四个点,水的电离程度最大是______ 点。
(2)相同条件下,0.1mol•L﹣1NH4Al(SO4)2中c(NH
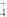 )
) )。
)。(3)如图1是0.1mol•L﹣1电解质溶液的pH随温度变化的图像
①其中符合0.1mol•L﹣1NH4Al(SO4)2的pH随温度变化的曲线是
②20℃时,0.1mol•L﹣1NH4Al(SO4)2中2c(
 )﹣c(
)﹣c( )﹣3c(Al3+)=
)﹣3c(Al3+)= (4)室温时,向100mL 0.1mol•L﹣1 NH4HSO4溶液中滴加0.1mol•L﹣1 NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2所示:试分析图2中a、b、c、d四个点,水的电离程度最大是
您最近半年使用:0次
名校
3 . 下列事实不一定能证明HNO2是弱电解质的是

| A.向HNO2中加入NaNO2固体后pH增大 |
| B.用HNO2溶液做导电实验,灯泡很暗 |
| C.向水中加入NaNO2固体,图水的电离平衡曲线可以从C点到D点 |
| D.常温下,pH=3的HNO2溶液与pH=11的NaOH溶液等体积混合,所得溶液pH<7 |
您最近半年使用:0次
4 . 常温下,下列各组离子在指定溶液中--定能大量共存的是
A.在NaClO和NaCl的混合溶液中: 、 、 、 、 、 、 |
B.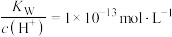 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.使甲基橙变黄色的溶液中: 、 、 、 、 、 、 |
D.由水电离的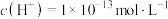 的溶液中 的溶液中 、 、 、 、 、 、 |
您最近半年使用:0次
名校
解题方法
5 . 下列关于电解质溶液的叙述中正确的是
| A.Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 |
| B.常温下,某溶液中由水电离出的c(H+)=10-5mol∙L-1,则此溶液可能是盐酸 |
C.物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c( )前者小于后者 )前者小于后者 |
D.常温下,1mol∙L-1的CH3COOH溶液与1mol∙L-1的NaOH溶液等体积混合后,所得混合液中: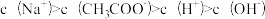 |
您最近半年使用:0次
6 . 常温下,0.1mol/L醋酸钠溶液的 。下列相关说法
。下列相关说法不正确 的是
 。下列相关说法
。下列相关说法A.醋酸钠溶液显碱性的原因是: |
B.常温下,醋酸钠溶液中: |
C.向10mL上述溶液中滴加5滴饱和 溶液, 溶液,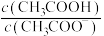 逐渐增大 逐渐增大 |
| D.在pH均为9的醋酸钠溶液和氨水中,水的电离程度:醋酸钠溶液>氨水 |
您最近半年使用:0次
解题方法
7 . 下列操作能促进水的电离且溶液呈酸性的是
| A.向水中加入Na2CO3溶液 | B.向水中加入NaHSO4溶液 |
| C.将水加热到100℃,使pH=6 | D.向水中加入NH4Cl固体 |
您最近半年使用:0次
名校
8 . 常温下,用浓度为 的
的 标准溶液滴定浓度均为
标准溶液滴定浓度均为 的
的 和
和 的混合溶液,滴定过程中溶液的
的混合溶液,滴定过程中溶液的 随
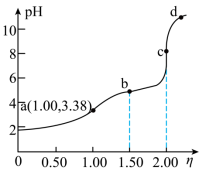
随 的变化曲线如图所示。下列说法错误的是
的变化曲线如图所示。下列说法错误的是
 的
的 标准溶液滴定浓度均为
标准溶液滴定浓度均为 的
的 和
和 的混合溶液,滴定过程中溶液的
的混合溶液,滴定过程中溶液的 随
随 的变化曲线如图所示。下列说法错误的是
的变化曲线如图所示。下列说法错误的是
A.b点: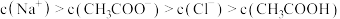 |
B.c点: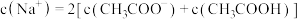 |
C.水的电离程度: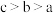 |
D.常温下 的水解平衡常数约为 的水解平衡常数约为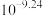 |
您最近半年使用:0次
名校
9 . 25℃时,苯酚(C6H5OH)的Ka=1.0×10-10,下列说法正确的是
| A.相同温度下,等pH的C6H5ONa和CH3COONa溶液中,c(C6H5O-)>c(CH3COO-) |
| B.25℃时,浓度均为0.10mol·L-1的C6H5ONa和C6H5OH的混合溶液呈碱性 |
| C.25℃时,C6H5OH溶液与NaOH溶液混合,测得pH=10.00,则此时溶液中c(C6H5O-)=c(C6H5OH) |
| D.25℃时,0.10mol·L-1的C6H5OH溶液中加少量C6H5ONa固体,水的电离程度变小 |
您最近半年使用:0次
10 . 下列曲线中,可以描述0.1 mol·L-1乙酸(甲,Ka=1.8×10-5)和0.1 mol·L-1氯乙酸(乙,Ka=1.4×10-3)的水溶液中,水电离出的c(H+)与加入水体积V的关系的是
A.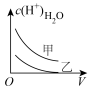 | B.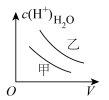 | C.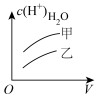 | D.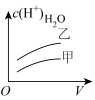 |
您最近半年使用:0次



