名校
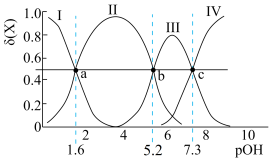
1 . 常温下,将一定量稀硫酸逐滴滴人高铁酸钠(Na2FeO4)溶液中,溶液中含铁微粒存在如下平衡;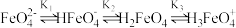 ,各微粒的物质的量分数δ(X)随pOH变化如图。下列说法正确的是
,各微粒的物质的量分数δ(X)随pOH变化如图。下列说法正确的是
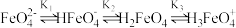 ,各微粒的物质的量分数δ(X)随pOH变化如图。下列说法正确的是
,各微粒的物质的量分数δ(X)随pOH变化如图。下列说法正确的是
A.III代表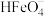 的变化曲线 的变化曲线 |
| B.a,b,c三点水的电离程度相等 |
C.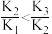 |
D.a点处: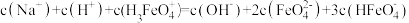 |
您最近一年使用:0次
2023-04-24更新
|
842次组卷
|
11卷引用:专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)
(已下线)专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)秘籍16 电解质溶液微粒变化及图象分析-备战2022年高考化学抢分秘籍(全国通用)辽宁省2022届高三实战猜题卷(六)化学试题(已下线)必刷卷05-2022年高考化学考前信息必刷卷(全国甲卷)(已下线)押江苏卷第13题 水溶液中的离子平衡 -备战2022年高考化学临考题号押题(江苏卷)河北省衡水中学2022-2023学年高三上学期四调考试化学试题(已下线)专题12 电解质溶液中的四大平衡常数(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(已下线)微专题 水溶液中函数图像的分析湖南省娄底市部分学校2022-2023学年高三三模化学试题江苏省盐城市实验高级中学2022-2023学年高三下学期第三次模拟考试化学试题辽宁省部分学校2023-2024高二上学期期末考试化学试卷
2 . 某水样中含一定浓度的 、
、 和其他不与酸碱反应的离子,取
和其他不与酸碱反应的离子,取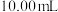 水样,用
水样,用 的
的 溶液进行滴定,溶液
溶液进行滴定,溶液 随滴加
随滴加 溶液体积的变化关系如图,下列说法正确的是
溶液体积的变化关系如图,下列说法正确的是

 、
、 和其他不与酸碱反应的离子,取
和其他不与酸碱反应的离子,取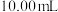 水样,用
水样,用 的
的 溶液进行滴定,溶液
溶液进行滴定,溶液 随滴加
随滴加 溶液体积的变化关系如图,下列说法正确的是
溶液体积的变化关系如图,下列说法正确的是
A.a点不含 离子 离子 |
| B.水的电离程度:a>b |
C.a点溶液中存在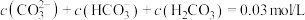 |
D.滴定过程中会发生: |
您最近一年使用:0次
3 . 常温下,pH均为2、体积均为V0的HA、 HB、HC三种酸溶液,分别加水稀释至体积为V,溶液pH随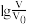 的变化关系如图所示,下列叙述错误的是
的变化关系如图所示,下列叙述错误的是

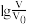 的变化关系如图所示,下列叙述错误的是
的变化关系如图所示,下列叙述错误的是
| A.常温下:Ka(HB)> Ka(HA) |
B.当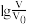 =4时,三种溶液同时升高温度, =4时,三种溶液同时升高温度, 减小 减小 |
| C.酸的物质的量浓度:b点<a点 |
| D.水的电离程度:b点<c点 |
您最近一年使用:0次
2022高三·全国·专题练习
名校
4 . 已知常温时HClO的Ka=3.0×10-8,HF的Ka=3.5×10-4,现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是
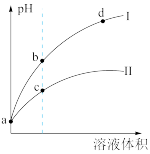

| A.曲线Ⅱ为氢氟酸稀释时pH变化曲线 |
| B.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗氢氟酸的体积较小 |
| C.b点溶液中水的电离程度比c点溶液中水的电离程度小 |
D.从b点到d点,溶液中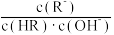 保持不变(HR代表HClO或HF) 保持不变(HR代表HClO或HF) |
您最近一年使用:0次
2022-09-28更新
|
1289次组卷
|
8卷引用:第21讲 电离平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)
(已下线)第21讲 电离平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)江西省赣州市十校协作2022-2023学年高二上学期期中联考化学试题(已下线)专项特训5 弱电解质电离常数计算与图像分析第1讲 弱电解质的电离平衡江苏省常熟市王淦昌高级中学2022-2023学年高二3月月考化学试题江西省永修县第一中学2023-2024学年高二上学期10月月考化学试题江西省南昌市第一中学2023-2024学年高二上学期10月月考化学试题四川省宜宾市叙州区第二中学校2023-2024学年高二上学期12月月考化学试题
5 . 25℃时,将1.0Lx mol ·L-1 CH3COOH溶液与0. 1 mol NaOH固体混合,使之充分反应。然后向该混合溶液中通入HCl气体或加入NaOH固体(忽略体积和温度变化),溶液pH随通入(或加入)物质的物质的量的变化如图所示。下列叙述正确的是


| A.水的电离程度:①>②>③ |
| B.点②对应的混合溶液中:c(CH3COOH)+c(CH3COO-)=x mol·L-1 |
| C.点③对应的混合溶液中:c(Na+)> c(CH3COO-) |
D.该温度下,CH3COOH的电离平衡常数Ka=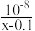 |
您最近一年使用:0次
2022-07-25更新
|
839次组卷
|
3卷引用:第23讲 弱电解质的电离平衡(讲)-2023年高考化学一轮复习讲练测(全国通用)
(已下线)第23讲 弱电解质的电离平衡(讲)-2023年高考化学一轮复习讲练测(全国通用)河南省开封市2021-2022学年高三第一次模拟考试理科综化学试题天津市耀华中学2022-2023学年高三上学期第三次月考化学试题
名校
6 . 常温下,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol·L-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。下列说法中不正确的是
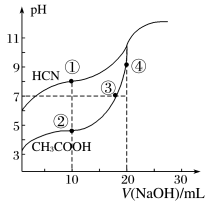

| A.CH3COOH的电离常数约为10-5 |
| B.水的电离程度:点①>点③>点② |
| C.在点①和点②所示溶液中:c(CN-)>c(CH3COO-) |
| D.在点③和点④之间的溶液中:c(CH3COO-)>c(CH3COOH) |
您最近一年使用:0次
解题方法
7 . 常温下,用0.1mol·L-1的NaOH溶液滴定20mL0.1mol·L-1HA溶液。溶液中A-(或HA)的分布系数δ、NaOH溶液体积V与pH的关系如图所示[已知:δ(HA)= ]。下列叙述错误的是
]。下列叙述错误的是

 ]。下列叙述错误的是
]。下列叙述错误的是
| A.曲线a表示的是HA的分布系数变化曲线 |
| B.HA的电离平衡常数的数量级为10-6 |
| C.p点对应的溶液中,c(A-)<3c(HA) |
| D.p、n、q中,水的电离程度最大的是q点 |
您最近一年使用:0次
8 . 常温下,向20mL浓度均为0.1mol·L-1的HX和CH3COOH的混合溶液中滴加0.1mol·L-1的氨水,测得溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积(V)的关系如图。(CH3COOH的Ka=1.8×10-5,NH3·H2O的Kb=1.8×10-5),下列说法正确的是


| A.常温时,同浓度的HX溶液比CH3COOH溶液的pH大 |
| B.a→c过程,水的电离程度先减小后增大 |
C.溶液pH=7时对应的点在c点和d点之间,此时溶液中存在: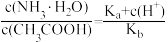 |
D.混合时若忽略体积变化,d点时:4c(NH )+4c(NH3·H2O)=0.3mol·L-1 )+4c(NH3·H2O)=0.3mol·L-1 |
您最近一年使用:0次
解题方法
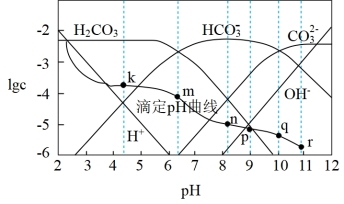
9 . 常温时,采用甲基橙和酚酞双指示剂,用盐酸滴定Na2CO3溶液,溶液中lgc(H2CO3)、lgc(HCO )、lgc(H+)、lgc(OH-)随溶液pH的变化及滴定曲线如图所示,下列说法不正确的是
)、lgc(H+)、lgc(OH-)随溶液pH的变化及滴定曲线如图所示,下列说法不正确的是
 )、lgc(H+)、lgc(OH-)随溶液pH的变化及滴定曲线如图所示,下列说法不正确的是
)、lgc(H+)、lgc(OH-)随溶液pH的变化及滴定曲线如图所示,下列说法不正确的是
| A.整个滴定过程中可先用酚酞再用甲基橙作指示剂 |
| B.n点的pH为m点和q点pH的平均值 |
C.r点溶液中c(OH-)=c(H+)+c(HCO )+2c(H2CO3) )+2c(H2CO3) |
| D.r点到k点对应的变化过程中,溶液中水的电离程度先减小后增大 |
您最近一年使用:0次
解题方法
10 . 25℃时,在体积均为100 mL、浓度均为0.1 mol·L-1的两种一元酸HA和HB的溶液中,分别加入NaOH固体(温度恢复至室温,溶液体积变化忽略不计), 随加入NaOH固体的物质的量的变化如图所示。下列有关说法不正确的是
随加入NaOH固体的物质的量的变化如图所示。下列有关说法不正确的是

 随加入NaOH固体的物质的量的变化如图所示。下列有关说法不正确的是
随加入NaOH固体的物质的量的变化如图所示。下列有关说法不正确的是
| A.酸性:HA> HB,且HA是强酸,HB是弱酸 |
| B.由水电离出的c(H+ )的顺序:a<b<c<d |
| C.c点溶液中:c(H+)=c(B-)-c(HB) +c(OH-) |
| D.d点溶液中:c(B-)=c(Na+)>c(H+)=c(OH-) |
您最近一年使用:0次



