名校
1 . 25℃时,三种酸的电离平衡常数如下,回答下列问题:
(1)一般情况下,当温度升高时,Ka__ (填“增大”、“减小”或“不变”).
(2)下列四种离子结合H+能力由大到小的顺序是__ (填序号);
a.CO b.ClO- c.CH3COO- d.HCO
b.ClO- c.CH3COO- d.HCO
(3)下列反应不能发生的是__ (填序号)
a.CO +2CH3COOH=2CH3COO-+CO2↑+H2O
+2CH3COOH=2CH3COO-+CO2↑+H2O
b.ClO-+CH3COOH=CH3COO-+HClO
c.CO +2HClO=CO2↑+H2O+2ClO-
+2HClO=CO2↑+H2O+2ClO-
d.HClO+CH3COO-=CH3COOH+ClO-
(4)用蒸馏水稀释0.1mol/L的醋酸,下列各式表示的数值随水量的增加而增大的是__ (填序号);
a.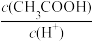 b.
b.
c. d.
d.
(5)体积均为10mL、c(H+)=10-2mol/L的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。则HX的电离平衡常数__ (填“大于”、“等于”或“小于”,下同)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来c(H+)__ 醋酸溶液中水电离出来的c(H+),理由是__ 。

| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7;K2=5.6×10-11 | 3.0×10-8 |
(2)下列四种离子结合H+能力由大到小的顺序是
a.CO
 b.ClO- c.CH3COO- d.HCO
b.ClO- c.CH3COO- d.HCO
(3)下列反应不能发生的是
a.CO
 +2CH3COOH=2CH3COO-+CO2↑+H2O
+2CH3COOH=2CH3COO-+CO2↑+H2Ob.ClO-+CH3COOH=CH3COO-+HClO
c.CO
 +2HClO=CO2↑+H2O+2ClO-
+2HClO=CO2↑+H2O+2ClO-d.HClO+CH3COO-=CH3COOH+ClO-
(4)用蒸馏水稀释0.1mol/L的醋酸,下列各式表示的数值随水量的增加而增大的是
a.
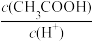 b.
b.
c.
 d.
d.
(5)体积均为10mL、c(H+)=10-2mol/L的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。则HX的电离平衡常数

您最近一年使用:0次
2 . 不同温度下,水溶液中 与
与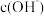 的关系如图所示.回答下列问题:
的关系如图所示.回答下列问题:

(1)T℃_______ 25℃(填“>”、“<”或“=”).
(2)向a点对应的醋酸溶液中滴加等物质的量浓度的NaOH溶液至b点,则两溶液的体积_________ (填“相等”或“不相等”).
(3)d点对应的食盐水
__________ ,呈__________ 性(填“酸”、“中”或“碱”).
(4)将等pH等体积的HCl和 分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m
分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m_______ n(填“大于、等于、小于”).
(5)常温下,将 的NaOH溶液
的NaOH溶液 与
与 的
的 溶液
溶液 混合,若所得混合溶液的
混合,若所得混合溶液的 ,则
,则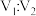 为
为____________ .
(6)常温下,0.05mol/L的 溶液中,由水所电离出的
溶液中,由水所电离出的 为
为___________ .
 与
与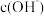 的关系如图所示.回答下列问题:
的关系如图所示.回答下列问题:
(1)T℃
(2)向a点对应的醋酸溶液中滴加等物质的量浓度的NaOH溶液至b点,则两溶液的体积
(3)d点对应的食盐水

(4)将等pH等体积的HCl和
 分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m
分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m(5)常温下,将
 的NaOH溶液
的NaOH溶液 与
与 的
的 溶液
溶液 混合,若所得混合溶液的
混合,若所得混合溶液的 ,则
,则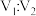 为
为(6)常温下,0.05mol/L的
 溶液中,由水所电离出的
溶液中,由水所电离出的 为
为
您最近一年使用:0次
解题方法
3 . 将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m__________ n(填“大于”、“等于”或“小于”)。
您最近一年使用:0次
解题方法
4 . 体积均为100mL、 pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数__________ (填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。


您最近一年使用:0次
名校
解题方法
5 . (1)已知常温时,0.1mol/L醋酸在水中有0.1%发生电离,则该溶液的pH=_____ ,醋酸的电离平衡常数Ka=______ 。
(2)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示:
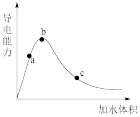
①a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是___ 。
②a、c两点对应的溶液分别吸收氨气,若两溶液最终pH均为7(25℃时),则a点溶液中的c(CH3COO-)_______ c点溶液中的c(NH4+)。(填“<”、“>”或“=”)
(3)25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
①H2CO3的第二级电离平衡常数的表达式Ka2=_______ 。
②25℃时,向0.1mol•L-1的氨水中缓缓通入CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是___ 。
A. B.
B.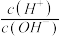 C.
C.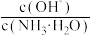 D.
D.
③向NaCN溶液中通入少量CO2气体,发生反应的离子方程式为___ 。
(2)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示:

①a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是
②a、c两点对应的溶液分别吸收氨气,若两溶液最终pH均为7(25℃时),则a点溶液中的c(CH3COO-)
(3)25℃时,部分物质的电离平衡常数如表所示:
| 化学式 | CH3COOH | NH3·H2O | H2CO3 | HCN |
| 电离平衡常数 | 1.7×10-5 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K=5.0×10-10 |
请回答下列问题:
①H2CO3的第二级电离平衡常数的表达式Ka2=
②25℃时,向0.1mol•L-1的氨水中缓缓通入CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是
A.
 B.
B.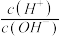 C.
C.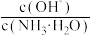 D.
D.
③向NaCN溶液中通入少量CO2气体,发生反应的离子方程式为
您最近一年使用:0次



