名校
1 . 设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.标准状况下, 含c分子数为 含c分子数为 |
B.1LpH=1的硫酸溶液含氢离子数为 |
C.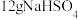 固体含阴离子数为 固体含阴离子数为 |
D.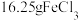 完全溶于沸水后,生成 完全溶于沸水后,生成 胶粒的数目为 胶粒的数目为 |
您最近半年使用:0次
2024-02-25更新
|
515次组卷
|
4卷引用:2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学
2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)四川省内江市第六中学2023-2024学年高三下学期入学考试理综试题-高中化学2024届陕西省西安博爱国际学校高三下学期第一次模拟考试理科综合试卷-高中化学
2 . 常温下,0.10 mol/L HCOONH4溶液中部分微粒( 、
、 、HCOOH、
、HCOOH、 )的
)的 (可通入加入NaOH或HCl调节溶液pH)关系如图所示。
(可通入加入NaOH或HCl调节溶液pH)关系如图所示。 ,
,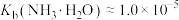 。下列说法正确的是
。下列说法正确的是


 、
、 、HCOOH、
、HCOOH、 )的
)的 (可通入加入NaOH或HCl调节溶液pH)关系如图所示。
(可通入加入NaOH或HCl调节溶液pH)关系如图所示。 ,
,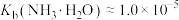 。下列说法正确的是
。下列说法正确的是

A.曲线②和③分别表示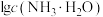 和 和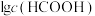 随pH的变化 随pH的变化 |
| B.溶液中M点对应的pH=7 |
C.HCOONH4的水解平衡常数 约为 约为 |
D.原溶液中 |
您最近半年使用:0次
2024-02-25更新
|
141次组卷
|
2卷引用:湖北省新高考协作体2023-2024学年高三下学期2月收心考试化学试题
3 .  为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是| A.2 g H218O与D216O的混合物中所含中子、电子数目均为NA |
B.标准状况下, 中电子的数目为 中电子的数目为 |
C. 的 的 溶液中 溶液中 的数目为 的数目为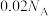 |
| D.1.7gH2O2中含有共价键数为0.1NA |
您最近半年使用:0次
名校
解题方法
4 . I.Mg(OH)2具有广泛的用途。以菱镁矿(主要成分是MgCO3,含少量Al2O3、FeO等)为原料制备Mg(OH)2的工艺流程如下:
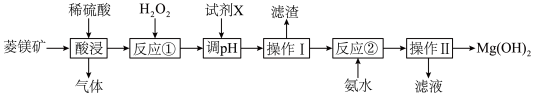
已知:常温下,部分氢氧化物开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“气体”的电子式是___________ 。
(2)下列操作不能显著增大“酸浸”速率的是___________ (填标号)。
a.适当增大稀硫酸的浓度 b.适当升高浸取液的温度 c.增大压强 d.将菱镁矿粉碎
(3)写出反应①的离子方程式:___________ 。
(4)“调pH”时,合适的pH是___________ (填标号)。
a.1.9 b.3.4 c.7.6 d.9.6
常温下,滴加氨水时,Mg2+的浓度为1.0×10-5 mol⋅L-1时被认为完全沉淀,这时的pH为x,x=___________ (已知:常温下, ,
, )。
)。
II.聚合硫酸铁 是一种无机高分子絮凝剂,可用于水的处理。
是一种无机高分子絮凝剂,可用于水的处理。
聚合硫酸铁 产品的组成可通过下列实验测定:
产品的组成可通过下列实验测定:
①称取一定质量的聚合硫酸铁样品配成100.00mL溶液A;
②准确量取20.00mL溶液A,加入足量盐酸酸化后,加BaCl2(ag)至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
③准确量取20.00mL溶液A,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250.00mL溶液B;
④准确量取25.00mL溶液B,用0.1000mol⋅L-1的KMnO4(H+)滴定至终点,消耗KMnO4(ag)8.00mL。
(5)该聚合硫酸铁的化学式为___________ 。若步骤③配制溶液B操作时间过长,则y会___________ (选填“偏大”“偏小”或“不变”)。

已知:常温下,部分氢氧化物开始沉淀和完全沉淀的pH如下表所示:
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 7.6 | 1.9 | 3.4 | 9.1 |
| 完全沉淀的pH | 9.6 | 3.2 | 4.8 |  |
(1)“气体”的电子式是
(2)下列操作不能显著增大“酸浸”速率的是
a.适当增大稀硫酸的浓度 b.适当升高浸取液的温度 c.增大压强 d.将菱镁矿粉碎
(3)写出反应①的离子方程式:
(4)“调pH”时,合适的pH是
a.1.9 b.3.4 c.7.6 d.9.6
常温下,滴加氨水时,Mg2+的浓度为1.0×10-5 mol⋅L-1时被认为完全沉淀,这时的pH为x,x=
 ,
, )。
)。II.聚合硫酸铁
 是一种无机高分子絮凝剂,可用于水的处理。
是一种无机高分子絮凝剂,可用于水的处理。聚合硫酸铁
 产品的组成可通过下列实验测定:
产品的组成可通过下列实验测定:①称取一定质量的聚合硫酸铁样品配成100.00mL溶液A;
②准确量取20.00mL溶液A,加入足量盐酸酸化后,加BaCl2(ag)至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
③准确量取20.00mL溶液A,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250.00mL溶液B;
④准确量取25.00mL溶液B,用0.1000mol⋅L-1的KMnO4(H+)滴定至终点,消耗KMnO4(ag)8.00mL。
(5)该聚合硫酸铁的化学式为
您最近半年使用:0次
名校
5 . I.已知298K时, ,
, 。
。
(1)向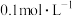 的CH3COONa溶液中逐滴滴加HNO2溶液,当溶液中
的CH3COONa溶液中逐滴滴加HNO2溶液,当溶液中 时,溶液的pH=
时,溶液的pH=___________ (保留2位小数);此时溶液中 为
为___________ (取整数)。
Ⅱ.25℃时,用Na2S沉淀Cu2+、Sn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如下图所示。
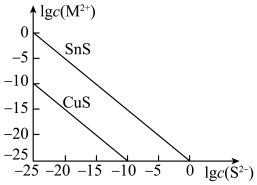
(2)25℃时Ksp(CuS)=___________。
(3)25℃时向50mL的Sn2+、Cu2+浓度均为0.01 的混合溶液中逐滴加入Na2S溶液。当Na2S溶液加到150mL时开始生成SnS沉淀,此时溶液中Cu2+浓度为
的混合溶液中逐滴加入Na2S溶液。当Na2S溶液加到150mL时开始生成SnS沉淀,此时溶液中Cu2+浓度为___________  。
。
 ,
, 。
。(1)向
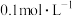 的CH3COONa溶液中逐滴滴加HNO2溶液,当溶液中
的CH3COONa溶液中逐滴滴加HNO2溶液,当溶液中 时,溶液的pH=
时,溶液的pH= 为
为Ⅱ.25℃时,用Na2S沉淀Cu2+、Sn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如下图所示。

(2)25℃时Ksp(CuS)=___________。
A. | B.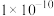 | C. | D. |
(3)25℃时向50mL的Sn2+、Cu2+浓度均为0.01
 的混合溶液中逐滴加入Na2S溶液。当Na2S溶液加到150mL时开始生成SnS沉淀,此时溶液中Cu2+浓度为
的混合溶液中逐滴加入Na2S溶液。当Na2S溶液加到150mL时开始生成SnS沉淀,此时溶液中Cu2+浓度为 。
。
您最近半年使用:0次
名校
解题方法
6 . 运用相关概念和原理,回答下列问题:
(1) 时,水的离子积常数
时,水的离子积常数 值为
值为______ 。
(2)在 的水溶液中,
的水溶液中, ,
, ,
, 与
与 的关系如图所示:
的关系如图所示:
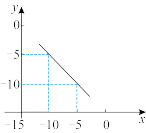
① 下,水的离子积常数为
下,水的离子积常数为________ 。
② 下,
下,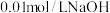 溶液中
溶液中 为
为_______ 
(3)已知 时,
时, 的
的 ,
, 的
的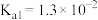 ,
,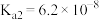 。若氨水的浓度为
。若氨水的浓度为 ,溶液中的
,溶液中的
________  。将
。将 通入该氨水中,当
通入该氨水中,当 降至
降至 时,溶液中的
时,溶液中的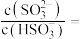
________ 。
(4)在化学分析中采用 为指示剂,以
为指示剂,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,利用
,利用 与
与 生成砖红色沉淀指示到达滴定终点。当溶液中
生成砖红色沉淀指示到达滴定终点。当溶液中 恰好完全沉淀(浓度等于
恰好完全沉淀(浓度等于 )时,溶液中
)时,溶液中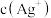 为
为______  ,此时溶液中
,此时溶液中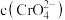 等于
等于________  (已知
(已知 、
、 的
的 分别为
分别为 和
和 )。
)。
(1)
 时,水的离子积常数
时,水的离子积常数 值为
值为(2)在
 的水溶液中,
的水溶液中, ,
, ,
, 与
与 的关系如图所示:
的关系如图所示: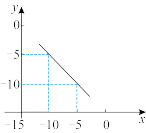
①
 下,水的离子积常数为
下,水的离子积常数为②
 下,
下,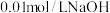 溶液中
溶液中 为
为
(3)已知
 时,
时, 的
的 ,
, 的
的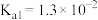 ,
,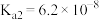 。若氨水的浓度为
。若氨水的浓度为 ,溶液中的
,溶液中的
 。将
。将 通入该氨水中,当
通入该氨水中,当 降至
降至 时,溶液中的
时,溶液中的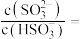
(4)在化学分析中采用
 为指示剂,以
为指示剂,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,利用
,利用 与
与 生成砖红色沉淀指示到达滴定终点。当溶液中
生成砖红色沉淀指示到达滴定终点。当溶液中 恰好完全沉淀(浓度等于
恰好完全沉淀(浓度等于 )时,溶液中
)时,溶液中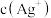 为
为 ,此时溶液中
,此时溶液中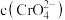 等于
等于 (已知
(已知 、
、 的
的 分别为
分别为 和
和 )。
)。
您最近半年使用:0次
名校
7 . 向两个锥形瓶中各加入0.048g镁条,塞紧橡胶塞,然后用注射器分别注入2 mL 2 mol⋅L 盐酸、2 mL 2 mol⋅L
盐酸、2 mL 2 mol⋅L 醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法错误的是
醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法错误的是
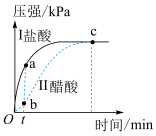
已知: 。
。
 盐酸、2 mL 2 mol⋅L
盐酸、2 mL 2 mol⋅L 醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法错误的是
醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法错误的是
已知:
 。
。A.0~t min内,反应速率 mol⋅L mol⋅L ⋅min ⋅min |
| B.溶液的pH:c>b |
C.反应结束后,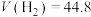 mL(标准状况下) mL(标准状况下) |
D.对于曲线Ⅱ,c点溶液中一定含有 、 、 、 、 和 和 |
您最近半年使用:0次
2024-01-19更新
|
50次组卷
|
2卷引用:四川省自贡市第一中学校2023-2024学年高二上学期期中考试化学试卷
名校
8 . pH定义为 ,
, 定义为
定义为 ,
, 表示25℃时水的离子积常数,则弱酸性溶液中的
表示25℃时水的离子积常数,则弱酸性溶液中的 可表示为
可表示为
 ,
, 定义为
定义为 ,
, 表示25℃时水的离子积常数,则弱酸性溶液中的
表示25℃时水的离子积常数,则弱酸性溶液中的 可表示为
可表示为A. | B. |
C. | D. |
您最近半年使用:0次
9 . 在室温下,下列叙述正确的是
| A.醋酸的电离平衡正向移动时,电离常数一定增大 |
| B.等浓度等体积的醋酸溶液和盐酸分别与氢氧化钠溶液反应,耗碱量相同 |
| C.用pH=1盐酸分别中和等体积pH=13氢氧化钠溶液和氨水,NaOH消耗盐酸的体积大 |
D.pH=2的盐酸与pH=1的硫酸比较,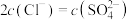 |
您最近半年使用:0次
名校
10 . 已知 是阿伏加德罗常数的值,下列说法不正确的是
是阿伏加德罗常数的值,下列说法不正确的是
 是阿伏加德罗常数的值,下列说法不正确的是
是阿伏加德罗常数的值,下列说法不正确的是A.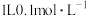 氯化铵溶液含有的 氯化铵溶液含有的 数目小于 数目小于 |
B.在密闭容器中充入 与 与 ,充分反应后转移电子的数目小于 ,充分反应后转移电子的数目小于 |
C. 溶液含有的阳离子数目大于 溶液含有的阳离子数目大于 |
D.常温下,1LpH=2的硫酸溶液中含有的 数目为 数目为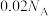 |
您最近半年使用:0次



