1 . 常温下,几种常见的弱酸的电离平衡常数如下表所示:
下列说法中正确的是
| 酸 |  |  |  |  |
| 电离平衡常数 |  |  | 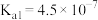  |  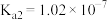 |
A.已知 溶液显酸性,则其中 溶液显酸性,则其中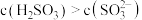 |
B.常温下,浓度均为 的 的 和 和 溶液混合,溶液酸性会减弱 溶液混合,溶液酸性会减弱 |
C.已知漂白性: ,漂白粉配制成溶液后放置在空气中,一段时间后漂白性会减弱 ,漂白粉配制成溶液后放置在空气中,一段时间后漂白性会减弱 |
D.常温下,浓度均为 的三种溶液: 的三种溶液: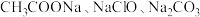 溶液中,碱性最强的是 溶液中,碱性最强的是 |
您最近半年使用:0次
名校
解题方法
2 . 化学反应总伴随着能量变化,研究化学反应中的能量变化对于人类的生产、生活有着重要的意义。回答下列问题:
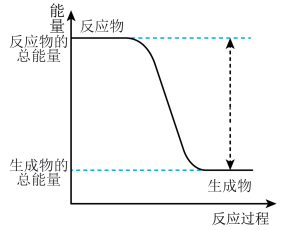
(1)下列化学反应满足图像中能量变化的有___________(填字母)。
(2)乙醇为绿色能源,在 、
、 下,实验测得
下,实验测得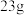 无水乙醇完全燃烧生成二氧化碳气体和液态水时放热
无水乙醇完全燃烧生成二氧化碳气体和液态水时放热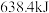 ,写出乙醇燃烧的热化学方程式:
,写出乙醇燃烧的热化学方程式:____________________________________________ 。
(3)已知如下图示关系,则
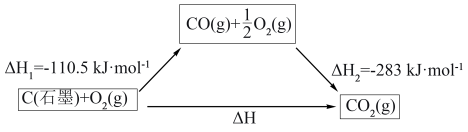
① 的燃烧热
的燃烧热
___________  。
。
②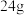 石墨完全燃烧放出的能量是
石墨完全燃烧放出的能量是___________  。
。
(4)中和反应为常见的放热反应,某兴趣小组设计实验探究中和反应反应热的测定[生成 ]。取三只烧杯分别加入
]。取三只烧杯分别加入 溶液,然后分别加入
溶液,然后分别加入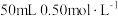 ①稀盐酸、②稀硝酸和③稀醋酸,测得中和反应反应热分别为
①稀盐酸、②稀硝酸和③稀醋酸,测得中和反应反应热分别为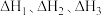 。
。
①醋酸的电离方程式为________________________ ,加入稍过量的碱,目的是____________________________ 。
②假设所有操作均正确,得到的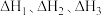 大小关系为
大小关系为______________________ 。

(1)下列化学反应满足图像中能量变化的有___________(填字母)。
| A.石灰石分解 | B.氯化铵与氢氧化钡晶体反应 |
| C.铝热反应 | D.钠与水反应 |
(2)乙醇为绿色能源,在
 、
、 下,实验测得
下,实验测得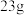 无水乙醇完全燃烧生成二氧化碳气体和液态水时放热
无水乙醇完全燃烧生成二氧化碳气体和液态水时放热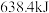 ,写出乙醇燃烧的热化学方程式:
,写出乙醇燃烧的热化学方程式:(3)已知如下图示关系,则

①
 的燃烧热
的燃烧热
 。
。②
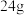 石墨完全燃烧放出的能量是
石墨完全燃烧放出的能量是 。
。(4)中和反应为常见的放热反应,某兴趣小组设计实验探究中和反应反应热的测定[生成
 ]。取三只烧杯分别加入
]。取三只烧杯分别加入 溶液,然后分别加入
溶液,然后分别加入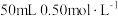 ①稀盐酸、②稀硝酸和③稀醋酸,测得中和反应反应热分别为
①稀盐酸、②稀硝酸和③稀醋酸,测得中和反应反应热分别为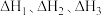 。
。①醋酸的电离方程式为
②假设所有操作均正确,得到的
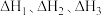 大小关系为
大小关系为
您最近半年使用:0次
名校
3 . 次磷酸(H3PO2)为一元中强酸,具有较强的还原性,可用电渗析法制备,“四室电渗析法”工作原理如图所示。下列叙述正确的是
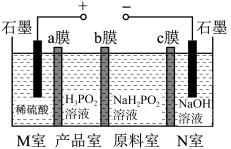

A.次磷酸H3PO2在水溶液中的电离可表示为:H3PO2 3H++PO 3H++PO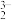 |
B.产品室中发生反应H++H2PO =H3PO2,该法还同时制得硫酸和NaOH两种副产品 =H3PO2,该法还同时制得硫酸和NaOH两种副产品 |
C.a膜和c膜均为阳离子交换膜,a膜可有效防止H2PO 被氧化 被氧化 |
| D.M室和N室石墨电极上产生的气体物质的量之比为2∶1 |
您最近半年使用:0次
2023-10-11更新
|
285次组卷
|
2卷引用:安徽省阜阳市第三中学2023-2024学年高二上学期12月二调(期中)化学试题
名校
4 . 下列电离方程式中正确的是
A.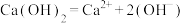 | B. |
C.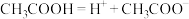 | D.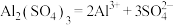 |
您最近半年使用:0次
名校
5 . 已知常温下草酸( )的电离平衡常数为
)的电离平衡常数为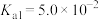 、
、 ;亚硫酸的电离平衡常数为
;亚硫酸的电离平衡常数为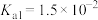 、
、 。
。
(1)草酸的一级电离方程式为___________ ;向草酸钾溶液中通入过量的 ,写出该反应的离子方程式
,写出该反应的离子方程式___________ 。
(2)实验室中用 草酸样品配制成
草酸样品配制成 溶液,然后取出
溶液,然后取出 ,用
,用 的酸性
的酸性 标准溶液滴定该
标准溶液滴定该 草酸溶液,以测定草酸样品的纯度,滴定终点时消耗
草酸溶液,以测定草酸样品的纯度,滴定终点时消耗 标准溶液。
标准溶液。
①下图中能正确表示盛有标准溶液的滴定管滴定前排气泡的操作是___________ (填字母)。
a.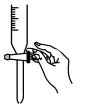 b.
b.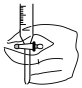 c.
c. 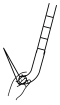 d.
d.
②达到滴定终点的现象是___________ 。该草酸样品中草酸的纯度是___________ (用含a、V的代数式表示)。
 )的电离平衡常数为
)的电离平衡常数为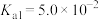 、
、 ;亚硫酸的电离平衡常数为
;亚硫酸的电离平衡常数为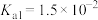 、
、 。
。(1)草酸的一级电离方程式为
 ,写出该反应的离子方程式
,写出该反应的离子方程式(2)实验室中用
 草酸样品配制成
草酸样品配制成 溶液,然后取出
溶液,然后取出 ,用
,用 的酸性
的酸性 标准溶液滴定该
标准溶液滴定该 草酸溶液,以测定草酸样品的纯度,滴定终点时消耗
草酸溶液,以测定草酸样品的纯度,滴定终点时消耗 标准溶液。
标准溶液。①下图中能正确表示盛有标准溶液的滴定管滴定前排气泡的操作是
a.
 b.
b. c.
c.  d.
d.
②达到滴定终点的现象是
您最近半年使用:0次
名校
6 . 向100 mL 0.01 mol·L-1Ba(OH)2溶液中滴加0.1 mol·L-1NaHCO3溶液,测得溶液的电导率变化如图。下列说法正确的是
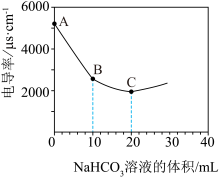

A.NaHCO3在水中的电离方程式为 |
B.A→B的过程中,溶液中 的浓度在逐渐增大 的浓度在逐渐增大 |
C.B→C的过程中,发生反应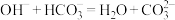 |
| D.B、C两点的阴离子浓度相等 |
您最近半年使用:0次
2023-09-23更新
|
275次组卷
|
7卷引用:安徽省灵璧中学2024届高三上学期一轮复习联考(一)化学试题
7 . 盐湖卤水(主要含 、
、 '、
'、 、
、 、
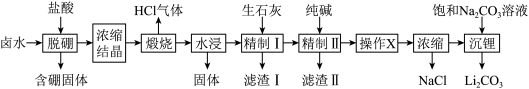
、 和硼酸根等)是锂盐的重要来源,一种以高镁卤水为原料经两段除镁制备Li2CO3的工艺流程如图:
和硼酸根等)是锂盐的重要来源,一种以高镁卤水为原料经两段除镁制备Li2CO3的工艺流程如图:
已知:硼原子有3个价电子,但有4个价轨道,这种价电子数少于价轨道数的原子称作缺电子原子。
常温下 、
、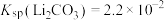 。
。
相关化合物的溶解度与温度的关系如图所示。
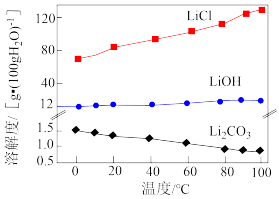
回答下列问题:
(1)含硼固体中的 晶体为层型片状结构,在层与层之间容易裂解,其原因是层与层之间通过
晶体为层型片状结构,在层与层之间容易裂解,其原因是层与层之间通过_______ 结合, 在水中的电离方程式为
在水中的电离方程式为_______ 。
(2) 与
与 溶液反应可制备硼砂
溶液反应可制备硼砂 ,硼砂分子中硼原子的化合价为
,硼砂分子中硼原子的化合价为_______ ;常温下 硼砂溶液中,
硼砂溶液中, 水解生成相同浓度的
水解生成相同浓度的 和
和 ,则溶液
,则溶液
_______ 。
(3)“水浸”后的固体主要成分为_______ (填化学式,下同);精制 后溶液中
后溶液中 的浓度为
的浓度为 ,则常温下精制II过程中
,则常温下精制II过程中 浓度应控制在
浓度应控制在_______  以下。
以下。
(4)精制II的目的是除去滤液中的_______ ,进行操作 的目的是除去溶液中的
的目的是除去溶液中的_______ 。
 、
、 '、
'、 、
、 、
、 和硼酸根等)是锂盐的重要来源,一种以高镁卤水为原料经两段除镁制备Li2CO3的工艺流程如图:
和硼酸根等)是锂盐的重要来源,一种以高镁卤水为原料经两段除镁制备Li2CO3的工艺流程如图:
已知:硼原子有3个价电子,但有4个价轨道,这种价电子数少于价轨道数的原子称作缺电子原子。
常温下
 、
、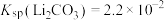 。
。相关化合物的溶解度与温度的关系如图所示。

回答下列问题:
(1)含硼固体中的
 晶体为层型片状结构,在层与层之间容易裂解,其原因是层与层之间通过
晶体为层型片状结构,在层与层之间容易裂解,其原因是层与层之间通过 在水中的电离方程式为
在水中的电离方程式为(2)
 与
与 溶液反应可制备硼砂
溶液反应可制备硼砂 ,硼砂分子中硼原子的化合价为
,硼砂分子中硼原子的化合价为 硼砂溶液中,
硼砂溶液中, 水解生成相同浓度的
水解生成相同浓度的 和
和 ,则溶液
,则溶液
(3)“水浸”后的固体主要成分为
 后溶液中
后溶液中 的浓度为
的浓度为 ,则常温下精制II过程中
,则常温下精制II过程中 浓度应控制在
浓度应控制在 以下。
以下。(4)精制II的目的是除去滤液中的
 的目的是除去溶液中的
的目的是除去溶液中的
您最近半年使用:0次
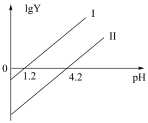
8 . H2X是一种二元弱酸。常温下向H2X溶液中滴加NaOH溶液,混合溶液里lgY[Y表示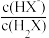 或
或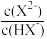 ]随pH的变化关系如图。常温下,下列叙述正确的是
]随pH的变化关系如图。常温下,下列叙述正确的是
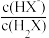 或
或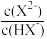 ]随pH的变化关系如图。常温下,下列叙述正确的是
]随pH的变化关系如图。常温下,下列叙述正确的是
A.直线Ⅰ中Y表示的是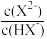 |
| B.电离平衡常数Ka2(H2X)的数量级为10-4 |
| C.pH=7.2时,c(HX-)=1000c(X2-) |
| D.当c(X2-)=c(H2X)时,溶液的pH为2.7 |
您最近半年使用:0次
名校
9 . 下列物质的电离方程式书写正确的是
A.Ba(OH)2=Ba2++(OH) | B.H2CO3 2H++CO 2H++CO |
C.NaHCO3=Na++H++CO | D.NaHSO4=Na++H++SO |
您最近半年使用:0次
名校
10 . 下列有关化学用语表示正确的是
A.中子数为7的碳原子: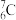 |
B.钙离子的电子式: |
C. 分子的结构式: 分子的结构式: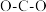 |
D. 的电离方程式: 的电离方程式: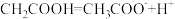 |
您最近半年使用:0次



