名校
解题方法
1 . 下列电离方程式正确的是
A.NaHSO4= Na++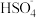 | B.NaHCO3⇌Na++H++ |
C.H3PO4⇌3H++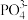 | D.HF ⇌H++F- |
您最近一年使用:0次
2021-06-02更新
|
377次组卷
|
3卷引用:福建省莆田第十五中学2019-2020学年高二下学期期末考试化学试题
2 . 人体内尿酸(HUr)含量偏高,关节滑液中产生尿酸钠晶体(NaUr)会引发痛风,NaUr(s)  Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
已知:①37℃时,Ka(HUr) = 4×10−6,Kw = 2.4×10−14,Ksp(NaUr) = 6.4×10−5
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为_______
(2)Kh为盐的水解常数,37℃时,Kh(Ur−)=_______ 。
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)_______ c(Ur−) (填“>”、“<”或“=”)。
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析出,请写出判断过程_______
(5)对于尿酸偏高的人群,下列建议正确的是_______ 。
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
 Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:已知:①37℃时,Ka(HUr) = 4×10−6,Kw = 2.4×10−14,Ksp(NaUr) = 6.4×10−5
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为
(2)Kh为盐的水解常数,37℃时,Kh(Ur−)=
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析出,请写出判断过程
(5)对于尿酸偏高的人群,下列建议正确的是
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
您最近一年使用:0次
2021-05-27更新
|
711次组卷
|
7卷引用:福建省福州一中2021届高三第五次模拟考试化学试题
福建省福州一中2021届高三第五次模拟考试化学试题海南省海口市2020届高三6月等级模拟试卷化学试题(已下线)第03章 物质在水溶液中的行为(A卷基础强化卷)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)海南省北京师范大学万宁附属中学2021届高三上学期第一次月考化学试题(已下线)第25讲 盐类水解(精练)-2022年高考化学一轮复习讲练测(已下线)第25讲 盐类水解(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第4讲 盐类的水解
名校
3 . 部分弱酸的电离平衡常数如下表:
下列选项正确的是
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K1=1.77×10-4 | K1=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
A.2CN- + H2O + CO2=2HCN + CO |
B.反应HCO +OH-⇌CO +OH-⇌CO +H2O的平衡常数K=5.6×103 +H2O的平衡常数K=5.6×103 |
C.0.1mol/LNa2CO3溶液中:c(H+)= c(OH-)+c(HCO )+2c(H2CO3) )+2c(H2CO3) |
| D.等体积等浓度的HCOONa和NaCN所含阴离子的数目相等 |
您最近一年使用:0次
2021-03-13更新
|
162次组卷
|
2卷引用:福建省龙岩市永定区坎市中学2022-2023学年高三上学期期中化学试题
解题方法
4 . 写出下列物质在水溶液中的电离方程式。
(1)KClO3:_______ ;
(2)HClO :_______ ;
(3)NH4Cl:_______ ;
(1)KClO3:
(2)HClO :
(3)NH4Cl:
您最近一年使用:0次
名校
解题方法
5 . 次磷酸(H3PO2)是一元中强酸,具有较强还原性,下列有关次磷酸及其盐的说法正确的是
A.次磷酸的电离方程式为H3PO2=H++ |
| B.NaH2PO2是次磷酸的正盐,其水溶液呈中性 |
| C.利用(H3PO2)进行化学镀银反应中,1molH3PO2最多还原4molAg+离子 |
| D.白磷与氢氧化钠溶液反应可得次磷酸盐,反应的化学方程式为P4+9NaOH=3Na3PO2+PH3↑+3H2O |
您最近一年使用:0次
2020-10-21更新
|
350次组卷
|
4卷引用:福建省泰宁第一中学2020届高三上学期第二次阶段考试化学试题
福建省泰宁第一中学2020届高三上学期第二次阶段考试化学试题内蒙古赤峰二中2021届高三上学期第二次月考化学试题(已下线)小题必刷32 盐类的水解影响因素及应用——2021年高考化学一轮复习小题必刷(通用版本)湖南省长沙市长郡中学2022-2023学年高三第三次月考化学试题
6 . 下列电离方程式正确的是( )
| A.H2SO4 = H+ + HSO42- | B.H3PO4=3H++ PO43— |
| C.NaHCO3=Na++H++ CO32— | D.CaCO3(熔融)=Ca2+ + CO32- |
您最近一年使用:0次
名校
解题方法
7 . (1)常温下将0.2mol/LHCl溶液与0.2mol/LMOH溶液等体积混合,测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)__ 0.2mol/LHCl溶液中由水电离出的c(H+)。(填“>”“<”或“=”),该混合溶液的物料守恒式为__ 。
(2)常温下若将0.2mol/LMOH溶液与0.1mol/LHCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度__ MCl的水解程度。(填“>”“<”或“=”)。
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH__ 。(填“>7”“<7”或“无法确定”)
(4)某温度时,测得0.01mol/L的NaOH溶液pH为11,在此温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合。若所得混合溶液为中性,且a=12,b=2,求Va∶Vb=__ 。
(2)常温下若将0.2mol/LMOH溶液与0.1mol/LHCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH
(4)某温度时,测得0.01mol/L的NaOH溶液pH为11,在此温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合。若所得混合溶液为中性,且a=12,b=2,求Va∶Vb=
您最近一年使用:0次
名校
解题方法
8 . 在下列物质中选择合适的完成下列各题。
①稀硝酸;②CO;③HF;④熔融NaHSO4;⑤CaO;⑥Cu;⑦蔗糖;⑧Fe2(SO4) 3;⑨酒精;⑩硫酸钡;⑪醋酸;⑫三氧化硫;⑬氯气;⑭醋酸钠
(1) 属于强电解质的是____________________ (填序号,下同) 。
(2) 属于弱电解质的是____________________ 。
(3) 属于非电解质的是_____________________ 。
(4) 写出③、⑭两种物质在水溶液中的电离方程式:③___________________________ ;_________________________________ 。
(5) 醋酸钠溶液显_________ 性(填酸或碱)的原因:______________________________________________________________ (用离子方程式表示)
①稀硝酸;②CO;③HF;④熔融NaHSO4;⑤CaO;⑥Cu;⑦蔗糖;⑧Fe2(SO4) 3;⑨酒精;⑩硫酸钡;⑪醋酸;⑫三氧化硫;⑬氯气;⑭醋酸钠
(1) 属于强电解质的是
(2) 属于弱电解质的是
(3) 属于非电解质的是
(4) 写出③、⑭两种物质在水溶液中的电离方程式:③
(5) 醋酸钠溶液显
您最近一年使用:0次
名校
解题方法
9 . 短周期元素A、B、C、D的位置如图所示,室温下D单质为淡黄色固体。
回答下列问题:
(1)C元素在周期表中的位置___ ,其在自然界中常见的氧化物是___ 晶体。
(2)A的单质在充足的氧气中燃烧得到的产物的结构式是___ ,其分子是__ 分子(“极性”或“非极性”)。
(3)四种元素中可用于航空航天合金材料的制备,其最高价氧化物的水化物的电离方程式为___ 。
(4)与B同周期最活泼的金属是___ ,如何证明它比B活泼?(结合有关的方程式进行说明)__ 。
| A | |||
| B | C | D |
(1)C元素在周期表中的位置
(2)A的单质在充足的氧气中燃烧得到的产物的结构式是
(3)四种元素中可用于航空航天合金材料的制备,其最高价氧化物的水化物的电离方程式为
(4)与B同周期最活泼的金属是
您最近一年使用:0次



