解题方法
1 . 根据实验目的,下列实验设计、现象及结论都正确的是
| 选项 | 实验目的 | 实验设计及现象 | 结论 |
| A | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | Na2CO3溶液中存在水解平衡 |
| B | 判断淀粉是否水解 | 向淀粉溶液中加入少量稀硫酸,加热,再加入银氨溶液,加热后未出现银镜 | 淀粉未水解 |
| C | 比较B和C的非金属性强弱 | 用pH计测定 溶液的pH,H2CO3溶液的pH更小 溶液的pH,H2CO3溶液的pH更小 | 非金属性: |
| D | 判断Fe3+与 的反应是否可逆 的反应是否可逆 | 向 溶液中滴加KSCN溶液,再加入少量 溶液中滴加KSCN溶液,再加入少量 固体,溶液先变成血红色后无明显变化 固体,溶液先变成血红色后无明显变化 | Fe3+与 的反应不可逆 的反应不可逆 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 化学与生产、生活密切相关。下列说法不正确 的是
| A.许多金属或它们的化合物都能发生焰色试验,用于鉴定金属元素 |
| B.明矾可用作净水剂和杀菌消毒剂 |
| C.用纯碱溶液除油污,加热可提高去污能力 |
| D.溴蒸气和NO2都是红棕色气体,可用AgNO3溶液或蒸馏水或CCl4鉴别 |
您最近一年使用:0次
解题方法
3 .  可用作白色颜料和阻燃剂,实验室中可利用
可用作白色颜料和阻燃剂,实验室中可利用 的水解反应制取
的水解反应制取 ,其总反应可表示为
,其总反应可表示为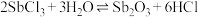 ,下列说法中
,下列说法中不正确 的是
 可用作白色颜料和阻燃剂,实验室中可利用
可用作白色颜料和阻燃剂,实验室中可利用 的水解反应制取
的水解反应制取 ,其总反应可表示为
,其总反应可表示为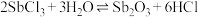 ,下列说法中
,下列说法中A. 水解过程中可能会产生 水解过程中可能会产生 |
B.配制 溶液时可以加入稀盐酸抑制水解 溶液时可以加入稀盐酸抑制水解 |
C.反应前期为促进水解反应的进行,操作时应将 缓慢加入少量水中 缓慢加入少量水中 |
D.为得到较多 ,可在反应后期加入少量氨水 ,可在反应后期加入少量氨水 |
您最近一年使用:0次
4 . 对 溶液进行一系列的实验,根据现象得出的结论
溶液进行一系列的实验,根据现象得出的结论不正确 的是
 溶液进行一系列的实验,根据现象得出的结论
溶液进行一系列的实验,根据现象得出的结论| 选项 | 操作 | 现象 | 结论 |
| A | 往 溶液中逐滴滴加 溶液中逐滴滴加 溶液 溶液 | 溶液变浑浊 |  与 与 反应生成 反应生成 ,说明 ,说明 酸性强于 酸性强于 |
| B |  溶液与 溶液与 溶液混合 溶液混合 | 产生沉淀并有气体冒出 |  和 和 能分别与水电离产生的 能分别与水电离产生的 和 和 反应,且水解相互促进 反应,且水解相互促进 |
| C | 向 溶液中加少量水稀释 溶液中加少量水稀释 | 溶液的碱性增强 | 稀释可以破坏 之间的氢键,使得 之间的氢键,使得 增大,碱性增强 增大,碱性增强 |
| D | 将饱和 溶液加热 溶液加热 | 一段时间后有固体析出 |  分解且生成的 分解且生成的 溶解度比 溶解度比 小而析出 小而析出 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 某研究小组利用电解锰渣(主要成分是MnS,含少量 、
、 、CaO)制备高纯
、CaO)制备高纯 晶体,流程如下:
晶体,流程如下:
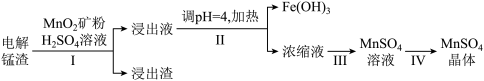
(1)下列有关说法不正确 的是___________。
(2)过程II需持续加热一段时间,目的是___________ 。
(3)过程III除去 并富集
并富集 的原理为:
的原理为: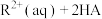 (油相)
(油相) (油相)
(油相) [
[ 表示
表示 或
或 ]。
]。
实验步骤如下:
①调节浓缩液pH,加入溶有HA的磺化煤油,系列操作,分离得水层;
②继续调节水层pH,加入溶有HA的磺化煤油,系列操作,分离得油层;
③向②所得油层中加入试剂X,系列操作,得 溶液。
溶液。
上述步骤中的进行“系列操作”的主要仪器名称是___________ ,试剂X为___________ 。
(4)不同温度下 的溶解度如下表。
的溶解度如下表。
从下列选项中选择“过程IV”的正确操作并排序:___________ 。
将 溶液加热至100℃→_________→________→洗涤→干燥
溶液加热至100℃→_________→________→洗涤→干燥
a.蒸发至出现大量晶体 b.蒸发至溶液表面出现晶膜
c.冷却结晶,过滤 d.趁热过滤
(5) 纯度的测定:准确称取mg产品,加入足量稀硫酸充分溶解后,加入足量
纯度的测定:准确称取mg产品,加入足量稀硫酸充分溶解后,加入足量 固体(不溶于水)将
固体(不溶于水)将 完全转化为
完全转化为 过滤,用
过滤,用 的
的 标准溶液滴定至终点,消耗20.00mL标准溶液,则
标准溶液滴定至终点,消耗20.00mL标准溶液,则 的纯度为
的纯度为___________ (用含m的代数式表示)。
 、
、 、CaO)制备高纯
、CaO)制备高纯 晶体,流程如下:
晶体,流程如下:
(1)下列有关说法
| A.过程I、II均涉及过滤操作 |
B.过程I,适当提高 溶液浓度可提高锰的浸出率 溶液浓度可提高锰的浸出率 |
C.过程I,加 可减少有毒气体的生成 可减少有毒气体的生成 |
| D.过程II,调pH最好选用NaOH溶液 |
(3)过程III除去
 并富集
并富集 的原理为:
的原理为: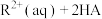 (油相)
(油相) (油相)
(油相) [
[ 表示
表示 或
或 ]。
]。实验步骤如下:
①调节浓缩液pH,加入溶有HA的磺化煤油,系列操作,分离得水层;
②继续调节水层pH,加入溶有HA的磺化煤油,系列操作,分离得油层;
③向②所得油层中加入试剂X,系列操作,得
 溶液。
溶液。上述步骤中的进行“系列操作”的主要仪器名称是
(4)不同温度下
 的溶解度如下表。
的溶解度如下表。| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 52.9 | 62.9 | 60.0 | 53.6 | 45.6 | 35.3 |
将
 溶液加热至100℃→_________→________→洗涤→干燥
溶液加热至100℃→_________→________→洗涤→干燥a.蒸发至出现大量晶体 b.蒸发至溶液表面出现晶膜
c.冷却结晶,过滤 d.趁热过滤
(5)
 纯度的测定:准确称取mg产品,加入足量稀硫酸充分溶解后,加入足量
纯度的测定:准确称取mg产品,加入足量稀硫酸充分溶解后,加入足量 固体(不溶于水)将
固体(不溶于水)将 完全转化为
完全转化为 过滤,用
过滤,用 的
的 标准溶液滴定至终点,消耗20.00mL标准溶液,则
标准溶液滴定至终点,消耗20.00mL标准溶液,则 的纯度为
的纯度为
您最近一年使用:0次
解题方法
6 . 下列实验方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究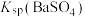 和 和 大小 大小 | 室温下,向浓度均为 的 的 和 和 混合溶液中滴加 混合溶液中滴加 溶液 溶液 | 出现白色沉淀,说明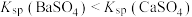 |
| B | 比较 、 、 结合 结合 能力的大小 能力的大小 | 室温下,用pH试纸分别测量0.1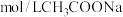 溶液和 溶液和 溶液的pH 溶液的pH | 测得 溶液和NaCN溶液的pH分别为9和11,说明 溶液和NaCN溶液的pH分别为9和11,说明 结合 结合 的能力更强 的能力更强 |
| C | 探究浓度对平衡的影响 | 向试管中加入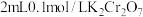 溶液,滴加5~10滴 溶液,滴加5~10滴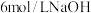 溶液 溶液 | 溶液由黄色变为橙色,说明加入氢氧化钠溶液后平衡向生成 的方向移动 的方向移动 |
| D | 验证铁的吸氧腐蚀 | 将除锈后的铁钉用浓盐酸浸泡后,放入连有导管的具支试管中,塞上橡胶塞,将导管末端浸入水中 | 几分钟后,导管中水柱上升,说明铁发生了吸氧腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 已知 、
、 、
、 、
、 均具有强氧化性,将溶液中的
均具有强氧化性,将溶液中的 、
、 、
、 完沉淀为氢氧化物需溶液的
完沉淀为氢氧化物需溶液的 分别为9.6、6.4、3.7。现有含有
分别为9.6、6.4、3.7。现有含有 杂质的
杂质的 ,首先将其制成水溶液,然后按图示步骤进行提纯:
,首先将其制成水溶液,然后按图示步骤进行提纯:
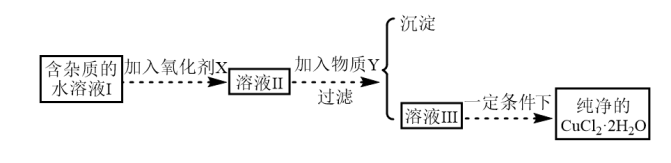
请回答下列问题:
(1)第一步除去 ,能否直接调整
,能否直接调整 将
将 沉淀除去?
沉淀除去?___________ (填“能”或“否”),理由是___________ 。
(2)本实验最适合的氧化剂X是___________ (填标号,下同)。
A. B.
B. C.
C. D.
D.
加入氧化剂的目的是___________ (用相应的离子方程式并加以文字说明)。
(3)物质Y可以是___________ 。
A. B.氨水 C.
B.氨水 C. D.
D. E.
E. F.
F.
(4)题中的“一定条件”的具体流程为:将溶液倒入到___________ (A.坩埚 B.蒸发皿)中,在___________ (C.空气中加热浓缩 D. 气流中加热浓度至
气流中加热浓度至___________ (E.大量晶体析出 F.溶液表面有晶膜析出),冷却结晶,用___________ (G.漏斗 H.分液漏斗)进行___________ (I.过滤 J.分液)。(选择相应的字母填空)
 、
、 、
、 、
、 均具有强氧化性,将溶液中的
均具有强氧化性,将溶液中的 、
、 、
、 完沉淀为氢氧化物需溶液的
完沉淀为氢氧化物需溶液的 分别为9.6、6.4、3.7。现有含有
分别为9.6、6.4、3.7。现有含有 杂质的
杂质的 ,首先将其制成水溶液,然后按图示步骤进行提纯:
,首先将其制成水溶液,然后按图示步骤进行提纯:
请回答下列问题:
(1)第一步除去
 ,能否直接调整
,能否直接调整 将
将 沉淀除去?
沉淀除去?(2)本实验最适合的氧化剂X是
A.
 B.
B. C.
C. D.
D.
加入氧化剂的目的是
(3)物质Y可以是
A.
 B.氨水 C.
B.氨水 C. D.
D. E.
E. F.
F.
(4)题中的“一定条件”的具体流程为:将溶液倒入到
 气流中加热浓度至
气流中加热浓度至
您最近一年使用:0次
23-24高二上·浙江·期末
8 . 工业上主要以确镁矿为原料制备础砂,其废渣硼镁泥的主要成分为MgCO3,还含有少量CaCO3、FeO、Fe2O3、 MnO、SiO2等杂质,经以下流程可制取水合硫酸镁和水合硫酸钙晶体,请回答:
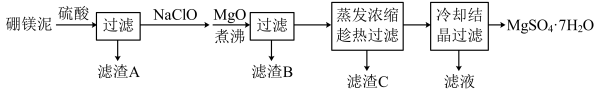
(1)滤渣B中的一种成分为MnO2,则生成MnO2的离子方程式为____________ 。
(2)流程中加入MgO并加热的目的分别是___________ 。
(3)向滤渣C(CaSO4·H2O)加入纯碱溶液,可使其转化为易溶于酸的CaCO3,则在反应后的上层清液中,c( ):c(
):c( )的值为
)的值为_________ [已知:Ksp(CaCO3)=4×10-9,Ksp(CaSO4)=5×10-5]
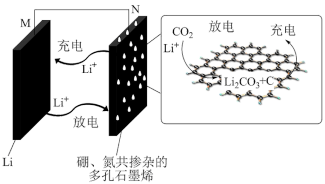
(4)研究人员开发了一种新型的硼、氮共掺杂的多孔石墨烯材料作为正极催化剂的锂-二氧化碳二次电池,实现子碳酸锂在电池中的高度可逆分解,其装置示意图如图所示。根据图示,写出放电时正极的电极反应式为______________ 。

(1)滤渣B中的一种成分为MnO2,则生成MnO2的离子方程式为
(2)流程中加入MgO并加热的目的分别是
(3)向滤渣C(CaSO4·H2O)加入纯碱溶液,可使其转化为易溶于酸的CaCO3,则在反应后的上层清液中,c(
 ):c(
):c( )的值为
)的值为(4)研究人员开发了一种新型的硼、氮共掺杂的多孔石墨烯材料作为正极催化剂的锂-二氧化碳二次电池,实现子碳酸锂在电池中的高度可逆分解,其装置示意图如图所示。根据图示,写出放电时正极的电极反应式为

您最近一年使用:0次
名校
9 . 常温下,下列说法中正确的是
① 溶液加水稀释时,
溶液加水稀释时, 将增大
将增大
②浓度均为0.1 mol/L的 、
、 混合溶液:
混合溶液:
③ 的稀
的稀 与
与 的氨水等体积混合后恰好完全反应,则
的氨水等体积混合后恰好完全反应,则
④物质的量浓度相同的溶液① ②
② ③
③ ,
, 由小到大的顺序是①③②
由小到大的顺序是①③②
①
 溶液加水稀释时,
溶液加水稀释时, 将增大
将增大②浓度均为0.1 mol/L的
 、
、 混合溶液:
混合溶液:
③
 的稀
的稀 与
与 的氨水等体积混合后恰好完全反应,则
的氨水等体积混合后恰好完全反应,则
④物质的量浓度相同的溶液①
 ②
② ③
③ ,
, 由小到大的顺序是①③②
由小到大的顺序是①③②| A.①② | B.①③ | C.②④ | D.③④ |
您最近一年使用:0次
2023-02-17更新
|
266次组卷
|
2卷引用:浙江省嘉兴高级中学2023-2024学年高二上学期期中考试化学试题
10 . 工业上可以利用 的水解反应生成T
的水解反应生成T ,再经焙烧可得
,再经焙烧可得 ,下列有关说法不正确的是
,下列有关说法不正确的是
 的水解反应生成T
的水解反应生成T ,再经焙烧可得
,再经焙烧可得 ,下列有关说法不正确的是
,下列有关说法不正确的是A. 生成 生成 的化学方程式可表示为: 的化学方程式可表示为: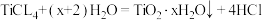 |
| B.制备时可加入大量水,同时加热,促使水解完全 |
C.利用类似方法还可制备SnO、 等化合物 等化合物 |
D. 的性质非常稳定,除制备 的性质非常稳定,除制备 外,还可广泛应用于涂料、橡胶和造纸等 外,还可广泛应用于涂料、橡胶和造纸等 |
您最近一年使用:0次
2023-02-13更新
|
135次组卷
|
2卷引用:浙江省舟山市2022-2023学年高二上学期期末检测化学试题



