1 . 钛白(主要成分 )用途广泛,常用来作高级白色颜料,在造纸工业中作填充剂,合成纤维中作消光剂。制取钛白的方法主要有两种,利用钛铁矿(主要成分
)用途广泛,常用来作高级白色颜料,在造纸工业中作填充剂,合成纤维中作消光剂。制取钛白的方法主要有两种,利用钛铁矿(主要成分 ,还有
,还有 、FeO、
、FeO、 等杂质)为原料,通过硫酸法和氯化法两种生产工艺制备钛白粉的流程如图所示,请回答下列问题:
等杂质)为原料,通过硫酸法和氯化法两种生产工艺制备钛白粉的流程如图所示,请回答下列问题: 形式存在,
形式存在, 在80℃左右水解生成
在80℃左右水解生成
(1)下列状态的钛元素形成的微粒中,电离其最外层的一个电子所需能量最小的是_______(填序号)。
(2)“酸溶”时主要成分发生反应的离子方程式为_______ 。
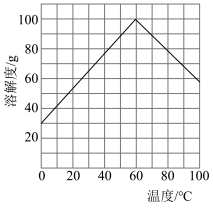
(3)“还原”时应选择合适的试剂X是_______ (填化学式);已知绿矾的溶解度随温度变化的曲线如图所示,从溶液中获得绿矾的操作为_______ 、过滤、洗涤、干燥。 在水中或潮湿空气中会发烟,可用于制作烟幕弹,原因是
在水中或潮湿空气中会发烟,可用于制作烟幕弹,原因是_______ (化学方程式表示)
(5)以上两种工艺流程中,请说出方法一优于方法二的理由_______ (写出一条即可)。
(6) 在自然界中有三种形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种形态中最稳定的一种,其晶胞如图所示,钛的配位数为
在自然界中有三种形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种形态中最稳定的一种,其晶胞如图所示,钛的配位数为_______ ,该晶体的密度为_______  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、b、
,用含a、b、 的代数式表示)。
的代数式表示)。
 )用途广泛,常用来作高级白色颜料,在造纸工业中作填充剂,合成纤维中作消光剂。制取钛白的方法主要有两种,利用钛铁矿(主要成分
)用途广泛,常用来作高级白色颜料,在造纸工业中作填充剂,合成纤维中作消光剂。制取钛白的方法主要有两种,利用钛铁矿(主要成分 ,还有
,还有 、FeO、
、FeO、 等杂质)为原料,通过硫酸法和氯化法两种生产工艺制备钛白粉的流程如图所示,请回答下列问题:
等杂质)为原料,通过硫酸法和氯化法两种生产工艺制备钛白粉的流程如图所示,请回答下列问题: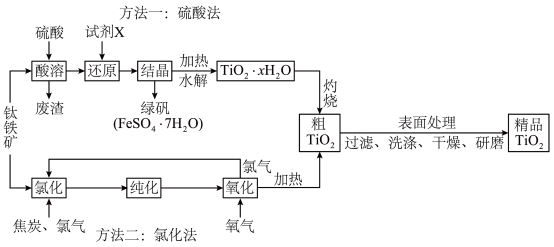
 形式存在,
形式存在, 在80℃左右水解生成
在80℃左右水解生成
(1)下列状态的钛元素形成的微粒中,电离其最外层的一个电子所需能量最小的是_______(填序号)。
A.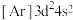 | B. | C.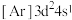 | D.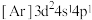 |
(2)“酸溶”时主要成分发生反应的离子方程式为
(3)“还原”时应选择合适的试剂X是
 在水中或潮湿空气中会发烟,可用于制作烟幕弹,原因是
在水中或潮湿空气中会发烟,可用于制作烟幕弹,原因是(5)以上两种工艺流程中,请说出方法一优于方法二的理由
(6)
 在自然界中有三种形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种形态中最稳定的一种,其晶胞如图所示,钛的配位数为
在自然界中有三种形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种形态中最稳定的一种,其晶胞如图所示,钛的配位数为 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、b、
,用含a、b、 的代数式表示)。
的代数式表示)。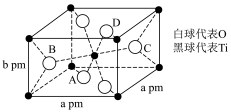
您最近一年使用:0次
名校
2 . 实验是化学的基本方法,它的学习功能是难以代替的,下列实验能达到实验目的的是
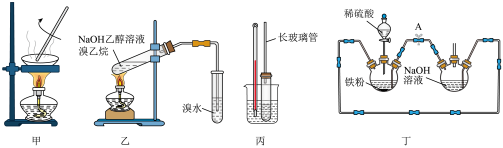
A.用装置甲蒸发 溶液制备少量硫酸镁晶体 溶液制备少量硫酸镁晶体 | B.装置乙中溴水逐渐褪色,能说明生成乙烯 |
| C.装置丙测定苯甲酸在一定温度下的溶解度 | D.装置丁制备少量氢氧化亚铁,并观察其颜色 |
您最近一年使用:0次
3 . 下列关于硫酸的说法正确的是
A.实验室用 与稀硫酸制取 与稀硫酸制取 |
| B.浓硫酸和NaI混合加热制取HI气体 |
C.配制 溶液时加入稀硫酸抑制 溶液时加入稀硫酸抑制 水解 水解 |
| D.苯的硝化反应实验中先将浓硫酸加入浓硝酸中充分混合 |
您最近一年使用:0次
名校
4 . 用下列实验装置进行相应实验,其中装置正确且能达到实验目的的是
|
|
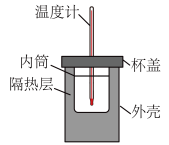
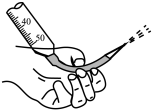
| A.测定中和反应的反应热 | B.为装有 溶液的滴定管排气泡 溶液的滴定管排气泡 |
|
|
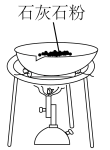
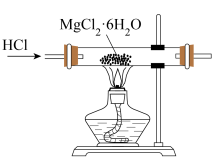
| C.煅烧石灰石 | D.制取无水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 常温下,用含有少量 的
的 溶液制备
溶液制备 的流程如图所示,已知:常温下,
的流程如图所示,已知:常温下,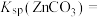
 、
、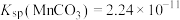 。
。
 的
的 溶液制备
溶液制备 的流程如图所示,已知:常温下,
的流程如图所示,已知:常温下,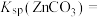
 、
、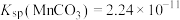 。
。
| A.“除锰”过程中要保持溶液呈较强的碱性 |
B.“沉锌”过程的离子方程式: |
C.为了便于操作,可直接将含 的硫酸锌溶液加入到 的硫酸锌溶液加入到 和氨水的混合溶液中 和氨水的混合溶液中 |
D.检验 中是否含有 中是否含有 的方法是干燥、加热灼烧,将产生的气体通过无水硫酸铜 的方法是干燥、加热灼烧,将产生的气体通过无水硫酸铜 |
您最近一年使用:0次
解题方法
6 . 肉桂酸钠(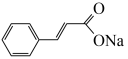 )是一种食品防腐剂,也是一种化妆品成分。某小组探究肉桂酸钠的性质。
)是一种食品防腐剂,也是一种化妆品成分。某小组探究肉桂酸钠的性质。
| 序号 | 操作 | 现象 |
 | 取适量肉桂酸钠溶于水中,滴加酚酞溶液 | 溶液变红色 |
 | 向酸性 溶液中滴加肉桂酸钠溶液,振荡 溶液中滴加肉桂酸钠溶液,振荡 | 溶液褪色 |
 | 向溴水中滴加肉桂酸钠溶液,振荡 | 溶液褪色 |
 可证明肉桂酸是
可证明肉桂酸是(2)由实验
 可知,肉桂酸钠具有
可知,肉桂酸钠具有 中发生反应的类型是
中发生反应的类型是实验(二):探究肉桂酸钠的水解(肉桂酸钠用NaR表示)。
(3)用肉桂酸钠固体配制
 溶液。
溶液。①下列仪器中,配制上述溶液不需要的是

(4)为了探究外界条件对NaR水解的影响,该小组设计如表所示实验:
| 序号 |  溶液/mL 溶液/mL | 蒸馏水/mL | 温度/℃ | 测定pH |
 | 10.0 | 0 | 25 | 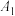 |
 | 5.0 | 5.0 | 25 | 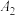 |
 | 10.0 | 0 | 45 |  |
 、
、 的目的是
的目的是②已知NaR水解为吸热反应,甲同学预测:
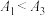 ,实验结果:
,实验结果: ,二者矛盾的主要原因是
,二者矛盾的主要原因是(5)该小组通过测定不同温度下NaR的水解常数
 ,确定温度对NaR水解程度的影响。
,确定温度对NaR水解程度的影响。【查阅资料】
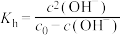 ,
, 为NaR溶液起始浓度。
为NaR溶液起始浓度。试剂和仪器:0.10 mol·L-1NaR溶液、0.100 0 mol·L-1盐酸、甲基橙溶液、pH计。
【设计实验】测定45℃下NaR的水解常数
 ,补充下表中实验。
,补充下表中实验。| 序号 | 实验 | 记录的数据 |
 | 取20.00mLNaR溶液,滴几滴甲基橙溶液,用 盐酸滴定至终点 盐酸滴定至终点 | 盐酸体积为 |
 | 测定45℃纯水的pH |  |
 |  |
【实验处理】
45℃下,

【实验结论】Kh(65℃)>Kh(55℃)>Kh(45℃),升高温度,NaR水解程度增大。
您最近一年使用:0次
名校
7 . 橡胶工业的硫化剂二氯化二硫( ,沸点:
,沸点: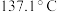 )是一种橙黄色液体,溶于
)是一种橙黄色液体,溶于 、
、 等,易水解,超过
等,易水解,超过 开始分解。可由
开始分解。可由 (沸点:
(沸点: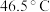 )与
)与 在
在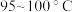 反应制备,同时有
反应制备,同时有 (沸点:
(沸点: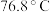 )生成。实验装置(部分夹持仪器已省略)如图所示(E加热装置已省略):
)生成。实验装置(部分夹持仪器已省略)如图所示(E加热装置已省略): ;
; 在
在 以上分解生成
以上分解生成 和
和 。
。
回答下列问题:
(1)利用上述装置制备 ,按气流从左到右的方向连接各仪器接口,正确的顺序是a→
,按气流从左到右的方向连接各仪器接口,正确的顺序是a→____________ (填小写字母,仪器不重复使用)。
(2)装置 中生成
中生成 的化学方程式为
的化学方程式为________________________ 。
(3)仪器X的名称是____________________ ,试剂Y的名称是_______________ 。
(4)实验过程中仪器X中回流的主要物质是____________ (填化学式)。
(5)已知减压条件下可降低液体沸点。实验完成后,对E中混合液选择减压蒸馏,其原因是_________________ 。
(6)本实验对于装置E,需考虑的因素是____________ (任写一种即可)。
(7) 遇水水解时,产生能使品红溶液褪色的气体,写出
遇水水解时,产生能使品红溶液褪色的气体,写出 遇水反应的化学方程式:
遇水反应的化学方程式:_______________ 。
 ,沸点:
,沸点: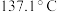 )是一种橙黄色液体,溶于
)是一种橙黄色液体,溶于 、
、 等,易水解,超过
等,易水解,超过 开始分解。可由
开始分解。可由 (沸点:
(沸点: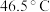 )与
)与 在
在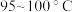 反应制备,同时有
反应制备,同时有 (沸点:
(沸点: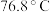 )生成。实验装置(部分夹持仪器已省略)如图所示(E加热装置已省略):
)生成。实验装置(部分夹持仪器已省略)如图所示(E加热装置已省略):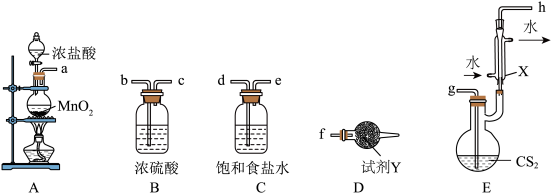
 ;
; 在
在 以上分解生成
以上分解生成 和
和 。
。回答下列问题:
(1)利用上述装置制备
 ,按气流从左到右的方向连接各仪器接口,正确的顺序是a→
,按气流从左到右的方向连接各仪器接口,正确的顺序是a→(2)装置
 中生成
中生成 的化学方程式为
的化学方程式为(3)仪器X的名称是
(4)实验过程中仪器X中回流的主要物质是
(5)已知减压条件下可降低液体沸点。实验完成后,对E中混合液选择减压蒸馏,其原因是
(6)本实验对于装置E,需考虑的因素是
(7)
 遇水水解时,产生能使品红溶液褪色的气体,写出
遇水水解时,产生能使品红溶液褪色的气体,写出 遇水反应的化学方程式:
遇水反应的化学方程式:
您最近一年使用:0次
2024-05-26更新
|
64次组卷
|
2卷引用:2024届河南省信阳市高三下学期高考考前押题理科综合试卷-高中化学
8 . 三氯化硼可用于有机反应催化剂、电子工业等,其熔点为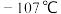 ,沸点为12.5℃,易水解。其制备及纯度测定实验如下:
,沸点为12.5℃,易水解。其制备及纯度测定实验如下:
Ⅰ.制备
将氯气通入装有mg 和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。
和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。
Ⅱ.纯度测定
已知:AgSCN是一种白色沉淀且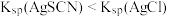 。
。
取反应后 的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
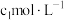
 溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以
溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以 溶液为指示剂,用
溶液为指示剂,用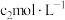 KSCN标准溶液滴定过量
KSCN标准溶液滴定过量 溶液,消耗标准溶液
溶液,消耗标准溶液 。
。
下列说法正确的是)
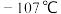 ,沸点为12.5℃,易水解。其制备及纯度测定实验如下:
,沸点为12.5℃,易水解。其制备及纯度测定实验如下:Ⅰ.制备
将氯气通入装有mg
 和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。
和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。Ⅱ.纯度测定
已知:AgSCN是一种白色沉淀且
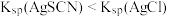 。
。取反应后
 的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
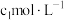
 溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以
溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以 溶液为指示剂,用
溶液为指示剂,用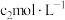 KSCN标准溶液滴定过量
KSCN标准溶液滴定过量 溶液,消耗标准溶液
溶液,消耗标准溶液 。
。下列说法正确的是)
| A.滴入最后半滴标准溶液,溶液由红色变为无色,且半分钟不褪色,说明达到滴定终点 |
B.实验所得产品的产率是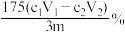 |
| C.若未加硝基苯,则测定结果将偏大 |
D.实验中用碱式滴定管盛放 水解液 水解液 |
您最近一年使用:0次
解题方法
9 . 铬酰氯是一种无机化合物,化学式为 ,熔点:
,熔点: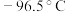 ,沸点:
,沸点: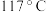 ,常温下为深红棕色液体,遇水剧烈反应产生大量白雾(铬酸、氯化氢)。在实验室中可由重铬酸钾、浓硫酸与氯化钾反应得到铬酰氯,反应机理为:浓硫酸先分别与重铬酸钾和氯化钾反应生成
,常温下为深红棕色液体,遇水剧烈反应产生大量白雾(铬酸、氯化氢)。在实验室中可由重铬酸钾、浓硫酸与氯化钾反应得到铬酰氯,反应机理为:浓硫酸先分别与重铬酸钾和氯化钾反应生成 和氯化氢气体两种中间产物,然后
和氯化氢气体两种中间产物,然后 迅速与氯化氢气体反应生成铬酰氯,实验装置如图(夹持装置略):
迅速与氯化氢气体反应生成铬酰氯,实验装置如图(夹持装置略):
(1)铬酰氯中 元素的化合价为
元素的化合价为___________ 。
(2)装置图中,仪器 的名称分别是
的名称分别是___________ 、___________ 。
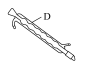
(3)有人建议将仪器B换成如图仪器D,效果会更好,你同意此观点吗?___________ (填“是”或“否”),若不同意,请说出原因:___________ 。 总反应方程式为
总反应方程式为___________ 。
(5)反应结束后,用电热套加热反应装置,收集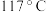 左右的馏分,收集装置选用冰水浴的目的是
左右的馏分,收集装置选用冰水浴的目的是___________ 。
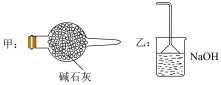
(6)铬酰氯遇水反应的化学方程式为___________ ,据此可知C中应选用下图装置中的___________ (填“甲”或“乙”),不用另一个的主要原因是___________ 。
 ,熔点:
,熔点: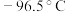 ,沸点:
,沸点: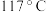 ,常温下为深红棕色液体,遇水剧烈反应产生大量白雾(铬酸、氯化氢)。在实验室中可由重铬酸钾、浓硫酸与氯化钾反应得到铬酰氯,反应机理为:浓硫酸先分别与重铬酸钾和氯化钾反应生成
,常温下为深红棕色液体,遇水剧烈反应产生大量白雾(铬酸、氯化氢)。在实验室中可由重铬酸钾、浓硫酸与氯化钾反应得到铬酰氯,反应机理为:浓硫酸先分别与重铬酸钾和氯化钾反应生成 和氯化氢气体两种中间产物,然后
和氯化氢气体两种中间产物,然后 迅速与氯化氢气体反应生成铬酰氯,实验装置如图(夹持装置略):
迅速与氯化氢气体反应生成铬酰氯,实验装置如图(夹持装置略):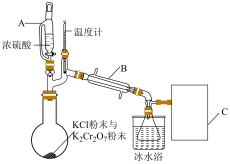
(1)铬酰氯中
 元素的化合价为
元素的化合价为(2)装置图中,仪器
 的名称分别是
的名称分别是(3)有人建议将仪器B换成如图仪器D,效果会更好,你同意此观点吗?
 总反应方程式为
总反应方程式为(5)反应结束后,用电热套加热反应装置,收集
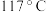 左右的馏分,收集装置选用冰水浴的目的是
左右的馏分,收集装置选用冰水浴的目的是(6)铬酰氯遇水反应的化学方程式为
您最近一年使用:0次
10 . 在工业流程题中常使用 作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对
作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对 与Mn+的反应情况进行了以下探究:
与Mn+的反应情况进行了以下探究:
已知:①Ca2++2 =CaCO3↓+CO2↑+H2O K1=5×104
=CaCO3↓+CO2↑+H2O K1=5×104
②Ca2++2 =Ca(OH)2↓+2CO2↑ K2=1×10-10
=Ca(OH)2↓+2CO2↑ K2=1×10-10
③Cu2++2 =CuCO3↓+CO2↑+H2O K3=8×106
=CuCO3↓+CO2↑+H2O K3=8×106
④Cu2++2 =Cu(OH)2↓+2CO2↑ K4=3×104
=Cu(OH)2↓+2CO2↑ K4=3×104
下列关于该探究实验的叙述正确的是
 作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对
作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对 与Mn+的反应情况进行了以下探究:
与Mn+的反应情况进行了以下探究:| 操作 | 现象 | |
| 1 | 0.5mol·L-1CaCl2溶液与NaHCO3溶液混合 | 产生气泡,生成白色沉淀 |
| 2 | 0.5mol·L-1CuCl2溶液与NaHCO3溶液混合 | 产生气泡,生成蓝色沉淀 |
| 3 | 0.5mol·L-1FeCl3溶液与NaHCO3溶液混合 | 产生大量气泡,生成红褐色沉淀 |
| 4 | 取2中的蓝色沉淀加热并将产物依次通过无水CuSO4和澄清石灰水 | 无水CuSO4变蓝,澄清石灰水变浑浊 |
 =CaCO3↓+CO2↑+H2O K1=5×104
=CaCO3↓+CO2↑+H2O K1=5×104②Ca2++2
 =Ca(OH)2↓+2CO2↑ K2=1×10-10
=Ca(OH)2↓+2CO2↑ K2=1×10-10③Cu2++2
 =CuCO3↓+CO2↑+H2O K3=8×106
=CuCO3↓+CO2↑+H2O K3=8×106④Cu2++2
 =Cu(OH)2↓+2CO2↑ K4=3×104
=Cu(OH)2↓+2CO2↑ K4=3×104下列关于该探究实验的叙述正确的是
| A.实验1生成的沉淀为Ca(OH)2 |
| B.实验2生成的沉淀为Cu(OH)2 |
C. 与M2+反应生成MCO3沉淀的离子方程式为M2++ 与M2+反应生成MCO3沉淀的离子方程式为M2++ =MCO3↓+H+ =MCO3↓+H+ |
D.实验3发生反应的离子方程式为Fe3++3 =Fe(OH)3↓+3CO2↑ =Fe(OH)3↓+3CO2↑ |
您最近一年使用:0次