解题方法
1 . 化学与生活、生产密切相关,下列说法不正确 的是
| A.用涂抹NaOH溶液的方法处理粘在手掌上的稀硫酸 |
| B.用在铁壳外表面连接镁块的方法预防海船腐蚀 |
| C.服用Na2SO4溶液缓解误食BaCl2造成的中毒 |
| D.用氯化铵和氯化锌溶液去除铁器表面的锈迹 |
您最近一年使用:0次
名校
解题方法
2 . 下列所示的物质间转化均能实现的是
A.MnO2(s)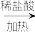 Cl2(g) Cl2(g) 漂白粉 漂白粉 |
B.S(s)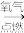 SO3(g) SO3(g) H2SO4(aq) H2SO4(aq) |
C.Cu(s) NO2(g) NO2(g) HNO3(aq) HNO3(aq) |
D.MgCl2(aq) MgCl2·6H2O(s) MgCl2·6H2O(s)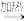 MgCl2(s) MgCl2(s) |
您最近一年使用:0次
解题方法
3 . 在给定条件下,下列关于物质间的转化能实现的是
A.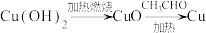 |
B.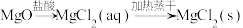 |
C.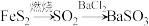 |
D.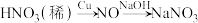 |
您最近一年使用:0次
解题方法
4 . 下列操作能促进水的电离且溶液呈酸性的是
| A.向水中加入Na2CO3溶液 | B.向水中加入NaHSO4溶液 |
| C.将水加热到100℃,使pH=6 | D.向水中加入NH4Cl固体 |
您最近一年使用:0次
5 . 下列说法不正确的是
| A.容量瓶、分液漏斗、滴定管使用前均要检漏 |
| B.pH计可用于酸碱中和滴定终点的判断 |
| C.用酸式滴定管量取20.00mL酸性KMnO4溶液 |
| D.将氯化镁溶液蒸干,可制得无水氯化镁固体 |
您最近一年使用:0次
名校
解题方法
6 . 周期表中ⅥA族元素及其化合物应用广泛。 具有杀菌、消毒、漂白等作用;
具有杀菌、消毒、漂白等作用; 是一种易燃的有毒气体(燃烧热为
是一种易燃的有毒气体(燃烧热为 ),常用于沉淀重金属离子;硫酰氯(
),常用于沉淀重金属离子;硫酰氯( )是重要的化工试剂,在催化剂作用下合成反应为
)是重要的化工试剂,在催化剂作用下合成反应为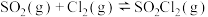
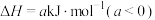 ;硒(
;硒(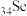 )和碲(
)和碲(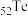 )的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,
)的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景, 具有较强的还原性,工业上通过电解强碱性
具有较强的还原性,工业上通过电解强碱性 溶液制备Te。下列方程式书写正确的是
溶液制备Te。下列方程式书写正确的是
 具有杀菌、消毒、漂白等作用;
具有杀菌、消毒、漂白等作用; 是一种易燃的有毒气体(燃烧热为
是一种易燃的有毒气体(燃烧热为 ),常用于沉淀重金属离子;硫酰氯(
),常用于沉淀重金属离子;硫酰氯( )是重要的化工试剂,在催化剂作用下合成反应为
)是重要的化工试剂,在催化剂作用下合成反应为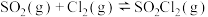
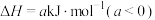 ;硒(
;硒(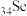 )和碲(
)和碲(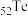 )的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,
)的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景, 具有较强的还原性,工业上通过电解强碱性
具有较强的还原性,工业上通过电解强碱性 溶液制备Te。下列方程式书写正确的是
溶液制备Te。下列方程式书写正确的是A. 遇水强烈水解生成两种酸: 遇水强烈水解生成两种酸: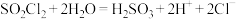 |
B.CuSe和浓硫酸反应: |
C. 的燃烧: 的燃烧:  |
D.电解强碱性 溶液的阴极反应: 溶液的阴极反应: |
您最近一年使用:0次
名校
解题方法
7 . 某研究小组利用 的还原性提纯
的还原性提纯 并制取
并制取 的方案如下:
的方案如下:不正确 的是
 的还原性提纯
的还原性提纯 并制取
并制取 的方案如下:
的方案如下: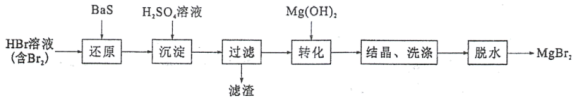
A.“沉淀”步骤中不可使用 溶液代替硫酸 溶液代替硫酸 |
B.滤渣中只有 |
C.“转化”步骤中发生反应的离子方程式为 |
D.将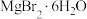 晶体在溴化氢气氛中加热得到 晶体在溴化氢气氛中加热得到 固体 固体 |
您最近一年使用:0次
名校
解题方法
8 . 回收锑冶炼厂的砷碱渣中砷的过程可表示为:

已知:①砷碱渣主要含Na3AsO4、Na[Sb(OH)6]、SiO2即少量砷的硫化物;
②25 ℃ Ka1(H3AsO4)=6×10-3、Ka[HSb(OH)6]=2.8×10-3、Ksp[Ca(OH)2]=a、Ksp[Ca5(AsO4)3(OH)]=b。
(1)“水浸”后所得溶液呈碱性,其原因可能是_______ 。
(2)“沉砷”过程发生反应: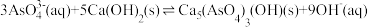 ,该反应的平衡常数K可以表示为
,该反应的平衡常数K可以表示为_______ (用含a、b的表达式作答)。
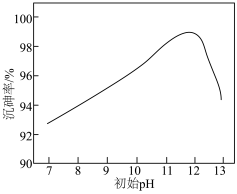
(3)在常温下,调节“过滤1”所得滤液的pH,沉砷率与滤液初始pH的关系如图所示。pH<12时,沉砷率随pH增大而增大的原因可能是_______ 。
(4)已知:硫代锑酸钠(Na3SbS4)易溶于水,在碱性溶液中较稳定。
①“过滤2”所得滤液中加入Na2S可以将Na[Sb(OH)6]转化为Na3SbS4,该反应的离子方程式为_______ 。
② Na2S须过量,原因是_______ 。
(5)“还原”步骤中,Ca5(AsO4)3(OH)先分解为Ca3(AsO4)2, Ca3(AsO4)2与C反应生成CO和砷蒸气,其物质的量之比为10:1。蒸气中砷分子为正四面体结构,其化学式为_______ 。
(6)砷的硫化物在自然界中主要为As4S6、As4S4等。已知As4S6中所有原子均为8电子稳定结构,且不存在四元环结构,不含As-As键和S-S键。其结构式可表示为_______ 。

已知:①砷碱渣主要含Na3AsO4、Na[Sb(OH)6]、SiO2即少量砷的硫化物;
②25 ℃ Ka1(H3AsO4)=6×10-3、Ka[HSb(OH)6]=2.8×10-3、Ksp[Ca(OH)2]=a、Ksp[Ca5(AsO4)3(OH)]=b。
(1)“水浸”后所得溶液呈碱性,其原因可能是
(2)“沉砷”过程发生反应:
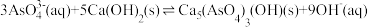 ,该反应的平衡常数K可以表示为
,该反应的平衡常数K可以表示为(3)在常温下,调节“过滤1”所得滤液的pH,沉砷率与滤液初始pH的关系如图所示。pH<12时,沉砷率随pH增大而增大的原因可能是

(4)已知:硫代锑酸钠(Na3SbS4)易溶于水,在碱性溶液中较稳定。
①“过滤2”所得滤液中加入Na2S可以将Na[Sb(OH)6]转化为Na3SbS4,该反应的离子方程式为
② Na2S须过量,原因是
(5)“还原”步骤中,Ca5(AsO4)3(OH)先分解为Ca3(AsO4)2, Ca3(AsO4)2与C反应生成CO和砷蒸气,其物质的量之比为10:1。蒸气中砷分子为正四面体结构,其化学式为
(6)砷的硫化物在自然界中主要为As4S6、As4S4等。已知As4S6中所有原子均为8电子稳定结构,且不存在四元环结构,不含As-As键和S-S键。其结构式可表示为
您最近一年使用:0次
名校
解题方法
9 . 下列说法不正确的是
| A.Na2CO3溶液呈碱性,可用于去除油污 |
| B.NH4Cl溶液呈酸性,可用于除铁锈 |
C.1 L 0.1 mol/L Na2CO3溶液中含 数为0.1NA 数为0.1NA |
| D.明矾溶于水能形成胶体,可用于净水 |
您最近一年使用:0次
名校
解题方法
10 . 高锰酸钾生产过程中产生的废锰矿(主要成分为 和
和 )可用于制备
)可用于制备 固体,工艺流程如下:
固体,工艺流程如下:

该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
回答以下问题:
(1)加入的 与
与 反应为
反应为 和
和 ,“调pH”步骤中,应调节pH范围为
,“调pH”步骤中,应调节pH范围为___________ ,滤渣3的主要成分为:___________
(2)取4.00 g 固体样品溶于适量水中,加硫酸酸化,用过量
固体样品溶于适量水中,加硫酸酸化,用过量 (难溶于水)将其完全氧化为
(难溶于水)将其完全氧化为 ,过滤,洗涤。洗涤滤液并入滤液后,用
,过滤,洗涤。洗涤滤液并入滤液后,用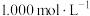
 溶液滴定至终点,消耗溶液50.00 mL。发生的反应为:
溶液滴定至终点,消耗溶液50.00 mL。发生的反应为: ,计算样品中
,计算样品中 的质量分数
的质量分数___________ (写出计算过程)。
 和
和 )可用于制备
)可用于制备 固体,工艺流程如下:
固体,工艺流程如下:
该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |
| 开始沉淀pH | 2.10 | 9.27 |
| 完全沉淀pH | 3.20 | 10.87 |
(1)加入的
 与
与 反应为
反应为 和
和 ,“调pH”步骤中,应调节pH范围为
,“调pH”步骤中,应调节pH范围为(2)取4.00 g
 固体样品溶于适量水中,加硫酸酸化,用过量
固体样品溶于适量水中,加硫酸酸化,用过量 (难溶于水)将其完全氧化为
(难溶于水)将其完全氧化为 ,过滤,洗涤。洗涤滤液并入滤液后,用
,过滤,洗涤。洗涤滤液并入滤液后,用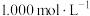
 溶液滴定至终点,消耗溶液50.00 mL。发生的反应为:
溶液滴定至终点,消耗溶液50.00 mL。发生的反应为: ,计算样品中
,计算样品中 的质量分数
的质量分数
您最近一年使用:0次



