名校
解题方法
1 . 在pH=1且含有大量 和
和 的溶液中,能大量存在的阴离子是
的溶液中,能大量存在的阴离子是
 和
和 的溶液中,能大量存在的阴离子是
的溶液中,能大量存在的阴离子是A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
2 . 食醋是烹饪美食的调味品,有效成分主要为醋酸(用 表示)。
表示)。 的应用与其电离平衡密切相关。25℃时,
的应用与其电离平衡密切相关。25℃时, 的
的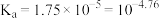 。
。
(1)配制250ml 0.1mol·L-1的 溶液,需
溶液,需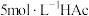 溶液的体积为
溶液的体积为___________ mL。
(2)下列关于 容量瓶的操作,正确的是___________。
容量瓶的操作,正确的是___________。
(3)某小组研究25℃下 电离平衡的影响因素。
电离平衡的影响因素。
提出假设。稀释 溶液或改变
溶液或改变 浓度,
浓度, 电离平衡会发生移动。设计方案并完成实验用浓度均为
电离平衡会发生移动。设计方案并完成实验用浓度均为 的
的 和
和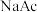 溶液,按下表配制总体积相同的系列溶液;测定
溶液,按下表配制总体积相同的系列溶液;测定 ,记录数据。
,记录数据。
①根据表中信息,补充数据:
___________ ,
___________ 。
②由实验Ⅰ和Ⅱ可知,稀释 溶液,电离平衡
溶液,电离平衡___________ (填”正”或”逆”)向移动;结合表中数据,给出判断理由:___________ 。
③由实验Ⅱ~VIII可知,增大 浓度,
浓度, 电离平衡逆向移动。
电离平衡逆向移动。
实验结论假设成立。
(4)小组分析上表数据发现:随着 的增加,
的增加, 的值逐渐接近
的值逐渐接近 的
的 。
。
查阅资料获悉:一定条件下,按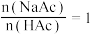 配制的溶液中,
配制的溶液中, 的值等于
的值等于 的
的 。
。
对比数据发现,实验VIII中 与资料数据
与资料数据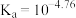 存在一定差异;推测可能由物质浓度准确程度不够引起,故先准确测定
存在一定差异;推测可能由物质浓度准确程度不够引起,故先准确测定 溶液的浓度再验证。移取
溶液的浓度再验证。移取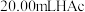 溶液,加入2滴酚酞溶液,用
溶液,加入2滴酚酞溶液,用 溶液滴定至终点,消耗体积为
溶液滴定至终点,消耗体积为 ,则该
,则该 溶液的浓度为
溶液的浓度为___________  ,滴定至终点时现象为
,滴定至终点时现象为___________ 。
 表示)。
表示)。 的应用与其电离平衡密切相关。25℃时,
的应用与其电离平衡密切相关。25℃时, 的
的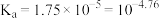 。
。(1)配制250ml 0.1mol·L-1的
 溶液,需
溶液,需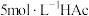 溶液的体积为
溶液的体积为(2)下列关于
 容量瓶的操作,正确的是___________。
容量瓶的操作,正确的是___________。A.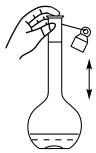 | B.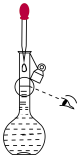 | C.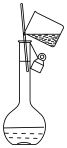 | D.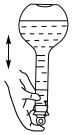 |
(3)某小组研究25℃下
 电离平衡的影响因素。
电离平衡的影响因素。提出假设。稀释
 溶液或改变
溶液或改变 浓度,
浓度, 电离平衡会发生移动。设计方案并完成实验用浓度均为
电离平衡会发生移动。设计方案并完成实验用浓度均为 的
的 和
和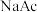 溶液,按下表配制总体积相同的系列溶液;测定
溶液,按下表配制总体积相同的系列溶液;测定 ,记录数据。
,记录数据。| 序号 | 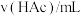 | 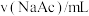 | 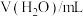 | 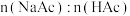 |  |
| Ⅰ | 40.00 | / | / | 0 | 2.86 |
| Ⅱ | 4.00 | / | 36.00 | 0 | 3.36 |
| … | |||||
| Ⅶ | 4.00 | a | b | 3:4 | 4.53 |
| Ⅷ | 4.00 | 4.00 | 32.00 | 1:1 | 4.65 |


②由实验Ⅰ和Ⅱ可知,稀释
 溶液,电离平衡
溶液,电离平衡③由实验Ⅱ~VIII可知,增大
 浓度,
浓度, 电离平衡逆向移动。
电离平衡逆向移动。实验结论假设成立。
(4)小组分析上表数据发现:随着
 的增加,
的增加, 的值逐渐接近
的值逐渐接近 的
的 。
。查阅资料获悉:一定条件下,按
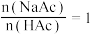 配制的溶液中,
配制的溶液中, 的值等于
的值等于 的
的 。
。对比数据发现,实验VIII中
 与资料数据
与资料数据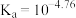 存在一定差异;推测可能由物质浓度准确程度不够引起,故先准确测定
存在一定差异;推测可能由物质浓度准确程度不够引起,故先准确测定 溶液的浓度再验证。移取
溶液的浓度再验证。移取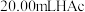 溶液,加入2滴酚酞溶液,用
溶液,加入2滴酚酞溶液,用 溶液滴定至终点,消耗体积为
溶液滴定至终点,消耗体积为 ,则该
,则该 溶液的浓度为
溶液的浓度为 ,滴定至终点时现象为
,滴定至终点时现象为
您最近一年使用:0次
名校
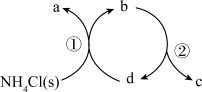
3 . 一种分解氯化铵实现产物分离的物质转化关系如下,其中b、d代表 或
或 中的一种。下列说法正确的是
中的一种。下列说法正确的是
 或
或 中的一种。下列说法正确的是
中的一种。下列说法正确的是
| A.实验室可以利用加热氯化铵分解制备氨气 |
B.a、c分别是 、 、 |
C.d既可以是 ,也可以是 ,也可以是 |
D.已知 为副产物,则通入水蒸气可减少 为副产物,则通入水蒸气可减少 的产生 的产生 |
您最近一年使用:0次
2023-09-23更新
|
504次组卷
|
3卷引用:吉林省长春市东北师范大学附属中学2023-2024学年高三上学期9月一模化学试题
吉林省长春市东北师范大学附属中学2023-2024学年高三上学期9月一模化学试题(已下线)专题02 元素化合物 有机化合物-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)黑龙江省肇东市第四中学校2023-2024学年高三上学期第二次月考化学试卷
名校
解题方法
4 . 请根据有关知识,填写下列空白:
(1)一种难溶的废弃矿渣杂卤石,其主要成分可表示为K2SO4·MgSO4·2CaSO4·2H2O,已知它在水溶液中存在如下平衡:K2SO4·MgSO4·2CaSO4·2H2O(s) 2K+(aq)+4
2K+(aq)+4 (aq)+Mg2+(aq)+2Ca2+(aq)+2H2O(l)。
(aq)+Mg2+(aq)+2Ca2+(aq)+2H2O(l)。
用化学平衡移动原理解释Ca(OH)2溶液能溶解出杂卤石中K+的原因:_____ 。
(2)向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L−1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.8×10−10,忽略溶液的体积变化,请计算:完全沉淀后,溶液中c(Ag+)=_____ mol·L−1.
(3)N2H4是一种高效清洁的火箭燃料。0.25molN2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量。
写出N2H4(g)完全燃烧生成氮气和气态水热化学方程式_____ 。
(4)硫酸亚铁溶液常压蒸干得到的固体物质是_____ ,原因是_____ 。
(5)NH4Cl溶液可作焊接时的除锈剂,原因是_____ 。
(1)一种难溶的废弃矿渣杂卤石,其主要成分可表示为K2SO4·MgSO4·2CaSO4·2H2O,已知它在水溶液中存在如下平衡:K2SO4·MgSO4·2CaSO4·2H2O(s)
 2K+(aq)+4
2K+(aq)+4 (aq)+Mg2+(aq)+2Ca2+(aq)+2H2O(l)。
(aq)+Mg2+(aq)+2Ca2+(aq)+2H2O(l)。用化学平衡移动原理解释Ca(OH)2溶液能溶解出杂卤石中K+的原因:
(2)向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L−1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.8×10−10,忽略溶液的体积变化,请计算:完全沉淀后,溶液中c(Ag+)=
(3)N2H4是一种高效清洁的火箭燃料。0.25molN2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量。
写出N2H4(g)完全燃烧生成氮气和气态水热化学方程式
(4)硫酸亚铁溶液常压蒸干得到的固体物质是
(5)NH4Cl溶液可作焊接时的除锈剂,原因是
您最近一年使用:0次
名校
解题方法
5 . 25℃时,如果取0.1mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8。回答以下问题:
(1)混合溶液的pH=8的原因:_______ (用离子方程式表示)。
(2)混合溶液中由水电离出的c(OH-)_______ (填“>”“<”或“=”)0.1mol·L-1NaOH溶液中由水电离出的c(OH-)。
(3)混合溶液中c(OH-)-c(HA)=_______ mol·L-1。
(4)同温度下,等浓度的四种盐溶液中c(NH )由大到小的顺序是
)由大到小的顺序是_______ (填字母)。
A.NH4HSO4 B.NH4A C.(NH4)2SO4 D.NH4Cl
(1)混合溶液的pH=8的原因:
(2)混合溶液中由水电离出的c(OH-)
(3)混合溶液中c(OH-)-c(HA)=
(4)同温度下,等浓度的四种盐溶液中c(NH
 )由大到小的顺序是
)由大到小的顺序是A.NH4HSO4 B.NH4A C.(NH4)2SO4 D.NH4Cl
您最近一年使用:0次
2023-09-15更新
|
361次组卷
|
2卷引用:吉林省长春市第八中学2022-2023学年高二上学期11月期中考试化学试题
名校
6 . 回答下列问题:
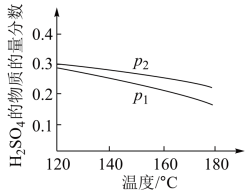
(1)对反应:3SO2(g)+2H2O(g)=2H2SO4(l)+S(s) ΔH2=−254kJ·mol−1,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。p2_____ p1(填“>”或“<”),得出该结论的理由是_____ 。
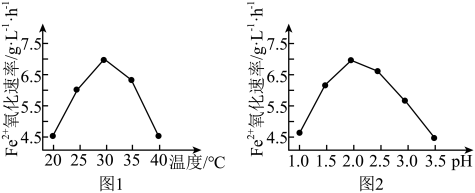
(2)已知:生物脱H2S的原理:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
由图1和图2判断使用硫杆菌的最佳条件为_____ 。若反应温度过高,反应速率下降,其原因是_____ 。
(3)在常温下,某硫酸和硫酸铝两种溶液的pH都是3,那么硫酸中水电离出的c(H+)是硫酸铝溶液中水电离出的c(H+)的_____ 倍
(4)常温下pH=4的FeCl3溶液和pH=10的K2CO3溶液中,水的电离程度前者_____ 后者(填“大于”、“等于”、“小于”)。
(1)对反应:3SO2(g)+2H2O(g)=2H2SO4(l)+S(s) ΔH2=−254kJ·mol−1,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。p2


(2)已知:生物脱H2S的原理:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4
 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O由图1和图2判断使用硫杆菌的最佳条件为
(3)在常温下,某硫酸和硫酸铝两种溶液的pH都是3,那么硫酸中水电离出的c(H+)是硫酸铝溶液中水电离出的c(H+)的
(4)常温下pH=4的FeCl3溶液和pH=10的K2CO3溶液中,水的电离程度前者
您最近一年使用:0次
名校
7 . 常温下,下列各组离子在指定溶液中一定能大量共存的有几项
A.无色溶液中:K+、 、 、 、Al3+ 、Al3+ |
B.水电离出的c(H+)=1×10−13mol/L的溶液中: 、 、 、 、 、 、 |
C.无色溶液中:K+、 、 、 、 、 |
D.pH=10的溶液中: 、Na+、 、Na+、 、 、 |
您最近一年使用:0次
2023-08-28更新
|
164次组卷
|
3卷引用:吉林省长春市朝阳区长春外国语学校2022-2023学年高二上学期11月期中化学试题
名校
8 . 下列对实验操作和现象的解释与结论正确的是
| 操作和现象 | 解释与结论 | |
| A | 常温下用pH试纸测得等浓度CH3COONa溶液的pH为9,NaNO2溶液的pH为8 | Ka(HNO2)>Ka(CH3COOH) |
| B | 向蔗糖溶液中滴加几滴稀硫酸,加热几分钟,然后加入银氨溶液,水浴加热,不能发生银镜反应 | 蔗糖未发生水解 |
| C | 室温下,向密闭容器中充入NO2,达平衡后,再慢慢扩大容器体积,最终容器中气体颜色比初次平衡时浅 | 2NO2(红棕色)⇌N2O4(无色)该平衡正向移动 |
| D | 向NaAlO2溶液中加入NaHCO3溶液,有白色沉淀生成 |  与 与 发生了剧烈的双水解反应 发生了剧烈的双水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-10更新
|
95次组卷
|
3卷引用:吉林省通化市梅河口市第五中学2022-2023学年高二下学期7月期末考试化学试题
2023高三·全国·专题练习
名校
9 . 下列各离子组中,因水解相互促进以致水解完全而不能大量共存的离子组是
A.H2PO 、Na+、Cl-、OH- 、Na+、Cl-、OH- | B.Pb2+、Hg2+、S2-、SO |
C.H+、Fe2+、NO 、SO 、SO | D.S2-、Na+、Cl-、Al3+ |
您最近一年使用:0次
2023-06-28更新
|
976次组卷
|
3卷引用:吉林省长春市第五中学2022-2023学年高二下学期第三学程(期末)化学试题
吉林省长春市第五中学2022-2023学年高二下学期第三学程(期末)化学试题吉林省长春市实验中学2022-2023学年高二下学期期末考试化学试题(已下线)第3讲 离子反应的应用(离子共存、离子检验和推断)
10 .  为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.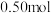 异丁烷分子中共价键的数目为 异丁烷分子中共价键的数目为 |
B.标准状况下, 中电子的数目为 中电子的数目为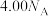 |
C. 的 的 溶液中 溶液中 的数目为 的数目为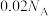 |
D. 的 的 溶液中 溶液中 的数目为 的数目为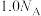 |
您最近一年使用:0次
2023-06-09更新
|
17132次组卷
|
23卷引用:吉林省通化市梅河口市博文学校2022-2023学年高二下学期期末考试化学试题
吉林省通化市梅河口市博文学校2022-2023学年高二下学期期末考试化学试题2023年高考全国甲卷化学真题(已下线)T10-阿伏伽德罗常数(已下线)2023年高考化学真题完全解读(全国甲卷)(ppt+word)(已下线)专题03 阿伏伽德罗常数的应用(已下线)专题03 阿伏伽德罗常数的应用(已下线)专题03 阿伏伽德罗常数的应用(已下线)考点06 物质的量 气体摩尔体积(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点02 物质的量 气体摩尔体积(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第9讲 物质的量浓度(已下线)专题03 化学计量-2023年高考化学真题题源解密(全国通用)福建省福州铜盘中学2022-2023学年高二下学期期末考试化学试题(已下线)专题03 阿伏加德罗常数与化学计算 -2023年高考化学真题题源解密(新高考专用)甘肃省武威市凉州区2024届高三上学期第一次诊断考试化学试题辽宁省沈阳市新民市高级中学2023-2024学年高三上学期10月月考化学试题福建省莆田第二十五中学2023-2024学年高三上学期期中考试化学试题(已下线)题型02 阿伏加德罗常数的判断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型09 有机物的结构与性质-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)福建省福州第十五中学2022-2023学年高二下学期期末考试化学试题云南省大理市下关第一中学2023-2024学年高二下学期3月月考化学试题福建省莆田五中2023-2024学年高二上学期第三次月考化学试卷 (已下线)FHgkyldyjhx02江西省南昌市八一中学2024届高三下学期三模测试化学试题



