下列对实验操作和现象的解释与结论正确的是
| 操作和现象 | 解释与结论 | |
| A | 常温下用pH试纸测得等浓度CH3COONa溶液的pH为9,NaNO2溶液的pH为8 | Ka(HNO2)>Ka(CH3COOH) |
| B | 向蔗糖溶液中滴加几滴稀硫酸,加热几分钟,然后加入银氨溶液,水浴加热,不能发生银镜反应 | 蔗糖未发生水解 |
| C | 室温下,向密闭容器中充入NO2,达平衡后,再慢慢扩大容器体积,最终容器中气体颜色比初次平衡时浅 | 2NO2(红棕色)⇌N2O4(无色)该平衡正向移动 |
| D | 向NaAlO2溶液中加入NaHCO3溶液,有白色沉淀生成 |  与 与 发生了剧烈的双水解反应 发生了剧烈的双水解反应 |
| A.A | B.B | C.C | D.D |
更新时间:2023-07-10 13:15:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法不正确的是
| A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 |
| B.2014年西非国家爆发了埃博拉疫情,埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 |
| C.金属着火时,可用细沙覆盖灭火;电器设备引起的火灾,不可用泡沫灭火器灭火 |
| D.在4mL0.1mol∙L-1的K2Cr2O7溶液中滴加数滴1mol/L的NaOH溶液,溶液颜色从橙色变成黄色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在容积恒为1 L的密闭容器中通入一定量N2O4,发生反应 △H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
△H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
 △H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
△H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是| t/s | 0 | 20 | 40 | 60 | 80 |
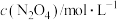 | 0.100 | 0.062 | 0.048 | 0.040 | 0.040 |
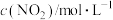 | 0 | 0.076 | 0.104 | 0.120 | 0.120 |
A.0~40 s,N2O4的平均反应速率为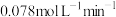 |
| B.80 s时,再充入N2O4、NO2各0.12 mol,平衡移动 |
| C.升高温度,反应的化学平衡常数值增大 |
| D.若压缩容器,达新平衡后,混合气颜色比原平衡时深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在一定条件下发生反应 2SO3(g) 2SO2(g)+O2(g),将2 mol SO3通入2 L容积恒定的密闭容器中,若维持容器内温度不变,5 min末测得SO3的物质的量为0.8 mol。则下列说法正确的是
2SO2(g)+O2(g),将2 mol SO3通入2 L容积恒定的密闭容器中,若维持容器内温度不变,5 min末测得SO3的物质的量为0.8 mol。则下列说法正确的是
 2SO2(g)+O2(g),将2 mol SO3通入2 L容积恒定的密闭容器中,若维持容器内温度不变,5 min末测得SO3的物质的量为0.8 mol。则下列说法正确的是
2SO2(g)+O2(g),将2 mol SO3通入2 L容积恒定的密闭容器中,若维持容器内温度不变,5 min末测得SO3的物质的量为0.8 mol。则下列说法正确的是| A.若某时刻消耗了1 molSO3同时生成了0.5molO2,则表明该反应达到了平衡状态 |
| B.若起始时充入3 mol SO3,起始时SO3分解速率不变 |
| C.0~5min,SO2的生成速率v(SO2)=0.12mol·L-1·min-1 |
| D.达到平衡时,SO2和SO3的浓度相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
A.25 ℃时,pH=7的NH4Cl与NH3·H2O混合溶液:c(H+)=c(OH-)=c( )=c(Cl-) )=c(Cl-) |
| B.25 ℃时,向10 mL pH=12的NaOH溶液中滴加等体积pH=2的CH3COOH溶液: c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C.0.1 mol·L-1的CH3COONa溶液与0.1 mol·L-1的CaCl2溶液等体积混合:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) |
D.浓度均为0.1 mol·L-1的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2溶液中,c( )的大小顺序为③>②>① )的大小顺序为③>②>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据实验操作和现象,下列相应实验结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 取  溶液于试管中,滴加过量氯水,溶液变橙色,再加入 溶液于试管中,滴加过量氯水,溶液变橙色,再加入 淀粉 淀粉 溶液,溶液变蓝色 溶液,溶液变蓝色 | 非金属性: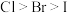 |
| B | 常温下,将铁片浸入足量浓硫酸中,铁片不溶解 | 常温下,铁与浓硫酸不反应 |
| C | 同温度下,分别测浓度均为 的 的 和 和 溶液的 溶液的 ,后者大于前者 ,后者大于前者 | 酸性: |
| D | 将溴乙烷与氢氧化钠的乙醇溶液混合加热后的气体产物通入溴的 溶液,溶液褪色 溶液,溶液褪色 | 溴乙烷发生了消去反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列推测不合理 的是
A.三氟乙酸 的酸性强于乙酸,所以三氟化氮 的酸性强于乙酸,所以三氟化氮 的碱性强于氨气 的碱性强于氨气 |
B.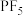 和 和 均为三角双锥结构的分子晶体,所以两者的沸点: 均为三角双锥结构的分子晶体,所以两者的沸点: |
C. 与 与 反应生成 反应生成 和 和 ,所以 ,所以 与 与 反应生成 反应生成 和 和 |
D.在相同条件下,水解能力 ,所以 ,所以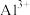 比 比 的水解能力更强 的水解能力更强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,取pH=2 的两种二元酸H2A与H2B各1mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述正确的是


| A.H2A为二元弱酸 |
| B.稀释前c(H2B)>c(H2A)=0.01mol /L |
| C.pH=3的NaHA水溶液中,离子浓度大小为c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-) |
| D.Na2B的水溶液中,离子浓度大小为c(Na+)>c(B2-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】丙炔酸( )是一元弱酸(简写成HR),一定条件下可以发生如图所示的转化。
)是一元弱酸(简写成HR),一定条件下可以发生如图所示的转化。
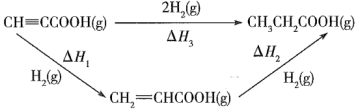
下列叙述错误的是
 )是一元弱酸(简写成HR),一定条件下可以发生如图所示的转化。
)是一元弱酸(简写成HR),一定条件下可以发生如图所示的转化。
下列叙述错误的是
A. |
B.将丙烯酸溶液加水稀释,促进丙烯酸电离,但 减小 减小 |
C.向HR溶液中滴加氨水至中性,此时溶液中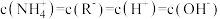 |
D.电解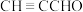 酸性溶液制HR,阳极反应为 酸性溶液制HR,阳极反应为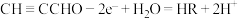 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】25℃时,用浓度为 的
的 溶液滴定
溶液滴定 浓度为
浓度为 的
的 溶液,滴定曲线如图所示。下列说法
溶液,滴定曲线如图所示。下列说法错误 的是。

 的
的 溶液滴定
溶液滴定 浓度为
浓度为 的
的 溶液,滴定曲线如图所示。下列说法
溶液,滴定曲线如图所示。下列说法
| A.应选用酚酞作指示剂 |
B. 点溶液中存在: 点溶液中存在: |
C.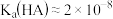 |
D.N点溶液中存在: |
您最近一年使用:0次



