1 . 下列实验能达到实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 将CuCl2•2H2O晶体置于坩埚中加热 | 制备CuCl2固体 |
| B | 加热氯化铵和氢氧化钙的混合物,并将产生的气体通过装有碱石灰的干燥管 | 制取氨气并干燥 |
| C | 向FeCl2溶液中滴加酸性高锰酸钾溶液 | 证明Fe2+具有还原性 |
| D | 向装有亚硫酸钠白色固体粉末的圆底烧瓶中加入浓硫酸,用排饱和亚硫酸钠溶液的方法收集气体 | 制取并收集二氧化硫 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 室温下,将 投入饱和 投入饱和 溶液中充分反应,沉淀由白色变为浅黄色 溶液中充分反应,沉淀由白色变为浅黄色 | 验证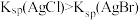 |
| B | 向含有酚酞的 溶液中滴加 溶液中滴加 溶液 溶液 | 根据溶液颜色变化,证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| C | 溶液中存在如下平衡: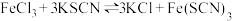 再加入少量氯化钾固体 再加入少量氯化钾固体 | 根据溶液颜色变化,验证勒夏特列原理 |
| D | 室温下,用 试纸分别测定浓度均为 试纸分别测定浓度均为 的 的 溶液和 溶液和 溶液的 溶液的 | 比较 和 和 的酸性强弱 的酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列实验能达到预期目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 等pH等体积HB和HA分别与NaOH溶液反应,HB消耗的NaOH溶液体积多 | 证明HA是强酸 |
| B | 向1 mL 0.2 mol·L-1 NaOH溶液中滴入2滴0.1 mol·L-1的MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol·L-1的FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下,溶度积常数:Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| C | 将SO2通入酸性KMnO4溶液中,紫红色褪去 | 证明SO2具有漂白性 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色会变浅 | 证明Na2CO3溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-08更新
|
194次组卷
|
5卷引用:吉林省辽源市东丰县五校2021-2022学年高二上学期期末考试化学试题
名校
4 . 回答下列问题:
(1)已知,常温下几种物质的电离常数如下:H2CO3:Ka1=4.5×10-7 Ka2=4.7×10-11;HClO:Ka=3.0×10-8。少量二氧化碳通入到次氯酸钠中的化学方程式_______
(2)25℃时,H2SO3的电离常数Ka1=1.0×10-2,Ka2=1.0×10-7。则该温度下 的水解常数
的水解常数
_______ ;若向 溶液中加入少量的
溶液中加入少量的 ,则溶液中
,则溶液中 将
将_______ (填“增大”“减小”或“不变”)。
(3)能证明 溶液中存在
溶液中存在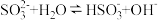 水解平衡的事实是
水解平衡的事实是_______ (填序号)。
A.滴入酚酞溶液变红,再加 溶液红色褪去
溶液红色褪去
B.滴入酚酞溶液变红,再加氯水后红色褪去
C.滴入酚酞溶液变红,再加 溶液后产生沉淀且红色褪去
溶液后产生沉淀且红色褪去
(4)已知室温下: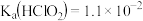 ,
, 。25℃时,浓度均为
。25℃时,浓度均为 的
的 溶液和
溶液和 溶液,两溶液中
溶液,两溶液中
_______ (填“>”“<”或“=”)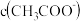 。若要使两溶液的pH相等,应
。若要使两溶液的pH相等,应_______ (填序号)。
a.向 溶液中加适量水
溶液中加适量水
b.向 溶液中加适量NaOH固体
溶液中加适量NaOH固体
c.向 溶液中加
溶液中加 固体
固体
d.向 溶液中加适量的水
溶液中加适量的水
(5)在空气中直接加热 晶体得不到纯净的无水
晶体得不到纯净的无水 ,原因是
,原因是_______ (用化学方程式表示)。由 晶体得到纯净的无水
晶体得到纯净的无水 的合理方法是
的合理方法是_______ 。
(1)已知,常温下几种物质的电离常数如下:H2CO3:Ka1=4.5×10-7 Ka2=4.7×10-11;HClO:Ka=3.0×10-8。少量二氧化碳通入到次氯酸钠中的化学方程式
(2)25℃时,H2SO3的电离常数Ka1=1.0×10-2,Ka2=1.0×10-7。则该温度下
 的水解常数
的水解常数
 溶液中加入少量的
溶液中加入少量的 ,则溶液中
,则溶液中 将
将(3)能证明
 溶液中存在
溶液中存在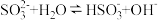 水解平衡的事实是
水解平衡的事实是A.滴入酚酞溶液变红,再加
 溶液红色褪去
溶液红色褪去B.滴入酚酞溶液变红,再加氯水后红色褪去
C.滴入酚酞溶液变红,再加
 溶液后产生沉淀且红色褪去
溶液后产生沉淀且红色褪去(4)已知室温下:
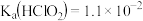 ,
, 。25℃时,浓度均为
。25℃时,浓度均为 的
的 溶液和
溶液和 溶液,两溶液中
溶液,两溶液中
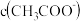 。若要使两溶液的pH相等,应
。若要使两溶液的pH相等,应a.向
 溶液中加适量水
溶液中加适量水b.向
 溶液中加适量NaOH固体
溶液中加适量NaOH固体c.向
 溶液中加
溶液中加 固体
固体d.向
 溶液中加适量的水
溶液中加适量的水(5)在空气中直接加热
 晶体得不到纯净的无水
晶体得不到纯净的无水 ,原因是
,原因是 晶体得到纯净的无水
晶体得到纯净的无水 的合理方法是
的合理方法是
您最近一年使用:0次
名校
5 . 常温下,下列叙述不正确的是
| A.pH=5的硫酸溶液稀释到原来的500倍,稀释后c(SO42-)与c(H+)之比约为1:10 |
| B.Na2CO3、NaHCO3两种盐溶液中,离子种类相同 |
| C.CH3COONa溶液中滴加少量浓盐酸后c(CH3COO-)增大 |
| D.滴入酚酞,NaNO2溶液显红色,证明HNO2是弱电解质 |
您最近一年使用:0次
2017-12-15更新
|
211次组卷
|
2卷引用:吉林省延边第二中学2017-2018学年高二上学期第二次月考化学试题
6 . 298K时,在H3PO4溶液中滴入NaOH溶液,含磷元素的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。下列说法不正确的是
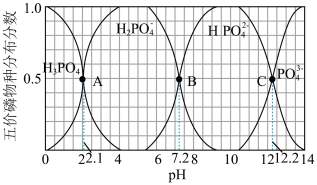

| A.Ka2(H3PO4)的数量级为10-8 |
| B.等物质的量NaH2PO4和Na2HPO4溶于水,其pH大于7.2 |
| C.向Na2HPO4溶液中加入足量的CaCl2溶液,溶液碱性减弱 |
| D.可依次选用甲基橙、酚酞作指示剂,标定反应终点 |
您最近一年使用:0次
名校
7 . 人体血液存在 (
( )与
)与 的缓冲体系,能有效除掉人体正常代谢时产生的少量酸、碱,保持pH的稳定,有关说法不正确的是
的缓冲体系,能有效除掉人体正常代谢时产生的少量酸、碱,保持pH的稳定,有关说法不正确的是
 (
( )与
)与 的缓冲体系,能有效除掉人体正常代谢时产生的少量酸、碱,保持pH的稳定,有关说法不正确的是
的缓冲体系,能有效除掉人体正常代谢时产生的少量酸、碱,保持pH的稳定,有关说法不正确的是A.代谢产生的 被 被 结合形成 结合形成 |
B.代谢产生的碱被 中和, 中和, 又由 又由 电离补充 电离补充 |
| C.血液中的缓冲体系可抵抗大量酸、碱的影响 |
D.人体出现酸中毒时可注射少量 溶液缓解 溶液缓解 |
您最近一年使用:0次
名校
解题方法
8 . 向某草酸溶液中滴加KOH溶液,溶液中 、
、 、
、 的物质的量浓度分数δ(X)[
的物质的量浓度分数δ(X)[ ]与pH的关系如图所示:
]与pH的关系如图所示:
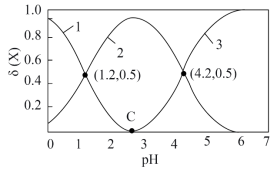
请回答下列问题:
(1)室温下,草酸的一级电离常数 为
为_______ ;
(2)①向草酸溶液中滴加KOH溶液至 的过程中主要反应的离子方程式为
的过程中主要反应的离子方程式为_______ 。
②0.1 moL
 溶液中,
溶液中,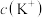
_______ 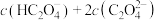 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
(3)室温下,通过下列实验探究0.0100 mol⋅L
 溶液的性质:
溶液的性质:
实验1:实验测得0.0100 mol⋅L
 溶液的pH为8.6。
溶液的pH为8.6。
实验2:向溶液中滴加等体积、0.0100 mol⋅L HCl溶液。pH由8.6降为4.8。
HCl溶液。pH由8.6降为4.8。
实验3:向溶液中加入等体积0.0200 mol⋅L
 溶液,出现白色沉淀。
溶液,出现白色沉淀。
实验4:向稀硫酸酸化的 ,溶液中滴加
,溶液中滴加 溶液至溶液褪色。
溶液至溶液褪色。
已知室温下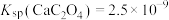 ,下列说法错误的是_______;
,下列说法错误的是_______;
(4)工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为: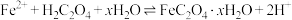 。
。
①制备时需添加氨水以提高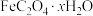 的产率,从化学平衡移动角度解释原因
的产率,从化学平衡移动角度解释原因_______ :
②测定草酸亚铁晶体(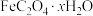 )的x值,实验如下:
)的x值,实验如下:
称取0.5400 g草酸亚铁晶体溶于一定浓度的硫酸中,用酸性 溶液漓定。到达滴定终点时,消耗0.1000 mol·L
溶液漓定。到达滴定终点时,消耗0.1000 mol·L 的酸性
的酸性 溶液18.00 mL。
溶液18.00 mL。
则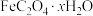 中
中
_______ ( 的摩尔质量是144 g⋅mol
的摩尔质量是144 g⋅mol )。
)。
 、
、 、
、 的物质的量浓度分数δ(X)[
的物质的量浓度分数δ(X)[ ]与pH的关系如图所示:
]与pH的关系如图所示:
请回答下列问题:
(1)室温下,草酸的一级电离常数
 为
为(2)①向草酸溶液中滴加KOH溶液至
 的过程中主要反应的离子方程式为
的过程中主要反应的离子方程式为②0.1 moL

 溶液中,
溶液中,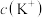
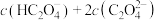 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);(3)室温下,通过下列实验探究0.0100 mol⋅L

 溶液的性质:
溶液的性质:实验1:实验测得0.0100 mol⋅L

 溶液的pH为8.6。
溶液的pH为8.6。实验2:向溶液中滴加等体积、0.0100 mol⋅L
 HCl溶液。pH由8.6降为4.8。
HCl溶液。pH由8.6降为4.8。实验3:向溶液中加入等体积0.0200 mol⋅L

 溶液,出现白色沉淀。
溶液,出现白色沉淀。实验4:向稀硫酸酸化的
 ,溶液中滴加
,溶液中滴加 溶液至溶液褪色。
溶液至溶液褪色。已知室温下
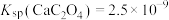 ,下列说法错误的是_______;
,下列说法错误的是_______;A.0.0100 mol⋅L  溶液中满足: 溶液中满足: |
B.实验2滴加盐酸过程中不可能存在: |
C.实验3所得上层清液中: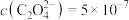 mol⋅L mol⋅L |
D.实验4发生反应的离子方程式为 |
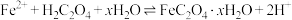 。
。①制备时需添加氨水以提高
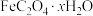 的产率,从化学平衡移动角度解释原因
的产率,从化学平衡移动角度解释原因②测定草酸亚铁晶体(
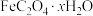 )的x值,实验如下:
)的x值,实验如下:称取0.5400 g草酸亚铁晶体溶于一定浓度的硫酸中,用酸性
 溶液漓定。到达滴定终点时,消耗0.1000 mol·L
溶液漓定。到达滴定终点时,消耗0.1000 mol·L 的酸性
的酸性 溶液18.00 mL。
溶液18.00 mL。则
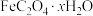 中
中
 的摩尔质量是144 g⋅mol
的摩尔质量是144 g⋅mol )。
)。
您最近一年使用:0次
名校
解题方法
9 . 下列有关盐类水解的说法正确的是
A. 和 和 在溶液中因为互相促进水解而不能大量共存 在溶液中因为互相促进水解而不能大量共存 |
B.0.1mol/L的 溶液中, 溶液中,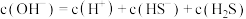 |
C.向盐酸中加入MgO固体,当溶液呈中性时, |
D.向AgCl悬浊液中加少量水,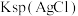 不变, 不变, 减小 减小 |
您最近一年使用:0次
名校
10 .  代表阿伏加德罗常数的值。下列相关说法正确的是
代表阿伏加德罗常数的值。下列相关说法正确的是
 代表阿伏加德罗常数的值。下列相关说法正确的是
代表阿伏加德罗常数的值。下列相关说法正确的是A.常温常压下,46g的 和 和 混合气体含有的原子数为 混合气体含有的原子数为 |
B.1L 溶液中阳离子的数目等于 溶液中阳离子的数目等于 |
C.标准状况下,11.2L 含有的非极性共价键数目为 含有的非极性共价键数目为 |
D.常温下,将0.1mol 溶于水中,充分反应后转移电子数目 溶于水中,充分反应后转移电子数目 |
您最近一年使用:0次



