名校
1 . 25℃时,0.1 mol•L-1溶液的pH如下表,下列有关说法正确的是
| 序号 | ① | ② | ③ | ④ |
| 溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
| pH | 7.0 | 7.0 | 8.1 | 8.4 |
| A.酸性强弱:HF<H2CO3 |
| B.①和②中溶质均未水解 |
| C.由水电离产生的c(H+):①>② |
| D.④溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)= c(Na+) |
您最近一年使用:0次
名校
2 . 下列关于0.10 mol·L-1的NH4Cl溶液的叙述不正确的是
| A.c(OH-) <c(H+) | B.c(Cl-)>c (NH4+) |
| C.c(NH4+)+c(Cl-)=0.10 mol·L-1 | D.c(NH4+)+c(NH3·H2O)=0.10 mol·L-1 |
您最近一年使用:0次
名校
3 . 室温下,0.1mol·L-1下列溶液的pH最大的是
| A.Na2CO3 | B.NaOH | C.NH4Cl | D.Na2SO4 |
您最近一年使用:0次
名校
4 . 根据下列化合物:①Na2CO3;②NaHC03;③ HCl;④NH4Cl;⑤ CH3COONa;⑥CH3COOH;⑦NH3·H2O。回答下列问题
(l)常温下,将0.1mol/LHCl和0.1mol/L NH3·H2O等体积混合后溶液的pH____ 7(填“<”“>”或“=”)。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=_____ ;在pH=3的CH3COOH溶液中,水电离出来的c(H+)与酸电离出的c(H+)之比等于_______ 。
(3)已知纯水中存在如下平衡:H2O+H2O====H3O++OH- △H>0 ,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是__ (填序号)。
A.向水中加入NaHSO4固体
B.向水中加入(NH4)2SO4固体
C.加热至100℃ [其中c(H+)=1×10-6mol/L]
D.向水中加入Na2CO3固体
(4)将①和②等浓度、等体积混合后溶液中各离子浓度由大到小的顺序为_________ 。
Ⅱ.(l)用惰性电极电解80℃无隔膜热的氯化钠水溶液,电解后最终得到NaClO3溶液,写出该电解池中发生的总反应方程式:_____________ ;当温度低于80℃时,会有部分NaClO生成,若NaCl、NaClO、NaClO3的混合物中氯元素的质量分数为50%,则混合物中氧元素的质量分数为__________ 。
(2)写出电解NaClO3生成NaClO4时的阳极反应式:___________ 。
(l)常温下,将0.1mol/LHCl和0.1mol/L NH3·H2O等体积混合后溶液的pH
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=
(3)已知纯水中存在如下平衡:H2O+H2O====H3O++OH- △H>0 ,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是
A.向水中加入NaHSO4固体
B.向水中加入(NH4)2SO4固体
C.加热至100℃ [其中c(H+)=1×10-6mol/L]
D.向水中加入Na2CO3固体
(4)将①和②等浓度、等体积混合后溶液中各离子浓度由大到小的顺序为
Ⅱ.(l)用惰性电极电解80℃无隔膜热的氯化钠水溶液,电解后最终得到NaClO3溶液,写出该电解池中发生的总反应方程式:
(2)写出电解NaClO3生成NaClO4时的阳极反应式:
您最近一年使用:0次
名校
解题方法
5 . 工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。并能以它们为原料生产一系列化工产品。为提高原料的利用率,节能降耗。设计如图所示工艺流程,其中氯碱工业装置中的电极未标出。

(1)电解饱和食盐水的化学方程式为___________________ 。
(2)为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是_______ (填序号)。
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
A.①④①②⑤③B.①②⑤④①③ C.①②④⑤③D.④②⑤
(3)图中NaOH溶液的质量分数a%、b%、c%,由大到小的顺序为_________ 。
(4)氯碱工业的产物NaOH与不同物质反应可以生成不同的盐。已知常温下,浓度均为0.1 mol/L的四种钠盐溶液pH如下表,下列说法不正确的是_______ (填序号)。
A.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是HClO
D.四种盐的阴离子结合H+能力最强的是HCO3-
(5)若利用电解氯化钠溶液所得的气体制36.5%的浓盐酸100t,最少需要消耗食盐_________ t。
(6)氯碱工业产品Cl2可用于冶炼钛铁矿得到金属钛,流程如图。写出钛铁矿经氯化法得到四氯化钛的化学方程式:____________________ 。
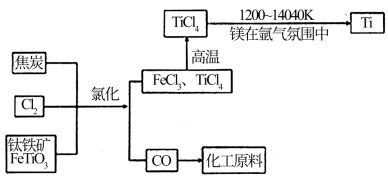
(7)氮气和氩气是两种化学性质相对稳定的气体。镁还原TiCl4的反应中为防止Mg和Ti被氧化选择稀有气体氩气。试用化学反应方程式解释不选用氮气的原因:__________________ 。

(1)电解饱和食盐水的化学方程式为
(2)为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
A.①④①②⑤③B.①②⑤④①③ C.①②④⑤③D.④②⑤
(3)图中NaOH溶液的质量分数a%、b%、c%,由大到小的顺序为
(4)氯碱工业的产物NaOH与不同物质反应可以生成不同的盐。已知常温下,浓度均为0.1 mol/L的四种钠盐溶液pH如下表,下列说法不正确的是
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
A.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是HClO
D.四种盐的阴离子结合H+能力最强的是HCO3-
(5)若利用电解氯化钠溶液所得的气体制36.5%的浓盐酸100t,最少需要消耗食盐
(6)氯碱工业产品Cl2可用于冶炼钛铁矿得到金属钛,流程如图。写出钛铁矿经氯化法得到四氯化钛的化学方程式:

(7)氮气和氩气是两种化学性质相对稳定的气体。镁还原TiCl4的反应中为防止Mg和Ti被氧化选择稀有气体氩气。试用化学反应方程式解释不选用氮气的原因:
您最近一年使用:0次
2017-04-01更新
|
294次组卷
|
3卷引用:2017届贵州省贵阳市第一中学高三下学期第六次适应性考试理综化学试卷
2017届贵州省贵阳市第一中学高三下学期第六次适应性考试理综化学试卷(已下线)贵州省贵阳市第一中学2017届高三下学期第六次适应性考试理科综合化学试题安徽省定远重点中学2017-2018学年高二上学期期末考试化学试题
名校
解题方法
6 . 在常温下,下列五种溶液:
①0.1mol/LNH4Cl ②0.1mol/LNH4HSO4 ③0.1mol/LCH3COONH4
④0.1mol/LNH3·H2O和0.1mol/LNH4Cl的混合溶液 ⑤0.1mol/LNH3·H2O
请根据要求填写下列空白:
(1)溶液①是______ 性(填“酸”、“碱”或“中”),其原因是____________ (用离子方程式表示)
(2)比较溶液②、③这C(NH4+)的大小关系是___________ (填“>”、“<”或“=”)
(3)在溶液④中,__________ 离子的浓度为0.1mol/L;NH3·H2O和_________ 离子的物质的量浓度之和为0.2mol/L。
(4)室温下测得溶液③的PH=7,则说明CH3COO-的水解程度________ (填“>”、“<”或“=”), NH4+的水解程度,C(CH3COO-)__________ C(NH4+)(填“>”、“<”或“=”)。
①0.1mol/LNH4Cl ②0.1mol/LNH4HSO4 ③0.1mol/LCH3COONH4
④0.1mol/LNH3·H2O和0.1mol/LNH4Cl的混合溶液 ⑤0.1mol/LNH3·H2O
请根据要求填写下列空白:
(1)溶液①是
(2)比较溶液②、③这C(NH4+)的大小关系是
(3)在溶液④中,
(4)室温下测得溶液③的PH=7,则说明CH3COO-的水解程度
您最近一年使用:0次
7 . 已知三种一元弱酸的酸性强弱 :HX>HY>HZ,则相同pH的NaX、NaY、NaZ溶液,其物质的量浓度由大到小的顺序正确的是
| A.NaX、NaY、NaZ | B.NaZ、NaY、NaX |
| C.NaY、NaZ、NaX | D.NaX、NaZ、NaY |
您最近一年使用:0次
2017-01-19更新
|
372次组卷
|
3卷引用:2016-2017学年贵州省凯里一中高二上期末化学卷
2016-2017学年贵州省凯里一中高二上期末化学卷贵州省金沙中学2019年普通高中学生学业基础水平测试化学试题(已下线)3.3.2 影响盐类水解的因素(重点练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)
10-11高二下·贵州遵义·期末
8 . 已知0.1mol/L的二元酸H2A溶液的pH=4,则下列说法中不正确的是
| A.在Na2A和NaHA溶液中离子种类相同 |
| B.在溶质物质的量浓度相等的Na2A和NaHA溶液中,阴离子总数相等 |
| C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-) |
| D.在Na2A溶液中一定有:c(OH-)=c(H+)+c(HA-)+2c(H2A) |
您最近一年使用:0次
2016-12-09更新
|
188次组卷
|
4卷引用:2010-2011年贵州省遵义四中高二下学期期末考试
(已下线)2010-2011年贵州省遵义四中高二下学期期末考试2016届河北省邯郸一中高三下学期研七考试理综化学试卷湖北省黄冈市黄梅国际育才高级中学2019-2020学年高二上学期9月月考化学试题甘肃省白银市第十中学2019-2020学年高二下学期第一次月考化学试题
名校
9 . 广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果都是参与反应的物质和水分别解离成两部分,再重新组合新的物质。根据上述观点,下列说法不正确的是
| A.PCl3的水解产物是PH3和HCl |
| B.CuCl2的水解产物是Cu(OH)2和HCl |
| C.NaClO的水解产物是HClO和NaOH |
| D.CaO2的水解产物是Ca(OH)2和H2O2 |
您最近一年使用:0次
2016-12-09更新
|
147次组卷
|
3卷引用:2016届贵州省凯里一中高三下学期开学模拟理综化学试卷
名校
解题方法
10 . 在相同温度下等体积、等物质的量浓度的4种稀溶液:①Na2SO4 ②H2SO3 ③NaHSO3 ④Na2S,所含带电微粒的数目由多到少的顺序是
| A.①=④>③=② | B.①=④>③>② | C.①>④>③>② | D.④>①>③>② |
您最近一年使用:0次
2016-12-09更新
|
460次组卷
|
5卷引用:【全国百强校】贵州省铜仁市思南中学2018-2019学年高二上学期期末考试化学试题



