解题方法
1 . 甲胺( )是一种一元弱碱。常温下,向
)是一种一元弱碱。常温下,向 中加入等体积
中加入等体积 的
的 。下列说法中正确的是
。下列说法中正确的是
 )是一种一元弱碱。常温下,向
)是一种一元弱碱。常温下,向 中加入等体积
中加入等体积 的
的 。下列说法中正确的是
。下列说法中正确的是A. 在水溶液的电离方程式为: 在水溶液的电离方程式为: |
B.混合后溶液中 |
C. 的 的 溶液中,水电离出来的 溶液中,水电离出来的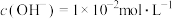 |
D.混合后的溶液中: |
您最近一年使用:0次
名校
解题方法
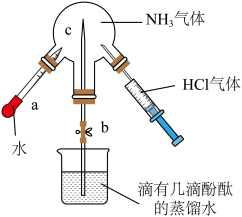
2 . 用如图装置分别进行两个实验:①先注入 ,再打开止水夹
,再打开止水夹 ;②先打开止水夹
;②先打开止水夹 ,再将
,再将 中水注入烧瓶。下列说法正确的是
中水注入烧瓶。下列说法正确的是
 ,再打开止水夹
,再打开止水夹 ;②先打开止水夹
;②先打开止水夹 ,再将
,再将 中水注入烧瓶。下列说法正确的是
中水注入烧瓶。下列说法正确的是
A.实验室可以加热 直接制取 直接制取 |
| B.实验②观察到烧瓶中产生红色的“喷泉” |
| C.实验①先产生白雾,然后观察到喷泉现象 |
D.实验①后烧瓶中一定存在 |
您最近一年使用:0次
2023-09-01更新
|
224次组卷
|
2卷引用:广东省佛山市南海区2024届高三摸底测试化学试题
名校
3 . 电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。常温下, 的电离常数
的电离常数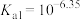 ,
,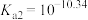 ,利用盐酸滴定某溶液中
,利用盐酸滴定某溶液中 的含量,其电位滴定曲线与pH曲线如图所示。下列说法正确的是
的含量,其电位滴定曲线与pH曲线如图所示。下列说法正确的是
 的电离常数
的电离常数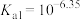 ,
,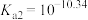 ,利用盐酸滴定某溶液中
,利用盐酸滴定某溶液中 的含量,其电位滴定曲线与pH曲线如图所示。下列说法正确的是
的含量,其电位滴定曲线与pH曲线如图所示。下列说法正确的是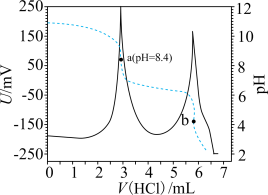
| A.该滴定过程需要加入酸碱指示剂 |
| B.水的电离程度:a<b |
C.a点溶液中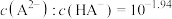 |
D.b点溶液中存在: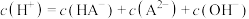 |
您最近一年使用:0次
2023-04-20更新
|
1067次组卷
|
3卷引用:广东省佛山市2023届普通高中教学质量检测(二)化学试题
解题方法
4 . 亚硝酸是一种弱酸,Ka(HNO2)=5.6×10-4,NaNO2可用于滴定分析。
(1)常温下,0.1 mol/L的NaNO2溶液呈__________ (填“酸性”、“中性”或“碱性”);原因是__________ (用离子方程式表示)。
(2)0.1 mol/LNaNO2溶液中部分微粒组分及浓度如图所示,X表示的是_______ (填写微粒化学式)。c(NO2-)+c(HNO2)=__________ mol/L。

(3)NaNO2用于测药物中对氨基苯磺酸(Ar-NH2)的含量。测定原理为:酸性环境中,NaNO2先转化为HNO2:HX + NaNO2 = HNO2 + NaX,HNO2再与Ar-NH2以物质的量比1:1发生反应。
①下列酸中,能作为HX来使用的是_______ 。
A.醋酸(Ka=1.8×10-5) B.盐酸 C.次氯酸(Ka=4.0×10-8)
②反应体系中,Ar-NH2和少量KI共存时,HNO2会先与Ar-NH2完全反应后,再氧化KI。滴定时用KI-淀粉糊剂作指示剂,滴定终点时淀粉糊剂显_______ 色。
③用该法测定含 Ar-NH2(Mr=173)药物样品的纯度,每次取0.400g样品,用0.100mol/L NaNO2标准溶液进行滴定,实验结果如下:
则该样品中对氨基苯磺酸的纯度是__________ 。
第二次实验数据出现异常,造成这种异常的原因可能是________ (填代号)。
a.锥形瓶洗净后未干燥
b.滴定终点时俯视读数
c.装标准溶液的滴定管未用标准溶液润洗
(4)已知298K时,H2CO3的Ka1=4.2×10-7、Ka2=5.61×10-11。将浓度均为0.1mol/L的Na2CO3及 HNO2溶液等体积混合,溶液中阴离子浓度由大到小的顺序为_______ 。
(1)常温下,0.1 mol/L的NaNO2溶液呈
(2)0.1 mol/LNaNO2溶液中部分微粒组分及浓度如图所示,X表示的是

(3)NaNO2用于测药物中对氨基苯磺酸(Ar-NH2)的含量。测定原理为:酸性环境中,NaNO2先转化为HNO2:HX + NaNO2 = HNO2 + NaX,HNO2再与Ar-NH2以物质的量比1:1发生反应。
①下列酸中,能作为HX来使用的是
A.醋酸(Ka=1.8×10-5) B.盐酸 C.次氯酸(Ka=4.0×10-8)
②反应体系中,Ar-NH2和少量KI共存时,HNO2会先与Ar-NH2完全反应后,再氧化KI。滴定时用KI-淀粉糊剂作指示剂,滴定终点时淀粉糊剂显
③用该法测定含 Ar-NH2(Mr=173)药物样品的纯度,每次取0.400g样品,用0.100mol/L NaNO2标准溶液进行滴定,实验结果如下:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗NaNO2溶液体积/mL | 20.12 | 20.90 | 20.00 | 19.88 |
第二次实验数据出现异常,造成这种异常的原因可能是
a.锥形瓶洗净后未干燥
b.滴定终点时俯视读数
c.装标准溶液的滴定管未用标准溶液润洗
(4)已知298K时,H2CO3的Ka1=4.2×10-7、Ka2=5.61×10-11。将浓度均为0.1mol/L的Na2CO3及 HNO2溶液等体积混合,溶液中阴离子浓度由大到小的顺序为
您最近一年使用:0次
名校
解题方法
5 . G是一种有机碱,溶于水成碱性的原理:G+H2O GH++OH-,室温下用0.1mol/L盐酸滴定10 mL0.1 mol/LG溶液,溶液pH的变化pH曲线如图所示。下列叙述正确的是
GH++OH-,室温下用0.1mol/L盐酸滴定10 mL0.1 mol/LG溶液,溶液pH的变化pH曲线如图所示。下列叙述正确的是
 GH++OH-,室温下用0.1mol/L盐酸滴定10 mL0.1 mol/LG溶液,溶液pH的变化pH曲线如图所示。下列叙述正确的是
GH++OH-,室温下用0.1mol/L盐酸滴定10 mL0.1 mol/LG溶液,溶液pH的变化pH曲线如图所示。下列叙述正确的是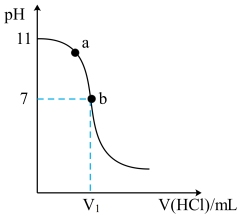
| A.G的近似电离常数是1×10-21 |
| B.V1>10 mL |
| C.水的电离程度:a<b |
| D.V(HCl)=20 mL 时,c(GH+)+c(G)=c(Cl-) |
您最近一年使用:0次
2022-11-27更新
|
204次组卷
|
2卷引用:广东省佛山市南海区2022-2023学年高二上学期学业水平测试化学试题
名校
解题方法
6 . 常温下,下列有关电解质溶液的说法错误的是
| A.相同浓度的HCOONa和NaF两溶液,前者的pH较大,则Ka(HCOOH)>Ka (HF) |
| B.相同浓度的HF和NaF两溶液等体积混合后pH<7,则溶液中c(F—)>c(Na+)>c(H+)>c(OH—) |
| C.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则Ksp(FeS)>Ksp(CuS) |
| D.在1mol·L-1Na2S溶液中,c(S2- )+c(HS—)+c(H2S)=1mol·L-1 |
您最近一年使用:0次
解题方法
7 . 常温下,用0.1mol·L-1的NaOH溶液滴定20mL0.1mol·L-1的H3PO2溶液,滴定过程中混合溶液的pH随加入的NaOH溶液体积变化关系如图所示,下列说法不正确的是
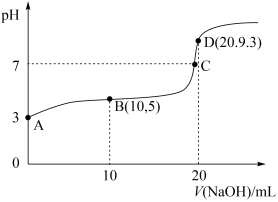

| A.常温下,Ka(H3PO2)的数量级为10—5 |
B.B点对应的溶液中:2[c(H+)—c(OH—)]=c(H2PO )—c(H3PO2) )—c(H3PO2) |
| C.H3PO2为一元弱酸 |
| D.滴定至V=20mL的过程中,溶液中由水电离出的c( H+)·(OH—)不变 |
您最近一年使用:0次
2022-05-02更新
|
548次组卷
|
6卷引用:广东省佛山市禅城区2022-2023学年高三统一调研测试(二) 化学试题
广东省佛山市禅城区2022-2023学年高三统一调研测试(二) 化学试题陕西省汉中市2022届高三教学质量第二次检测考试理科综合能力测试化学试题(已下线)专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)(已下线)专题10水溶液中的离子平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-2022年高考真题+模拟题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)
名校
8 . 葡萄酒中含有的酒石酸 常用作食品添加剂。已知
常用作食品添加剂。已知 溶液呈碱性,
溶液呈碱性, 溶液呈酸性。下列说法正确的是
溶液呈酸性。下列说法正确的是
 常用作食品添加剂。已知
常用作食品添加剂。已知 溶液呈碱性,
溶液呈碱性,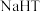 溶液呈酸性。下列说法正确的是
溶液呈酸性。下列说法正确的是A.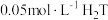 溶液的 溶液的 |
B.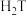 溶液的 溶液的 随温度升高而减小 随温度升高而减小 |
C.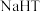 在水中的电离方程式为: 在水中的电离方程式为: |
D. 溶液中: 溶液中: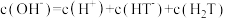 |
您最近一年使用:0次
2022-04-14更新
|
792次组卷
|
6卷引用:广东省佛山市普通高中2022届高三教学质量检测(二)化学试题
名校
解题方法
9 . 常温下,用0.1 mol/LNaOH溶液滴定20 mL等浓度的HA溶液的滴定曲线如图所示,下列说法正确的是


A.常温下,HA的电离平衡常数 |
B.b点溶液中: |
C.d点溶液中: |
| D.水的电离程度:d>c>e |
您最近一年使用:0次
2022-01-19更新
|
208次组卷
|
2卷引用:广东省佛山市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
10 . 0.1 mol/L NaOH溶液与盐酸酸化的0.02 mol/LFeCl3溶液滴定时t-pH曲线如图所示(已知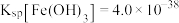 ,lg2=0.3)。下列说法正确的是
,lg2=0.3)。下列说法正确的是

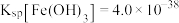 ,lg2=0.3)。下列说法正确的是
,lg2=0.3)。下列说法正确的是
| A.如图为FeCl3溶液滴定NaOH溶液的t-pH曲线 |
B.由曲线上a点pH,可计算室温下Fe3+的水解常数 |
| C.曲线上b点表示Fe3+恰好沉淀完全 |
D.c点存在关系: |
您最近一年使用:0次
2022-01-13更新
|
588次组卷
|
5卷引用:广东省佛山市2021-2022学年高三上学期普通高中第一次教学质量检测化学试卷
广东省佛山市2021-2022学年高三上学期普通高中第一次教学质量检测化学试卷(已下线)第19周 周测卷-备战2022年高考化学周测与晚练(新高考专用)(已下线)黄金卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)福建省龙岩第一中学2021-2022学年高二下学期开学考试(实验班)化学试题湖南省岳阳教研联盟2022-2023学年高二上学期期中联考化学试题



