名校
1 . 25℃,用浓度为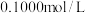 的
的 溶液滴定
溶液滴定 浓度为
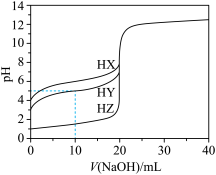
浓度为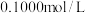 的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是
的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是
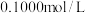 的
的 溶液滴定
溶液滴定 浓度为
浓度为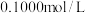 的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是
的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX |
B. 时,三种溶液中 时,三种溶液中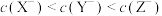 |
C.将上述HX、HY溶液等体积混合后用 溶液滴定至HX恰好完全反应时,溶液存在: 溶液滴定至HX恰好完全反应时,溶液存在: |
D.若进行HZ浓度测定,洗净碱式滴定管后直接取标准 溶液进行滴定,则测定结果偏低 溶液进行滴定,则测定结果偏低 |
您最近一年使用:0次
2024-02-29更新
|
153次组卷
|
2卷引用:吉林省梅河口市第五中学2023-2024学年高二下学期开学化学试题
名校
解题方法
2 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.25℃, 的 的 溶液中, 溶液中, 总数为 总数为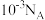 |
B.25℃,纯水中 总数为 总数为 |
C.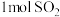 与 与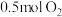 充分反应后,生成物的分子数为 充分反应后,生成物的分子数为 |
D.常温下,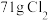 通入 通入 水中,转移电子数为 水中,转移电子数为 |
您最近一年使用:0次
2023-11-04更新
|
227次组卷
|
4卷引用:吉林省松原市前郭县第五高级中学2023~2024学年高二上学期期中考试化学试题
3 . 常温下,向 的
的 溶液中滴入NaOH溶液,随着pH变化溶液中浓度最大的含磷微粒如图所示。下列说法正确的是
溶液中滴入NaOH溶液,随着pH变化溶液中浓度最大的含磷微粒如图所示。下列说法正确的是

 的
的 溶液中滴入NaOH溶液,随着pH变化溶液中浓度最大的含磷微粒如图所示。下列说法正确的是
溶液中滴入NaOH溶液,随着pH变化溶液中浓度最大的含磷微粒如图所示。下列说法正确的是
A. 时, 时, |
B. 时, 时, |
C. 时, 时, |
D.若用 的 的 溶液进行实验, 溶液进行实验, 将向左移动 将向左移动 |
您最近一年使用:0次
2023-05-10更新
|
432次组卷
|
4卷引用:吉林省长春市东北师大附属中学2023-2024学年高二上学期 期末化学试卷
吉林省长春市东北师大附属中学2023-2024学年高二上学期 期末化学试卷福建省南平市2023届高中毕业班第三次质量检测化学试题(已下线)第14练 水溶液中粒子浓度的关系判断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)
4 . 亚硝酸( )是一种弱酸,常温条件下,其电离平衡常数为
)是一种弱酸,常温条件下,其电离平衡常数为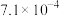 。下列说法不正确的是
。下列说法不正确的是
 )是一种弱酸,常温条件下,其电离平衡常数为
)是一种弱酸,常温条件下,其电离平衡常数为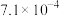 。下列说法不正确的是
。下列说法不正确的是A.0.1 mol·L  的水溶液中: 的水溶液中: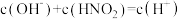 |
B.向0.1 mol·L  水溶液加少量水, 水溶液加少量水, 的值增大 的值增大 |
C.0.2 mol·L  溶液与0.1 mol·L 溶液与0.1 mol·L NaOH溶液等体积混合,溶液呈酸性 NaOH溶液等体积混合,溶液呈酸性 |
D.0.1 mol·L  溶液中离子浓度大小关系: 溶液中离子浓度大小关系: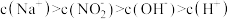 |
您最近一年使用:0次
2023-02-12更新
|
463次组卷
|
5卷引用:吉林省长春外国语学校2023-2024学年高二上学期11月期中考试化学试题
吉林省长春外国语学校2023-2024学年高二上学期11月期中考试化学试题广东省揭阳市普通高中2023届高三上学期期末教学质量测试化学试题(已下线)2022年福建省高考真题变式题(选择题1-5)(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题11-13)浙江省乐清市知临中学2022-2023学年高二下学期6月期末考试化学试题
名校
解题方法
5 . 醋酸(CH3COOH)是一种常见的弱酸。下列叙述正确的是
| A.pH=3的CH3COOH溶液中,c(H+)=c(CH3COO-) |
| B.pH=8的CH3COONa溶液中,c(CH3COO-)<c(Na+) |
| C.0.1mol·L-1CH3COONa溶液中,c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| D.0.1mol·L-1CH3COONa溶液中,c(Na+)=c(CH3COO-)+c(OH-) |
您最近一年使用:0次
2023-01-13更新
|
150次组卷
|
2卷引用:吉林省长春市第五中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
6 . 以0.1mol/L NaOH溶液滴定20.00mL 0.1mol/L 溶液的滴定曲线如图。已知:酚酞的变色范围是pH8.2~10
溶液的滴定曲线如图。已知:酚酞的变色范围是pH8.2~10不正确 的是
 溶液的滴定曲线如图。已知:酚酞的变色范围是pH8.2~10
溶液的滴定曲线如图。已知:酚酞的变色范围是pH8.2~10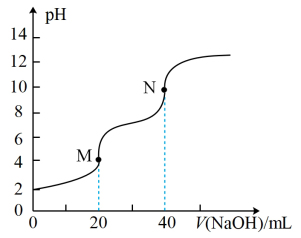
A.M点主要溶质为 |
| B.N点可用酚酞作指示剂指示滴定终点 |
C.N点溶液: |
D.M→N过程中,均满足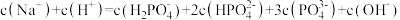 |
您最近一年使用:0次
2023-01-07更新
|
506次组卷
|
6卷引用:吉林省四平市第一高级中学2023-2024学年高二上学期第二次月考化学试卷
名校
解题方法
7 . 某二元酸 在水中的电离方程式为
在水中的电离方程式为 、
、 。下列有关说法中不正确的是
。下列有关说法中不正确的是
 在水中的电离方程式为
在水中的电离方程式为 、
、 。下列有关说法中不正确的是
。下列有关说法中不正确的是A.常温下 的 的 溶液的 溶液的 小于1 小于1 |
B. 溶液一定显酸性 溶液一定显酸性 |
C. 的 的 溶液中 溶液中 |
D. 溶液中存在 溶液中存在 |
您最近一年使用:0次
2023-02-14更新
|
152次组卷
|
2卷引用:吉林省白城市通榆县2022-2023学年高二上学期期末联合考试化学试题
名校
解题方法
8 . 已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,物质的量溶度相同的三种溶液①NaF溶液②NaClO溶液③Na2CO3溶液,其pH由大到小的顺序是_______ (填序号)。
(2)25℃时,pH=4的NH4Cl溶液中各离子浓度的大小关系为_______ 。
(3)NaClO溶液中的电荷守恒关系为_______ 。
(4)用离子方程式说明碳酸氢钠溶液呈碱性的原因_______ 。
(5)25℃下,将pH=12的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则V1:V2=
,则V1:V2=_______ 。
| 化学式 | HF | HClO | H2CO3 | NH3·H2O |
| 电离常数 | 6.8×10−4 | 4.7×10−8 | K1=4.3×10−7 K2=5.6×10−11 | Kb=1.7×10−5 |
(2)25℃时,pH=4的NH4Cl溶液中各离子浓度的大小关系为
(3)NaClO溶液中的电荷守恒关系为
(4)用离子方程式说明碳酸氢钠溶液呈碱性的原因
(5)25℃下,将pH=12的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
 ,则V1:V2=
,则V1:V2=
您最近一年使用:0次
2022-09-22更新
|
580次组卷
|
5卷引用:吉林省长春市北师大附属学校2021-2022学年高二上学期期末考试化学试题
名校
9 . 回答下列问题:
(1)已知 时,水的离子积常数
时,水的离子积常数 ,该温度下测得
,该温度下测得 溶液的
溶液的 。则
。则
_______ 25℃(填“>”、“<”或“=”)。 在水溶液中的电离方程式为
在水溶液中的电离方程式为_______ 。
(2)已知氢氟酸、次氯酸、碳酸在室温下的电离常数分别为:
根据上述数据,回答下列问题:
①比较同浓度的 、
、 溶液的
溶液的 值大小:
值大小:
_______  。
。
②少量的 通入
通入 溶液中,写出反应的离子方程式
溶液中,写出反应的离子方程式_______ 。
(3)用标准 溶液对测定白醋中醋酸的浓度,完全反应时所得溶液的
溶液对测定白醋中醋酸的浓度,完全反应时所得溶液的 大致为9。
大致为9。
①该实验应选用_______ 作指示剂:判断酸碱中和滴定反应到达滴定终点时的现象为_______ 。
②为减小实验误差,一共进行了三次实验,假设每次所取白醋体积均为 ,
, 标准液浓度为
标准液浓度为 ,三次实验结果记录如表:
,三次实验结果记录如表:
从上表可以看出,第一次实验中记录消耗 溶液的体积明显多于后两次,其原因可能是
溶液的体积明显多于后两次,其原因可能是_______ 。
A.实验结束时,俯视刻度线读取滴定终点时 溶液的体积
溶液的体积
B.滴定前碱式滴定管尖嘴有气泡,滴定结束尖嘴部分充满溶液
C.盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗
D.锥形瓶预先用食用白醋润洗过
E.滴加 溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定
溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)25℃时,有 的一组
的一组 、
、 混合溶液,溶液中
混合溶液,溶液中 和
和 与溶液
与溶液 的关系如图所示。下列说法错误的是_______。
的关系如图所示。下列说法错误的是_______。

(1)已知
 时,水的离子积常数
时,水的离子积常数 ,该温度下测得
,该温度下测得 溶液的
溶液的 。则
。则
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(2)已知氢氟酸、次氯酸、碳酸在室温下的电离常数分别为:
 | 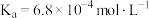 |
 |  |
 |   |
根据上述数据,回答下列问题:
①比较同浓度的
 、
、 溶液的
溶液的 值大小:
值大小:
 。
。②少量的
 通入
通入 溶液中,写出反应的离子方程式
溶液中,写出反应的离子方程式(3)用标准
 溶液对测定白醋中醋酸的浓度,完全反应时所得溶液的
溶液对测定白醋中醋酸的浓度,完全反应时所得溶液的 大致为9。
大致为9。①该实验应选用
②为减小实验误差,一共进行了三次实验,假设每次所取白醋体积均为
 ,
, 标准液浓度为
标准液浓度为 ,三次实验结果记录如表:
,三次实验结果记录如表:| 实验次数 | 第一次 | 第二次 | 第三次 |
消耗 溶液体积/ 溶液体积/ | 26.02 | 25.35 | 25.30 |
从上表可以看出,第一次实验中记录消耗
 溶液的体积明显多于后两次,其原因可能是
溶液的体积明显多于后两次,其原因可能是A.实验结束时,俯视刻度线读取滴定终点时
 溶液的体积
溶液的体积B.滴定前碱式滴定管尖嘴有气泡,滴定结束尖嘴部分充满溶液
C.盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗
D.锥形瓶预先用食用白醋润洗过
E.滴加
 溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定
溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定(4)25℃时,有
 的一组
的一组 、
、 混合溶液,溶液中
混合溶液,溶液中 和
和 与溶液
与溶液 的关系如图所示。下列说法错误的是_______。
的关系如图所示。下列说法错误的是_______。
A.曲线Ⅰ表示 |
B. 的数量级为 的数量级为 |
C. 时, 时,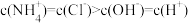 |
D. 时, 时, |
您最近一年使用:0次
2022-03-24更新
|
220次组卷
|
3卷引用:吉林省长春希望高中2021-2022学年高二上学期期末考试化学试题
名校
解题方法
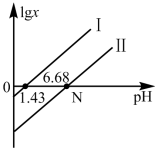
10 . 常温下,向 溶液中滴加
溶液中滴加 溶液至过量,最终生成
溶液至过量,最终生成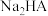 ,滴定曲线如图所示,其中
,滴定曲线如图所示,其中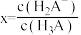 或
或 。下列说法正确的是
。下列说法正确的是
 溶液中滴加
溶液中滴加 溶液至过量,最终生成
溶液至过量,最终生成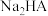 ,滴定曲线如图所示,其中
,滴定曲线如图所示,其中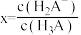 或
或 。下列说法正确的是
。下列说法正确的是
A.曲线Ⅱ对应的 |
B.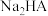 溶液有: 溶液有: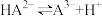 |
C.N点满足关系: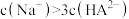 |
D.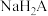 水溶液呈碱性 水溶液呈碱性 |
您最近一年使用:0次
2022-01-20更新
|
88次组卷
|
2卷引用:吉林省梅河口市第五中学等名校2021-2022学年高二上学期期末联考化学试题



