名校
解题方法
1 . 回答下列问题。
(1)向滴有酚酞的氨水中加入少量的氯化铵固体,观察到的现象是___________ ,用平衡原理解释原因___________ 。
(2)常温下,0.1 mol/L 的NaOH溶液的pH=___________ ,0.05mol/L的硫酸的pH=___________ ,取一定体积的两溶液混合,所得混合液的pH=2,则所取硫酸溶液的体积与NaOH溶液的体积比为___________ 。
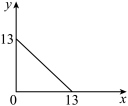
(3)某温度(t℃)下的溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示,此温度时,水的离子积常数Kw为___________ ,则该温度t___________ 25℃(填“>”“<”或“=”)。
(4)25℃时,pH=3的酸酸溶液和pH=11的NaOH溶液中由水电离出的c(H+)之比为___________ 。
(1)向滴有酚酞的氨水中加入少量的氯化铵固体,观察到的现象是
(2)常温下,0.1 mol/L 的NaOH溶液的pH=
(3)某温度(t℃)下的溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示,此温度时,水的离子积常数Kw为

(4)25℃时,pH=3的酸酸溶液和pH=11的NaOH溶液中由水电离出的c(H+)之比为
您最近一年使用:0次
名校
2 . 下列物质① 、 ②
、 ② 、③NaOH、④
、③NaOH、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 、⑧
、⑧ 、⑨Fe、⑩氯化钠溶液
、⑨Fe、⑩氯化钠溶液
(1)属于非电解质的是:___________ ;属于强电解质的是:___________ ;属于弱电解质的是:___________ ;既不是电解质也不是非电解质,常温下能导电的物质是___________ (均填序号)。
(2)写出①的电离方程式___________ 。
(3)向⑦的溶液中滴加几滴浓盐酸,平衡___________ 移动(填“正向”、“逆向”或“不移动”),平衡时溶液中
___________ (填“增大”、“减小”或者“不变”),
___________ (填“增大”、“减小”或者“不变”)。
(4)将 的①溶液和
的①溶液和 的③溶液等体积混合后溶液显酸性,原因是
的③溶液等体积混合后溶液显酸性,原因是___________ (结合有关离子方程式说明)。
(5)将标准状况下2.24L⑥缓慢通入 的③的溶液中,气体被充分吸收,离子浓度大小关系
的③的溶液中,气体被充分吸收,离子浓度大小关系___________ 。
(6)将足量⑥缓慢通入 的③的溶液中,所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
的③的溶液中,所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度___________ 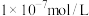 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH___________ (填“增大”、“减小”、或“不变”)。
 、 ②
、 ② 、③NaOH、④
、③NaOH、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 、⑧
、⑧ 、⑨Fe、⑩氯化钠溶液
、⑨Fe、⑩氯化钠溶液(1)属于非电解质的是:
(2)写出①的电离方程式
(3)向⑦的溶液中滴加几滴浓盐酸,平衡


(4)将
 的①溶液和
的①溶液和 的③溶液等体积混合后溶液显酸性,原因是
的③溶液等体积混合后溶液显酸性,原因是(5)将标准状况下2.24L⑥缓慢通入
 的③的溶液中,气体被充分吸收,离子浓度大小关系
的③的溶液中,气体被充分吸收,离子浓度大小关系(6)将足量⑥缓慢通入
 的③的溶液中,所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
的③的溶液中,所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度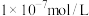 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH
您最近一年使用:0次
名校
3 .  溶液在稀释过程中,溶液中逐渐增大的量是
溶液在稀释过程中,溶液中逐渐增大的量是
① ②
② ③pH ④
③pH ④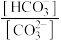
 溶液在稀释过程中,溶液中逐渐增大的量是
溶液在稀释过程中,溶液中逐渐增大的量是①
 ②
② ③pH ④
③pH ④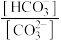
| A.①③ | B.①④ | C.②③ | D.②④ |
您最近一年使用:0次
2023-11-06更新
|
498次组卷
|
6卷引用:上海市上海中学2022-2023学年高二上学期期中考试化学试题
上海市上海中学2022-2023学年高二上学期期中考试化学试题【精品卷】3.3.2 影响盐类水解的主要因素课堂例题-人教版2023-2024学年选择性必修1(已下线)寒假作业06 盐类的水解-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)河北省高碑店市崇德实验中学2023-2024学年高二上学期期中考试化学试题 上海市新中高级中学2023-2024学年高二下学期阶段检测化学试题 陕西省兴平市南郊高级中学2023-2024学年高二上学期第三次化学质量检测题
4 . 下列说法不正确的是
| A.水分解变成氢气和氧气属于不自发反应 |
| B.用润湿的pH试纸测稀NaOH溶液的pH,测定值偏小 |
| C.NaHCO3溶液加水稀释,水解程度增大,电离程度减小 |
| D.将pH=3的醋酸溶液稀释1000倍得到pH<6醋酸溶液 |
您最近一年使用:0次
名校
解题方法
5 . 下列现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 等体积等浓度的MgCl2和NaOH溶液混合后,再滴加几滴FeCl3 | 先产生白色沉淀,后沉淀消失 | Fe3+水解出H+造成Mg(OH)2溶解 |
| B | 将通过灼热碎瓷片后的石蜡油蒸气通入到溴水中 | 溴水褪色 | 产物中一定含乙烯 |
| C | SO2分别通入石蕊、品红溶液 | 前者变红,后者褪色 | SO2漂白具有选择性 |
| D | 向5mL0.1mol/LK2Cr2O7溶液滴加5滴浓硫酸 | 溶液颜色由橙色变黄色 | 浓硫酸溶于水放热使平衡移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-09更新
|
540次组卷
|
4卷引用:四川省成都第七中学2022-2023学年高三上学期期中化学试题
名校
6 .  的化学性质与
的化学性质与 相似。用
相似。用 配制氯化亚锡溶液的操作为:加盐酸溶解→加水稀释→加4~5粒锡→移液保存。下列关于
配制氯化亚锡溶液的操作为:加盐酸溶解→加水稀释→加4~5粒锡→移液保存。下列关于 的相关实验叙述正确的是
的相关实验叙述正确的是

 的化学性质与
的化学性质与 相似。用
相似。用 配制氯化亚锡溶液的操作为:加盐酸溶解→加水稀释→加4~5粒锡→移液保存。下列关于
配制氯化亚锡溶液的操作为:加盐酸溶解→加水稀释→加4~5粒锡→移液保存。下列关于 的相关实验叙述正确的是
的相关实验叙述正确的是
| A.用A装置稀释浓盐酸 | B.用B装置加快 溶解 溶解 |
C.用C装置保存 溶液 溶液 | D.用D装置制备无水 |
您最近一年使用:0次
名校
7 . 无水 是一种重要的化工原料,其熔点306℃、沸点316℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。一般采用低共熔混合物反应法(熔融法)制备高纯度的三氯化铁,其模拟反应装置如下:
是一种重要的化工原料,其熔点306℃、沸点316℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。一般采用低共熔混合物反应法(熔融法)制备高纯度的三氯化铁,其模拟反应装置如下:
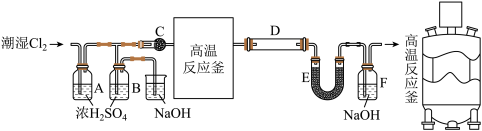
实验过程:在一个带有耐酸衬里的反应器中(即图中的高温反应釜),将70% 和30%KCl在600℃下共熔。再将铁屑溶解于共熔物中,再通入干燥氯气。反应生成的升华后导出,再经冷凝收集。
和30%KCl在600℃下共熔。再将铁屑溶解于共熔物中,再通入干燥氯气。反应生成的升华后导出,再经冷凝收集。
回答下列问题:
(1)C装置的名称为_______ ;
(2)当氯气通入时,A中有酸雾产生。为吸收酸雾,C中应盛放的物质为_______;(填字母)
(3)高温反应釜中发生反应的化学方程式为_______ ;
(4)E装置的作用为_______ ;
(5)为研究 的性质,某化学兴趣小组取一定质量的
的性质,某化学兴趣小组取一定质量的 (摩尔质量为
(摩尔质量为 )在惰性气体保护下受热分解时,所得固体产物的剩余质量分数(剩余质量与原样品质量的百分比)随温度变化的曲线如图所示。试利用图中信息并结合所学的知识,回答下列各问题:
)在惰性气体保护下受热分解时,所得固体产物的剩余质量分数(剩余质量与原样品质量的百分比)随温度变化的曲线如图所示。试利用图中信息并结合所学的知识,回答下列各问题:

已知:A为红褐色固体,B中含有三种元素,C为红棕色固体,D为黑色固体。
①固体产物的化学式B是_______ ,D是_______ ;
②由C得到D的化学方程式为_______ 。
 是一种重要的化工原料,其熔点306℃、沸点316℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。一般采用低共熔混合物反应法(熔融法)制备高纯度的三氯化铁,其模拟反应装置如下:
是一种重要的化工原料,其熔点306℃、沸点316℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。一般采用低共熔混合物反应法(熔融法)制备高纯度的三氯化铁,其模拟反应装置如下:
实验过程:在一个带有耐酸衬里的反应器中(即图中的高温反应釜),将70%
 和30%KCl在600℃下共熔。再将铁屑溶解于共熔物中,再通入干燥氯气。反应生成的升华后导出,再经冷凝收集。
和30%KCl在600℃下共熔。再将铁屑溶解于共熔物中,再通入干燥氯气。反应生成的升华后导出,再经冷凝收集。回答下列问题:
(1)C装置的名称为
(2)当氯气通入时,A中有酸雾产生。为吸收酸雾,C中应盛放的物质为_______;(填字母)
A. | B.CaO | C. | D.NaOH |
(4)E装置的作用为
(5)为研究
 的性质,某化学兴趣小组取一定质量的
的性质,某化学兴趣小组取一定质量的 (摩尔质量为
(摩尔质量为 )在惰性气体保护下受热分解时,所得固体产物的剩余质量分数(剩余质量与原样品质量的百分比)随温度变化的曲线如图所示。试利用图中信息并结合所学的知识,回答下列各问题:
)在惰性气体保护下受热分解时,所得固体产物的剩余质量分数(剩余质量与原样品质量的百分比)随温度变化的曲线如图所示。试利用图中信息并结合所学的知识,回答下列各问题:
已知:A为红褐色固体,B中含有三种元素,C为红棕色固体,D为黑色固体。
①固体产物的化学式B是
②由C得到D的化学方程式为
您最近一年使用:0次
2022-11-03更新
|
422次组卷
|
3卷引用:湖北省鄂东南联盟2022-2023学年高三上学期期中联考化学试题
名校
解题方法
8 . 氨基羧酸盐在工农业、生活中有着广泛应用,其中氨基甲酸铵(NH2COONH4)可用作肥料、洗涤剂等。实验室用下图所示装置制备氨基甲酸铵,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则主要生成碳酸氢铵。
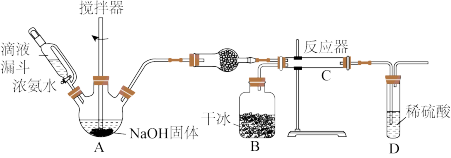
(1)盛放NaOH固体的仪器名称是_______ ,干燥管中的试剂为_______ 。
(2)无水条件下合成氨基甲酸铵的化学反应方程式为_______ ;若该反应能自发进行,则该反应的
_______ 0,(填“>”或“<”);对比碳酸钙和盐酸反应制取CO2,该实验利用干冰升华制取CO2,其优点有_______ 。
A.提供较低的反应温度,有利于过程的自发进行
B.所得氨基甲酸铵含杂质较少
C.更加绿色环保
D.对CO2的流速能更好的调控与掌握
(3)上述实验装置存在缺陷,改进的方法是_______ 。(写出其中任意1条)
(4)某小组拟在相同温度下,探究氨基甲酸铵浓度对氨基甲酸铵水解反应速率的影响。限选试剂与仪器:2.0mol/L NH2COONH4溶液、蒸馏水、烧杯、量筒、秒表、电导率仪、恒温水浴槽。设计实验方案:在不同氨基甲酸铵溶液浓度下,测定电导率数值的变化量相同所需的时间。参照下表格式,在表中的空白栏目填上需记录的待测物理量和所拟定的数据。(数据用字母表示,其中体积用V1、V2等表示)______
(5)该小组在上述实验方案基础上又进行了探究,分别用两份不同初始浓度的氨基甲酸铵溶液在不同温度下测定水解反应速率,得到c(NH2COO-)随时间的变化趋势如图所示。根据图中信息,能说明该水解反应速率随温度升高而加快的证据是_______ 。


(1)盛放NaOH固体的仪器名称是
(2)无水条件下合成氨基甲酸铵的化学反应方程式为

A.提供较低的反应温度,有利于过程的自发进行
B.所得氨基甲酸铵含杂质较少
C.更加绿色环保
D.对CO2的流速能更好的调控与掌握
(3)上述实验装置存在缺陷,改进的方法是
(4)某小组拟在相同温度下,探究氨基甲酸铵浓度对氨基甲酸铵水解反应速率的影响。限选试剂与仪器:2.0mol/L NH2COONH4溶液、蒸馏水、烧杯、量筒、秒表、电导率仪、恒温水浴槽。设计实验方案:在不同氨基甲酸铵溶液浓度下,测定电导率数值的变化量相同所需的时间。参照下表格式,在表中的空白栏目填上需记录的待测物理量和所拟定的数据。(数据用字母表示,其中体积用V1、V2等表示)
| 物理量 实验序号 | 温度T(℃) | 导电率变化量∆S | … | |||
| 1 | a | b | ||||
| 2 | a | b |

您最近一年使用:0次
2022-10-09更新
|
275次组卷
|
3卷引用:广东省六校2022-2023学年高三上学期第二次联考化学试题
9 . 请你设计实验探究促进或抑制 水解的条件,了解影响盐类水解程度的因素。
水解的条件,了解影响盐类水解程度的因素。
可供选择的仪器、用品和试剂:烧杯、试管、玻璃棒、胶头滴管、量筒、酒精灯、 计、
计、 试纸;1 mol∙L−1盐酸、氯化氢气体、1 mol∙L−1氢氧化钠溶液、1 mol∙L−1氯化铁溶液、蒸馏水。
试纸;1 mol∙L−1盐酸、氯化氢气体、1 mol∙L−1氢氧化钠溶液、1 mol∙L−1氯化铁溶液、蒸馏水。
完成下列探究过程:
(1)写出 水解的离子方程式:
水解的离子方程式:_______ 。
(2)针对影响 水解的因素提出假设:
水解的因素提出假设:
假设1:溶液的酸碱性;
假设2:_______ ;
假设3:_______ 。
(3)基于以上3个假设,设计出实验方案,将实验操作、预期现象和结论填在下表中。
 水解的条件,了解影响盐类水解程度的因素。
水解的条件,了解影响盐类水解程度的因素。可供选择的仪器、用品和试剂:烧杯、试管、玻璃棒、胶头滴管、量筒、酒精灯、
 计、
计、 试纸;1 mol∙L−1盐酸、氯化氢气体、1 mol∙L−1氢氧化钠溶液、1 mol∙L−1氯化铁溶液、蒸馏水。
试纸;1 mol∙L−1盐酸、氯化氢气体、1 mol∙L−1氢氧化钠溶液、1 mol∙L−1氯化铁溶液、蒸馏水。完成下列探究过程:
(1)写出
 水解的离子方程式:
水解的离子方程式:(2)针对影响
 水解的因素提出假设:
水解的因素提出假设:假设1:溶液的酸碱性;
假设2:
假设3:
(3)基于以上3个假设,设计出实验方案,将实验操作、预期现象和结论填在下表中。
| 步骤编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② | ||
| ③ |
您最近一年使用:0次
10 . 冰壶比赛称为“冰上的国际象棋”,制作冰壶用的标准砥石的化学成分为石英碱长正长岩,常见的组分有钾长石K[AlSi3O8]和钠长石Na[AlSi3O8]等。完成下列填空:
(1)上述所涉及的元素中,具有相同电子数的简单离子半径由大到小的顺序是_______ ,原子核外有两个未成对电子的元素有_______ 。
(2)用一个化学方程式比较钠和铝的金属性的强弱_______ ,并用原子结构知识的观点解释原因_______ 。
(3)我国科学家发展了一种在200℃熔盐体系中,采用金属Al还原二氧化硅或硅酸盐、钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能,配平下列方程式_______ 。
______Al+_______K[AlSi3O8]+_______AlCl3→_______Si+_______AlOCl+_______KAlO2;
上述反应中若产生14g硅,转移的电子数为_______ 。
(4)KAlO2溶液中,n(K+)_______ n(AlO )(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因
)(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因_______ 。
(1)上述所涉及的元素中,具有相同电子数的简单离子半径由大到小的顺序是
(2)用一个化学方程式比较钠和铝的金属性的强弱
(3)我国科学家发展了一种在200℃熔盐体系中,采用金属Al还原二氧化硅或硅酸盐、钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能,配平下列方程式
______Al+_______K[AlSi3O8]+_______AlCl3→_______Si+_______AlOCl+_______KAlO2;
上述反应中若产生14g硅,转移的电子数为
(4)KAlO2溶液中,n(K+)
 )(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因
)(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因
您最近一年使用:0次



