名校
解题方法
1 . 回答下列问题。
(1)向滴有酚酞的氨水中加入少量的氯化铵固体,观察到的现象是___________ ,用平衡原理解释原因___________ 。
(2)常温下,0.1 mol/L 的NaOH溶液的pH=___________ ,0.05mol/L的硫酸的pH=___________ ,取一定体积的两溶液混合,所得混合液的pH=2,则所取硫酸溶液的体积与NaOH溶液的体积比为___________ 。
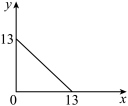
(3)某温度(t℃)下的溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示,此温度时,水的离子积常数Kw为___________ ,则该温度t___________ 25℃(填“>”“<”或“=”)。
(4)25℃时,pH=3的酸酸溶液和pH=11的NaOH溶液中由水电离出的c(H+)之比为___________ 。
(1)向滴有酚酞的氨水中加入少量的氯化铵固体,观察到的现象是
(2)常温下,0.1 mol/L 的NaOH溶液的pH=
(3)某温度(t℃)下的溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示,此温度时,水的离子积常数Kw为

(4)25℃时,pH=3的酸酸溶液和pH=11的NaOH溶液中由水电离出的c(H+)之比为
您最近一年使用:0次
名校
2 . 下列物质① 、 ②
、 ② 、③NaOH、④
、③NaOH、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 、⑧
、⑧ 、⑨Fe、⑩氯化钠溶液
、⑨Fe、⑩氯化钠溶液
(1)属于非电解质的是:___________ ;属于强电解质的是:___________ ;属于弱电解质的是:___________ ;既不是电解质也不是非电解质,常温下能导电的物质是___________ (均填序号)。
(2)写出①的电离方程式___________ 。
(3)向⑦的溶液中滴加几滴浓盐酸,平衡___________ 移动(填“正向”、“逆向”或“不移动”),平衡时溶液中
___________ (填“增大”、“减小”或者“不变”),
___________ (填“增大”、“减小”或者“不变”)。
(4)将 的①溶液和
的①溶液和 的③溶液等体积混合后溶液显酸性,原因是
的③溶液等体积混合后溶液显酸性,原因是___________ (结合有关离子方程式说明)。
(5)将标准状况下2.24L⑥缓慢通入 的③的溶液中,气体被充分吸收,离子浓度大小关系
的③的溶液中,气体被充分吸收,离子浓度大小关系___________ 。
(6)将足量⑥缓慢通入 的③的溶液中,所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
的③的溶液中,所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度___________ 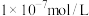 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH___________ (填“增大”、“减小”、或“不变”)。
 、 ②
、 ② 、③NaOH、④
、③NaOH、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 、⑧
、⑧ 、⑨Fe、⑩氯化钠溶液
、⑨Fe、⑩氯化钠溶液(1)属于非电解质的是:
(2)写出①的电离方程式
(3)向⑦的溶液中滴加几滴浓盐酸,平衡


(4)将
 的①溶液和
的①溶液和 的③溶液等体积混合后溶液显酸性,原因是
的③溶液等体积混合后溶液显酸性,原因是(5)将标准状况下2.24L⑥缓慢通入
 的③的溶液中,气体被充分吸收,离子浓度大小关系
的③的溶液中,气体被充分吸收,离子浓度大小关系(6)将足量⑥缓慢通入
 的③的溶液中,所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
的③的溶液中,所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度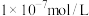 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH
您最近一年使用:0次
名校
3 .  溶液在稀释过程中,溶液中逐渐增大的量是
溶液在稀释过程中,溶液中逐渐增大的量是
① ②
② ③pH ④
③pH ④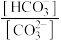
 溶液在稀释过程中,溶液中逐渐增大的量是
溶液在稀释过程中,溶液中逐渐增大的量是①
 ②
② ③pH ④
③pH ④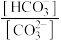
| A.①③ | B.①④ | C.②③ | D.②④ |
您最近一年使用:0次
2023-11-06更新
|
493次组卷
|
6卷引用:上海市上海中学2022-2023学年高二上学期期中考试化学试题
上海市上海中学2022-2023学年高二上学期期中考试化学试题课时2影响盐类水解的主要因素课堂例题(已下线)寒假作业06 盐类的水解-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)河北省高碑店市崇德实验中学2023-2024学年高二上学期期中考试化学试题 上海市新中高级中学2023-2024学年高二下学期阶段检测化学试题 陕西省兴平市南郊高级中学2023-2024学年高二上学期第三次化学质量检测题
4 . 常温下稀FeCl3溶液中:Fe3++3H2O⇌Fe(OH)3+3H+,下列操作能使c(Fe3+)增大的是
| A.加入少量的H2SO4溶液 | B.加水稀释 |
| C.加热 | D.加入少量NaOH溶液 |
您最近一年使用:0次
5 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 有白色沉淀生成,溶液红色变浅 | 证明纯碱溶液呈碱性是由 水解引起的 水解引起的 |
| B | 室温下,用pH试纸测定浓度均为0.1mol/L的NaClO溶液、CH3COONa溶液pH | NaClO溶液的pH较大 | 酸性:HClO<CH3COOH |
| C | 向1mL 0.1mol/LNaOH溶液中滴入2滴0.1mol/L MgCl2溶液,再滴入2滴0.1mol/L CuSO4溶液 | 沉淀颜色变化:白色—蓝色 | Ksp:Cu(OH)2<Mg(OH)2 |
| D | 分别向两支试管中加入同浓度、同体积的草酸溶液,再分别加入同体积、不同浓度的酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色时间不同 | 浓度不同反应速率不同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-16更新
|
359次组卷
|
2卷引用:福建省厦门第一中学2022-2023学年高三上学期12月月考化学试题
名校
解题方法
6 . 常温下,向20mL0.2mol·L-1H2A溶液中滴加0.2mol·L-1NaOH溶液。有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。根据图示判断,下列说法正确的是


| A.当V(NaOH溶液)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) |
| B.NaHA溶液中:c(OH-)+2c(A2-)=c(H+)+c(H2A) |
| C.当V(NaOH溶液)=40mL时,其溶液中水的电离程度比纯水大 |
| D.向Na2A溶液加入水的过程中,pH可能增大也可能减小 |
您最近一年使用:0次
名校
7 . 下列措施能使NaClO溶液的水解平衡正向移动,水解程度反而减小的是
| A.增大NaClO溶液浓度 | B.加水稀释 |
| C.升高温度 | D.加入适量NaOH固体 |
您最近一年使用:0次
2023-01-09更新
|
585次组卷
|
5卷引用:四川省成都市蓉城名校联盟2022-2023学年高二上学期期末联考化学试卷
8 . 下列说法不正确的是
| A.水分解变成氢气和氧气属于不自发反应 |
| B.用润湿的pH试纸测稀NaOH溶液的pH,测定值偏小 |
| C.NaHCO3溶液加水稀释,水解程度增大,电离程度减小 |
| D.将pH=3的醋酸溶液稀释1000倍得到pH<6醋酸溶液 |
您最近一年使用:0次
名校
9 . pH均为4的稀硫酸和硫酸铝溶液加水稀释时的pH变化曲线如图,下列说法正确的是


| A.Y曲线代表稀硫酸 |
B.a点和b点溶液中 :b<a :b<a |
C.b、c两点的溶液中水电离出的 相等 相等 |
D.a、c点对应的两溶液中,稀硫酸中 与硫酸铝溶液中 与硫酸铝溶液中 的比值比稀释前的比值大 的比值比稀释前的比值大 |
您最近一年使用:0次
名校
解题方法
10 . 粗硫酸铜中常含有难溶性杂质和少量 、
、 ,某小组用粗硫酸铜制取较纯净的胆矾晶体并用碘量法测定其纯度,请回答下列问题:
,某小组用粗硫酸铜制取较纯净的胆矾晶体并用碘量法测定其纯度,请回答下列问题:
Ⅰ.胆矾晶体( )的制备
)的制备
配制硫酸铜溶液:将一定质量的粗硫酸铜置于盛有稀硫酸的烧杯中,加热并不断搅拌使可溶性部分充分溶解,停止加热。
除杂:往溶液中加入过量3%的 溶液并加热,充分反应后再持续加热一段时间,冷却后调节溶液pH至3.5~4,过滤、洗涤,将滤液和洗涤液转移至蒸发皿中。
溶液并加热,充分反应后再持续加热一段时间,冷却后调节溶液pH至3.5~4,过滤、洗涤,将滤液和洗涤液转移至蒸发皿中。
结晶:用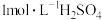 调节pH至1~2,然后经过一系列实验操作,最后经洗涤、干燥得到胆矾晶体。
调节pH至1~2,然后经过一系列实验操作,最后经洗涤、干燥得到胆矾晶体。
(1)结合上述操作,除所给仪器外,配制硫酸铜溶液的过程中还需要的玻璃仪器有_______ (填仪器名称)。
(2)除杂过程中,加入 反应的离子方程式
反应的离子方程式_______ ,是调节溶液pH至3.5~4的目的是_______ 。
(3)结晶过程中,调节pH的目的是_______ ,“一系列实验操作”步骤有_______ 。
Ⅱ.碘量法测定胆矾晶体的纯度:
称取胆矾晶体m g,加适量稀硫酸和水配成250mL溶液,每次取25.00mL,加入过量的KI溶液(杂质不参与反应),再加几滴淀粉溶液,用 溶液滴定至终点
溶液滴定至终点
(已知: ,
, )。
)。
(4)有关滴定管的正确操作顺序为(填字母):_______ 。
检漏→蒸馏水洗涤→→→→→→开始滴定。
A.装入滴定液至零刻度以上
B.调整滴定液液面至零刻度或零刻度以下
C.排除气泡
D.用滴定液润洗2~3次
E.记录起始读数
(5)滴定终点时的现象为_______ 。
(6)若平均消耗 溶液V mL,则所得样品中
溶液V mL,则所得样品中 的纯度为
的纯度为_______ ×100%(用含字母的表达式表示)。
 、
、 ,某小组用粗硫酸铜制取较纯净的胆矾晶体并用碘量法测定其纯度,请回答下列问题:
,某小组用粗硫酸铜制取较纯净的胆矾晶体并用碘量法测定其纯度,请回答下列问题:Ⅰ.胆矾晶体(
 )的制备
)的制备配制硫酸铜溶液:将一定质量的粗硫酸铜置于盛有稀硫酸的烧杯中,加热并不断搅拌使可溶性部分充分溶解,停止加热。
除杂:往溶液中加入过量3%的
 溶液并加热,充分反应后再持续加热一段时间,冷却后调节溶液pH至3.5~4,过滤、洗涤,将滤液和洗涤液转移至蒸发皿中。
溶液并加热,充分反应后再持续加热一段时间,冷却后调节溶液pH至3.5~4,过滤、洗涤,将滤液和洗涤液转移至蒸发皿中。结晶:用
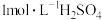 调节pH至1~2,然后经过一系列实验操作,最后经洗涤、干燥得到胆矾晶体。
调节pH至1~2,然后经过一系列实验操作,最后经洗涤、干燥得到胆矾晶体。(1)结合上述操作,除所给仪器外,配制硫酸铜溶液的过程中还需要的玻璃仪器有
(2)除杂过程中,加入
 反应的离子方程式
反应的离子方程式(3)结晶过程中,调节pH的目的是
Ⅱ.碘量法测定胆矾晶体的纯度:
称取胆矾晶体m g,加适量稀硫酸和水配成250mL溶液,每次取25.00mL,加入过量的KI溶液(杂质不参与反应),再加几滴淀粉溶液,用
 溶液滴定至终点
溶液滴定至终点(已知:
 ,
, )。
)。(4)有关滴定管的正确操作顺序为(填字母):
检漏→蒸馏水洗涤→→→→→→开始滴定。
A.装入滴定液至零刻度以上
B.调整滴定液液面至零刻度或零刻度以下
C.排除气泡
D.用滴定液润洗2~3次
E.记录起始读数
(5)滴定终点时的现象为
(6)若平均消耗
 溶液V mL,则所得样品中
溶液V mL,则所得样品中 的纯度为
的纯度为
您最近一年使用:0次



