名校
1 .  是食品加工中最为快捷的食品添加剂,用于焙烤食品;
是食品加工中最为快捷的食品添加剂,用于焙烤食品; 在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1) 可作净水剂,其理由是
可作净水剂,其理由是_______ (用必要的化学用语和相关文字说明)。
(2)相同条件下, 中
中
_______ (填“等于”“大于”或“小于”) 中
中 。
。
(3)如图所示是 电解质溶液的pH随温度变化的图像。
电解质溶液的pH随温度变化的图像。
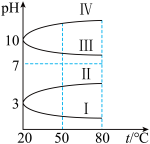
①其中符合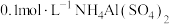 的pH随温度变化的曲线是
的pH随温度变化的曲线是_______ (填Ⅰ、Ⅱ、Ⅲ、Ⅳ),导致pH随温度变化的原因是_______ 。
②20℃时, 中
中
_______  。
。
(4)室温时,向 溶液中滴加
溶液中滴加 溶液,所得溶液pH与
溶液,所得溶液pH与 溶液体积的关系曲线如图所示。试分析图中a、b、c、d四个点,水的电离程度最大的是
溶液体积的关系曲线如图所示。试分析图中a、b、c、d四个点,水的电离程度最大的是_______ 点;在b点,溶液中各离子浓度由大到小的排列顺序是_______ 。

 是食品加工中最为快捷的食品添加剂,用于焙烤食品;
是食品加工中最为快捷的食品添加剂,用于焙烤食品; 在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
在分析试剂、医药、电子工业中用途广泛。请回答下列问题:(1)
 可作净水剂,其理由是
可作净水剂,其理由是(2)相同条件下,
 中
中
 中
中 。
。(3)如图所示是
 电解质溶液的pH随温度变化的图像。
电解质溶液的pH随温度变化的图像。
①其中符合
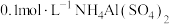 的pH随温度变化的曲线是
的pH随温度变化的曲线是②20℃时,
 中
中
 。
。(4)室温时,向
 溶液中滴加
溶液中滴加 溶液,所得溶液pH与
溶液,所得溶液pH与 溶液体积的关系曲线如图所示。试分析图中a、b、c、d四个点,水的电离程度最大的是
溶液体积的关系曲线如图所示。试分析图中a、b、c、d四个点,水的电离程度最大的是
您最近一年使用:0次
2023-10-28更新
|
478次组卷
|
3卷引用:吉林省长春市东北师范大学附属中学2023-2024学年高二上学期10月期中化学试题
吉林省长春市东北师范大学附属中学2023-2024学年高二上学期10月期中化学试题(已下线)寒假作业06 盐类的水解-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)浙江省杭州东方中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
2 . 二氧化碳(碳酸)、碳酸氢盐及碳酸盐在生产和生活中有广泛的用途。
(1)碳酸( )、次氯酸(HClO)的电离平衡常数如表:
)、次氯酸(HClO)的电离平衡常数如表:
将少量 气体通入NaClO溶液中,反应的离子方程式为
气体通入NaClO溶液中,反应的离子方程式为_______ 。
(2)小苏打( )可用作糕点的发酵剂。
)可用作糕点的发酵剂。 溶液显
溶液显_______ (填“酸”、“碱”或“中”)性,溶液中含碳微粒浓度大小关系为_______ 。
(3)泡沫灭火器中存放的物质主要是 和
和 溶液,使用时,将两物质混合即可产生大量的
溶液,使用时,将两物质混合即可产生大量的 气体,写出反应的离子方程式
气体,写出反应的离子方程式_______ 。
(4)热的纯碱溶液能去除衣物表面的油污,原因是_______ (用离子方程式表示)。 溶液中存在的阴离子浓度大小关系为
溶液中存在的阴离子浓度大小关系为_______ 。
(5)常温下,向20.00mL 溶液中逐滴滴加0.1mol/L盐酸,溶液中含碳元素的三种微粒
溶液中逐滴滴加0.1mol/L盐酸,溶液中含碳元素的三种微粒 、
、 、
、 (
( 因逸出未画出)的物质的量分数随溶液pH变化的部分情况如图所示。
因逸出未画出)的物质的量分数随溶液pH变化的部分情况如图所示。
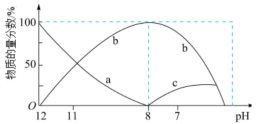
①下列叙述正确的是_______ 。
a. 的溶液中不存在
的溶液中不存在
b.曲线b代表的微粒是
c.当 时,
时,
d. 的溶液中
的溶液中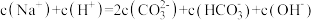
②量取20.00mL 溶液应选用的仪器是
溶液应选用的仪器是_______ (填“酸式滴定管”“碱式滴定管”或“量筒”),将量取的 溶液注入锥形瓶中,滴入几滴酚酞作指示剂,用0.1000mol/L的标准盐酸进行滴定,滴定终点的现象是
溶液注入锥形瓶中,滴入几滴酚酞作指示剂,用0.1000mol/L的标准盐酸进行滴定,滴定终点的现象是_______ 。若消耗盐酸的体积为21.40mL,则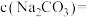
_______ mol/L(结果保留四位有效数字)。
(1)碳酸(
 )、次氯酸(HClO)的电离平衡常数如表:
)、次氯酸(HClO)的电离平衡常数如表:| 弱酸 |  | HClO |
| 电离平衡常数(25℃) |   |  |
 气体通入NaClO溶液中,反应的离子方程式为
气体通入NaClO溶液中,反应的离子方程式为(2)小苏打(
 )可用作糕点的发酵剂。
)可用作糕点的发酵剂。 溶液显
溶液显(3)泡沫灭火器中存放的物质主要是
 和
和 溶液,使用时,将两物质混合即可产生大量的
溶液,使用时,将两物质混合即可产生大量的 气体,写出反应的离子方程式
气体,写出反应的离子方程式(4)热的纯碱溶液能去除衣物表面的油污,原因是
 溶液中存在的阴离子浓度大小关系为
溶液中存在的阴离子浓度大小关系为(5)常温下,向20.00mL
 溶液中逐滴滴加0.1mol/L盐酸,溶液中含碳元素的三种微粒
溶液中逐滴滴加0.1mol/L盐酸,溶液中含碳元素的三种微粒 、
、 、
、 (
( 因逸出未画出)的物质的量分数随溶液pH变化的部分情况如图所示。
因逸出未画出)的物质的量分数随溶液pH变化的部分情况如图所示。
①下列叙述正确的是
a.
 的溶液中不存在
的溶液中不存在
b.曲线b代表的微粒是

c.当
 时,
时,
d.
 的溶液中
的溶液中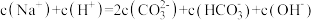
②量取20.00mL
 溶液应选用的仪器是
溶液应选用的仪器是 溶液注入锥形瓶中,滴入几滴酚酞作指示剂,用0.1000mol/L的标准盐酸进行滴定,滴定终点的现象是
溶液注入锥形瓶中,滴入几滴酚酞作指示剂,用0.1000mol/L的标准盐酸进行滴定,滴定终点的现象是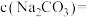
您最近一年使用:0次
名校
3 . 铝及铝的化合物有着极为广泛的用途。
(1)金属铝的生产是以Al2O3为原料,在熔融状态下用石墨做阴极和阳极进行电解:
2Al2O3 4Al+3O2↑,则电解时不断消耗的电极是
4Al+3O2↑,则电解时不断消耗的电极是_____ (填“阳极”或“阴极”)
(2)铝片、石墨、空气和海水构成的原电池可用于航标供电,该原电池正极的电极反应是_____ 。
(3)泡沫灭火器中NaHCO3溶液和Al2(SO4)3溶液发生反应的离子方程式是______ 。
(4)在配制AlCl3溶液时,防止溶液出现浑浊现象,溶液中应加入_____ 。
(5)Mg(OH)2固体能除去镁盐溶液中Al3+,原因是_____ 。(用离子方程式表示)
(1)金属铝的生产是以Al2O3为原料,在熔融状态下用石墨做阴极和阳极进行电解:
2Al2O3
 4Al+3O2↑,则电解时不断消耗的电极是
4Al+3O2↑,则电解时不断消耗的电极是(2)铝片、石墨、空气和海水构成的原电池可用于航标供电,该原电池正极的电极反应是
(3)泡沫灭火器中NaHCO3溶液和Al2(SO4)3溶液发生反应的离子方程式是
(4)在配制AlCl3溶液时,防止溶液出现浑浊现象,溶液中应加入
(5)Mg(OH)2固体能除去镁盐溶液中Al3+,原因是
您最近一年使用:0次
名校
解题方法
4 . 镁的化合物具有广泛用途,请回答有关镁的下列问题:
(1)单质镁在空气中燃烧的主要产物是________ ,还生成少量的________ (填化学式)。
(2)物质的量为0.10mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为_____________
A.3.2g B.4.0g C.4.2g D.4.6g
(3)镁作为一种强还原剂,还用于钛和铀的生产,写出镁与TiCl4在高温条件下制取钛的化学方程式_______________ 。
(4)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077),Mg2Cu与H2反应的化学方程式为___________ 。
(5)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是__________ ,该化合物水解时生成甲烷、氯化镁和氢氧化镁,请写出该反应的化学方程式______________________ 。
(1)单质镁在空气中燃烧的主要产物是
(2)物质的量为0.10mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为
A.3.2g B.4.0g C.4.2g D.4.6g
(3)镁作为一种强还原剂,还用于钛和铀的生产,写出镁与TiCl4在高温条件下制取钛的化学方程式
(4)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077),Mg2Cu与H2反应的化学方程式为
(5)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是
您最近一年使用:0次
名校
5 . NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是__________________ 。(用必要的化学用语和相关文字说明)。
(2)相同条件下,0.1 mol·L-1 NH4Al(SO4)2中c(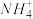 )
)________ (填“等于”“大于”或“小于”)0.1 mol·L-1 NH4HSO4中c(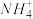 )。
)。
(3)0.1 mol·L-1电解质溶液的pH随温度变化的图象如图所示:

①其中符合0.1 mol·L-1 NH4Al(SO4)2的pH随温度变化的曲线是________ (填写序号),导致pH随温度变化的原因是__________________ ;
②20℃时,0.1mol·L-1NH4Al(SO4)2中2c( )-c(
)-c(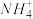 )-3c(Al3+)=
)-3c(Al3+)=________ (填数值)。
(1)NH4Al(SO4)2可作净水剂,其理由是
(2)相同条件下,0.1 mol·L-1 NH4Al(SO4)2中c(
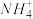 )
)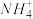 )。
)。(3)0.1 mol·L-1电解质溶液的pH随温度变化的图象如图所示:

①其中符合0.1 mol·L-1 NH4Al(SO4)2的pH随温度变化的曲线是
②20℃时,0.1mol·L-1NH4Al(SO4)2中2c(
 )-c(
)-c(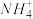 )-3c(Al3+)=
)-3c(Al3+)=
您最近一年使用:0次
2019-11-27更新
|
121次组卷
|
2卷引用:黑龙江省哈尔滨市尚志市尚志中学2019-2020学年高二上学期期中化学试题
6 . 盐和碳酸氢盐的用途非常广泛。
(1)据记载古人用草木灰(K2CO3)洗头发,可以除去头皮上的油污,用文字表述其原因_________________________________ 。
(2)现代泡沫灭火器的外筒装的是NaHCO3 溶液,内筒装的是 Al2(SO4)3 溶液,使用时只需将灭火器倒过来,即可喷出大量泡沫,起到灭火作用,请用离子方程式表示其原理_____ 。
(1)据记载古人用草木灰(K2CO3)洗头发,可以除去头皮上的油污,用文字表述其原因
(2)现代泡沫灭火器的外筒装的是NaHCO3 溶液,内筒装的是 Al2(SO4)3 溶液,使用时只需将灭火器倒过来,即可喷出大量泡沫,起到灭火作用,请用离子方程式表示其原理
您最近一年使用:0次
名校
解题方法
7 . I甲、乙、丙、丁分别是由H+、Na+、Al3+、Ba2+、OH-、Cl-、HCO3- 离子中的两种组成,可以发生如图转化:

(1)写出无色气体B的一种用途_____________________________ 。
(2)甲与乙反应的离子方程式为:____________________________ 。
(3)白色沉淀A可能溶解在溶液D中,其溶解的化学方程式为:________________ 。
II无水NiCl2在有机合成中有着极为重要的作用,工业上常用含镍原料所制得的NiCl2·6H2O在亚硫酰氯(SOCl2)中加热脱水制得,已知SOCl2能与水反应生成SO2和HCl。写出NiCl2·6H2O在亚硫酰氯(SOCl2)中加热脱水制无水NiCl2的化学方程式___________________________________ ,NiCl2·6H2O需在亚硫酰氯(SOCl2)中加热脱水的原因是________________________________ 。
III锰及其化合物用途广泛。锰的化合物有60多种,其中以二氧化锰(MnO2)最稳定。将固体草酸锰(MnC2O4·2H2O)放在一个可以称出质量的容器里加热。固体质量随温度的变化关系如图所示,则:214 ℃时,剩余固体的成分为___________ (填化学式); 943 ℃时,剩余固体的成分为__________ (填名称)。


(1)写出无色气体B的一种用途
(2)甲与乙反应的离子方程式为:
(3)白色沉淀A可能溶解在溶液D中,其溶解的化学方程式为:
II无水NiCl2在有机合成中有着极为重要的作用,工业上常用含镍原料所制得的NiCl2·6H2O在亚硫酰氯(SOCl2)中加热脱水制得,已知SOCl2能与水反应生成SO2和HCl。写出NiCl2·6H2O在亚硫酰氯(SOCl2)中加热脱水制无水NiCl2的化学方程式
III锰及其化合物用途广泛。锰的化合物有60多种,其中以二氧化锰(MnO2)最稳定。将固体草酸锰(MnC2O4·2H2O)放在一个可以称出质量的容器里加热。固体质量随温度的变化关系如图所示,则:214 ℃时,剩余固体的成分为

您最近一年使用:0次
2018-01-01更新
|
447次组卷
|
2卷引用:福建省莆田第六中学2018届高三上学期期中考试化学试题



