1 . 下列实验中均使用了饱和食盐水,实验设计不严谨的是
| 编号 | A | B | C | D |
| 实验 | 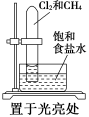 | 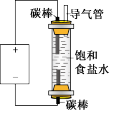 | 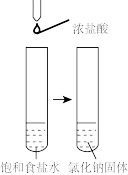 | 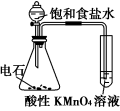 |
| 目的 | 验证甲烷与氯气发生化学反应 | 制消毒液 | 验证氯化钠的溶解平衡 | 得到平稳的气流 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-12-25更新
|
172次组卷
|
2卷引用:上海市杨浦区2022届高三一模化学试题
名校
2 . 已知常温下CaCO3的Ksp=2.8×10-9,CaSO4的Ksp=9.1×10-6,将CaCO3与CaSO4的饱和溶液等体积混合,再加入足量浓CaCl2溶液,下列说法正确的是
| A.只产生CaCO3沉淀 | B.产生等量的CaCO3和CaSO4沉淀 |
| C.产生的CaSO4沉淀更多 | D.产生的CaCO3沉淀更多 |
您最近一年使用:0次
2019-07-03更新
|
513次组卷
|
6卷引用:上海市第三女子中学2023-2024学年高二上学期等级班12月测试化学试题
上海市第三女子中学2023-2024学年高二上学期等级班12月测试化学试题 湖北省天门市、仙桃市、潜江市2018-2019学年高二下学期期末考试化学试题(已下线)2019年11月14日 《每日一题》人教版(选修4)——溶度积的应用江西省赣州市宁师中学2019-2020学年高二12月月考化学试题(已下线)3.4+难溶电解质的溶解平衡-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)【精品卷】3.4.2 沉淀溶解平衡的应用-人教版2023-2024学年选择性必修1
名校
3 . 欲使Ca(OH)2悬浊液变澄清,可以选择加入的试剂是( )
| A.CaCl2浓溶液 | B.NaOH浓溶液 | C.NH4Cl浓溶液 | D.MgCl2浓溶液 |
您最近一年使用:0次
2020-10-23更新
|
275次组卷
|
2卷引用:上海市复旦大学附属中学2021届高三上学期第一次教学质量检测化学试题
4 . 常温下,Ca(OH)2的溶解度为0.16克/100克水。向盛有50毫升水的烧杯中加入2克生石灰,搅拌后恢复到原温。下列说法正确的是
| A.在此过程中,水的Kw值始终保持不变 |
| B.在此过程中,Ca(OH)2的电离程度先变大后变小,最后不变 |
| C.反应结束后,溶液中水的电离程度比纯水小 |
| D.最后所得体系中的平衡状态只有水的电离平衡 |
您最近一年使用:0次
名校
解题方法
5 . 某同学为了验证难溶的氯化银在水中也存在溶解平衡,设计了如下实验方案:( )
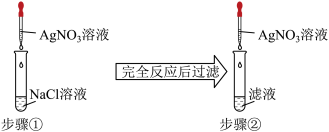

| A.步骤①中应加入过量的AgNO3溶液 |
| B.步骤①中应使NaCl溶液过量 |
| C.步骤②中现象是无沉淀产生 |
| D.步骤②中选用的AgNO3溶液浓度应小于步骤① |
您最近一年使用:0次
2020-04-03更新
|
220次组卷
|
2卷引用:2018年上海市高中学生化学竞赛(“华理一化工杯”)初赛试题
名校
6 . 已知25℃时,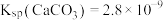 ,
, 式量为100。
式量为100。
(1)书写表示 沉淀溶解平衡的方程式
沉淀溶解平衡的方程式___________ 。
(2)计算25℃ 的溶解度
的溶解度___________  水。(保留2位有效数字)
水。(保留2位有效数字)
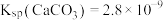 ,
, 式量为100。
式量为100。(1)书写表示
 沉淀溶解平衡的方程式
沉淀溶解平衡的方程式(2)计算25℃
 的溶解度
的溶解度 水。(保留2位有效数字)
水。(保留2位有效数字)
您最近一年使用:0次
名校
7 . 饱和硫酸铜溶液中放入一块不规则胆矾晶体,保持温度不变,胆矾晶体形状逐渐变为规则。下列有关描述正确的是( )
| A.此过程中,胆矾晶体质量发生改变 |
| B.比过程中,溶解速率大于结晶速率 |
| C.此过程中,溶解速率小于结晶速率 |
| D.此过程中,始终保持溶解平衡状态 |
您最近一年使用:0次
名校
解题方法
8 . 关于沉淀溶解平衡和溶度积常数,下列说法不正确的是
| A.Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
B.向1 mL 2mo/L NaOH溶液中先滴加2滴0.1mol/L  溶液,再滴加2滴0.1mo/L 溶液,再滴加2滴0.1mo/L  溶液,先生成白色沉淀,后生成红褐色沉淀,说明 溶液,先生成白色沉淀,后生成红褐色沉淀,说明 |
C.25℃时 在水中的溶解度大于其在 在水中的溶解度大于其在 溶液中的溶解度 溶液中的溶解度 |
D.已知某温度下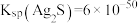 , ,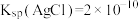 ,则 ,则 的平衡常数约为 的平衡常数约为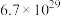 |
您最近一年使用:0次
2021-12-04更新
|
154次组卷
|
2卷引用:上海市上海中学2023-2024学年高二上学期期中考试化学试题
解题方法
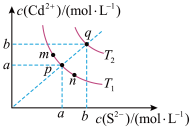
9 . 绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料。其在水中CdS(s) Cd2+(aq)+S2-(aq),达到沉淀溶解平衡时,定义溶度积Ksp=c(Cd2+)·c(S2-)。下图为CdS的沉淀溶解平衡曲线。下列说法错误的是
Cd2+(aq)+S2-(aq),达到沉淀溶解平衡时,定义溶度积Ksp=c(Cd2+)·c(S2-)。下图为CdS的沉淀溶解平衡曲线。下列说法错误的是
 Cd2+(aq)+S2-(aq),达到沉淀溶解平衡时,定义溶度积Ksp=c(Cd2+)·c(S2-)。下图为CdS的沉淀溶解平衡曲线。下列说法错误的是
Cd2+(aq)+S2-(aq),达到沉淀溶解平衡时,定义溶度积Ksp=c(Cd2+)·c(S2-)。下图为CdS的沉淀溶解平衡曲线。下列说法错误的是
| A.图中a和b分别为T1、T2温度下CdS在水中的溶解度 |
| B.图中各点对应的Ksp的关系为:Ksp(m)<Ksp(n)<Ksp(p)<Ksp(q) |
| C.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动 |
| D.加水稀释,q点沿qp线向p方向移动 |
您最近一年使用:0次
名校
解题方法
10 . 已知,常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.3×10-17,下列叙述正确的是
| A.常温下,AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小 |
| B.向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色 |
| C.0.1molAgCl和0.1molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |
| D.向AgCl的饱和溶液中加入NaCl晶体有AgCl析出,溶液中c(Ag+)仍与c(Cl-)相等 |
您最近一年使用:0次
2020-11-03更新
|
273次组卷
|
4卷引用:上海市上海中学2022-2023学年高二上学期期中考试化学试题
上海市上海中学2022-2023学年高二上学期期中考试化学试题上海市新中高级中学2023-2024学年高二下学期阶段检测化学试题 重庆市秀山高级中学校2020-2021学年高二上学期10月月考化学试题(已下线)专题3.4.1 难溶电解质的溶解平衡(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)



