1 . 室温下,氢氧化钙固体在水溶液中达到溶解平衡:Ca(OH)2 (s)  Ca2++2OH-,向其中加入以下物质,恢复到室温,Ca(OH)2固体减少的是
Ca2++2OH-,向其中加入以下物质,恢复到室温,Ca(OH)2固体减少的是
 Ca2++2OH-,向其中加入以下物质,恢复到室温,Ca(OH)2固体减少的是
Ca2++2OH-,向其中加入以下物质,恢复到室温,Ca(OH)2固体减少的是| A.CH3COONa | B.AlCl3 | C.NaOH | D.CaCl2 |
您最近一年使用:0次
2 . 捕集CO2的技术对解决全球温室效应意义重大。目前国际空间站处理CO2的一个重要方法是将CO2还原,涉及的化学反应如下:CO2(g)+4H2(g)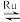 CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)
完成下列填空:
(1)该反应的平衡常数表达式为________________________________ 。如果改变某种条件,平衡向正反应方向移动,则平衡常数________ (填写编号)。
a、一定增大 b、一定减小 c、可能增大 d、可能减小 e、可能不变
(2)为了提高CO2的捕获百分率,可采取的措施是____________________ 。(任写一条)
(3)向2L某密闭容器充入1mol CO2和4mol H2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为_______________ 。CO2还可应用于纯碱工业。工业生产纯碱的过程中,向饱和的氨化食盐水中通入足量CO2的生产环节又被称为“碳酸化”。
(4)碳酸化时产生的现象是____________________________ 。碳酸化过程中,溶液中c(CO32-)的变化情况为____________________ 。
(5)碳酸化后过滤,留在滤液中的阳离子主要有_______________ (填写化学式)。简述检验滤液中Cl- 离子的实验操作。________________________________
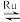 CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)完成下列填空:
(1)该反应的平衡常数表达式为
a、一定增大 b、一定减小 c、可能增大 d、可能减小 e、可能不变
(2)为了提高CO2的捕获百分率,可采取的措施是
(3)向2L某密闭容器充入1mol CO2和4mol H2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为
(4)碳酸化时产生的现象是
(5)碳酸化后过滤,留在滤液中的阳离子主要有
您最近一年使用:0次
3 . 将足量的AgCl(s)分别添加到下述四种溶液中,所得溶液c(Ag+)最小的是
| A.10 mL 0.4mol·L-1的盐酸 | B.10 mL 0.3mol·L-1MgCl2溶液 |
| C.10 mL 0.5mol·L-1NaCl溶液 | D.10 mL 0.1mol·L-1AlCl3溶液 |
您最近一年使用:0次
2016-12-09更新
|
271次组卷
|
6卷引用:上海市六校2015年高三下学期第二次联考化学试题
4 . 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知: pX=-lgc(X)。下列说法正确的是
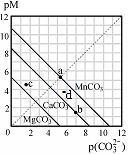

| A.在该温度下,MgCO3、MnCO3的溶解度依次增大 |
| B.d点可表示MnCO3的过饱和溶液,且c(Mn2+)>c(CO32-) |
| C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |
| D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO32-) |
您最近一年使用:0次
5 . 已知25℃时溶解度:AgCl> AgI,若在5 mL含有KCl和KI各为0.01mol/L的溶液中,加入8 mL 0.01 mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
| A.c(K+)>c(NO3-)>c(Ag+)=c(Cl-)+c(I-) | B.c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| C.c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-) | D.c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) |
您最近一年使用:0次
6 . 常温下,往饱和石灰水中加入一定量的生石灰,一段时间后恢复到原温度,以下叙述错误的是
| A.有溶质析出 | B.溶液中Ca2+的数目不变 |
| C.溶剂的质量减小 | D.溶液的pH不变 |
您最近一年使用:0次
2016-12-09更新
|
311次组卷
|
3卷引用:2015届上海市闵行区高三下学期质量调研考试(二模)化学试卷
名校
7 . 钒被称为“工业味精”,在发展现代工业、国防等方面发挥着重要的作用。 有强氧化性,在实验室以
有强氧化性,在实验室以 为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为
为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为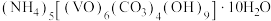 ,是制备热敏材料
,是制备热敏材料 的原料。过程如下:
的原料。过程如下:

已知:①氧化性: ;②
;② 能被
能被 氧化。
氧化。
1.步骤I中除生成 外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为
外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为___________ 。若只用浓盐酸与 反应也能制备
反应也能制备 溶液,从环保角度分析,使用
溶液,从环保角度分析,使用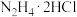 的目的是
的目的是___________ 。
步骤Ⅱ可在如图装置中进行: 被氧化,上述装置依次连接的合理顺序为c→
被氧化,上述装置依次连接的合理顺序为c→___________ (按气流方向,用小写字母表示)。盛有 溶液的仪器名称为
溶液的仪器名称为___________ 。
3.连接好装置,检查气密性良好后,加入试剂,开始实验,具体操作为___________ 。
4.实验结束时,将析出的产品过滤,用饱和 溶液洗涤。请从化学平衡的角度解释使用饱和
溶液洗涤。请从化学平衡的角度解释使用饱和 溶液洗涤晶体的原因:
溶液洗涤晶体的原因:___________ 。证明沉淀已经洗涤干净的方法是___________ 。
测定粗产品中钒的含量。实验步骤如下:
称量a g产品于锥形瓶中,用稀硫酸溶解后得到的溶液,加入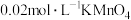 溶液至稍过量,加入某还原剂除去过量
溶液至稍过量,加入某还原剂除去过量 溶液,最后用
溶液,最后用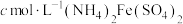 标准溶液滴定至终点(
标准溶液滴定至终点( ),消耗标准溶液的体积为b mL。
),消耗标准溶液的体积为b mL。
5.粗产品中钒的质量分数表达式为___________ (以 计,式量为67)。
计,式量为67)。
6.若 标准溶液部分变质,则测定结果
标准溶液部分变质,则测定结果___________ 。
A.偏高 B.偏低 C.无影响
 有强氧化性,在实验室以
有强氧化性,在实验室以 为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为
为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为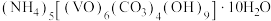 ,是制备热敏材料
,是制备热敏材料 的原料。过程如下:
的原料。过程如下:
已知:①氧化性:
 ;②
;② 能被
能被 氧化。
氧化。1.步骤I中除生成
 外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为
外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为 反应也能制备
反应也能制备 溶液,从环保角度分析,使用
溶液,从环保角度分析,使用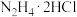 的目的是
的目的是步骤Ⅱ可在如图装置中进行:

 被氧化,上述装置依次连接的合理顺序为c→
被氧化,上述装置依次连接的合理顺序为c→ 溶液的仪器名称为
溶液的仪器名称为3.连接好装置,检查气密性良好后,加入试剂,开始实验,具体操作为
4.实验结束时,将析出的产品过滤,用饱和
 溶液洗涤。请从化学平衡的角度解释使用饱和
溶液洗涤。请从化学平衡的角度解释使用饱和 溶液洗涤晶体的原因:
溶液洗涤晶体的原因:测定粗产品中钒的含量。实验步骤如下:
称量a g产品于锥形瓶中,用稀硫酸溶解后得到的溶液,加入
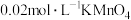 溶液至稍过量,加入某还原剂除去过量
溶液至稍过量,加入某还原剂除去过量 溶液,最后用
溶液,最后用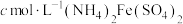 标准溶液滴定至终点(
标准溶液滴定至终点( ),消耗标准溶液的体积为b mL。
),消耗标准溶液的体积为b mL。5.粗产品中钒的质量分数表达式为
 计,式量为67)。
计,式量为67)。6.若
 标准溶液部分变质,则测定结果
标准溶液部分变质,则测定结果A.偏高 B.偏低 C.无影响
您最近一年使用:0次
名校
8 . 向饱和澄清石灰水中加入少量CaC2,充分反应后立即测定所得溶液中离子浓度,下列预测正确的是
| A.c(Ca2+)、c(OH-)一定增大 | B.c(Ca2+)、c(OH-)一定保持不变 |
| C.c(Ca2+)、c(OH-)均可能减小 | D.c(OH-)增大、c(H+)减小 |
您最近一年使用:0次
2016-12-09更新
|
145次组卷
|
3卷引用:2015届上海市长宁区高三上学期教学质量检测化学试卷
9 . 请回答:
(1)写出CH3Cl的电子式____ 。
(2)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下10g甲硅烷自燃放出热量473.5kJ,其热化学方程式是____ 。
(3)工业废水中加入难溶于水的FeS使其中的Cu2+离子转化为沉淀,写出该反应的离子方程式___ 。
(4)碱性条件下发生下列反应,配平该反应的离子方程式:__ ClO3﹣+__ Fe3++__ =__ Cl﹣+__ FeO42﹣+__ 。
(1)写出CH3Cl的电子式
(2)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下10g甲硅烷自燃放出热量473.5kJ,其热化学方程式是
(3)工业废水中加入难溶于水的FeS使其中的Cu2+离子转化为沉淀,写出该反应的离子方程式
(4)碱性条件下发生下列反应,配平该反应的离子方程式:
您最近一年使用:0次
10 . 关于某温度时的饱和溶液的说法中,正确的是
| A.已溶解的溶质和未溶解的溶质质量相等 |
| B.溶质不再溶解,因此从表面看溶质不再减少,也不再增加 |
| C.升高温度,饱和溶液将变为不饱和溶液 |
| D.溶质的溶解和结晶继续进行,且速率相等 |
您最近一年使用:0次



