名校
解题方法
1 . 将等量的固体Mg(OH)2,置于等体积的下列液体中,最终固体剩余最少的是( )
| A.在纯水中 | B.在0.1mol/L的MgCl2溶液中 |
| C.在0.1mol/L的NH3·H2O中 | D.在0.1mol/L的CH3COOH溶液中 |
您最近一年使用:0次
2020-01-04更新
|
194次组卷
|
3卷引用:上海市静安区2020届高三上学期第一次模拟考试化学试题
真题
名校
2 . 向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中
| A.c(Ca2+)、c(OH-)均增大 | B.c(Ca2+)、c(OH-)均保持不变 |
| C.c(Ca2+)、c(OH-)均减小 | D.c(OH-)增大、c(H+)减小 |
您最近一年使用:0次
2016-12-09更新
|
1802次组卷
|
4卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(上海卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(上海卷)上海市虹口区2016届高三12月第二次分层练习化学试题(已下线)上海市宝山区行知中学2015届高三上学期第一次月考化学试题上海市实验学校2021-2022学年高三下学期4月月考化学试题
2012·上海奉贤·二模
3 . 工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。该法的工艺流程为
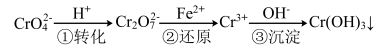
其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显____________ 色.
(2)能说明第①步反应达平衡状态的是_____________ 。
a Cr2O72-和CrO42-的浓度相同 b 2v(Cr2O72-)=v(CrO42-)
c 溶液的颜色不变 d.溶液的pH值不变
(3)第②步中,还原0.01mol Cr2O72-离子,需要________ mol的FeSO4·7H2O。
(4)许多过渡(金属)元素的氢氧化物在水中有两种电离方式,Cr(OH)3在溶液中存在以下平衡:H+ + CrO2-(亮绿色)+H2O Cr(OH)3(s)
Cr(OH)3(s) Cr3+(紫色)+ 3OH-
Cr3+(紫色)+ 3OH-
下列有关说法中正确的是_______
a 加酸则平衡向右移动,则生成Cr3+盐,加碱则平衡向左移动,生成亚铬酸盐(CrO2-)
b 在一定条件下存在:Cr(OH)3+OH-=CrO2-+2H2O;Cr(OH)3+3H+=Cr3++3H2O
c Cr3+盐中加入NaOH溶液,先产生沉淀,后沉淀消失,溶液变成无色
d Cr(OH)3(固)在水中的存在叁个平衡

其中第①步存在平衡:2CrO42-(黄色)+2H+
 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O(1)若平衡体系的pH=2,则溶液显
(2)能说明第①步反应达平衡状态的是
a Cr2O72-和CrO42-的浓度相同 b 2v(Cr2O72-)=v(CrO42-)
c 溶液的颜色不变 d.溶液的pH值不变
(3)第②步中,还原0.01mol Cr2O72-离子,需要
(4)许多过渡(金属)元素的氢氧化物在水中有两种电离方式,Cr(OH)3在溶液中存在以下平衡:H+ + CrO2-(亮绿色)+H2O
 Cr(OH)3(s)
Cr(OH)3(s) Cr3+(紫色)+ 3OH-
Cr3+(紫色)+ 3OH-下列有关说法中正确的是
a 加酸则平衡向右移动,则生成Cr3+盐,加碱则平衡向左移动,生成亚铬酸盐(CrO2-)
b 在一定条件下存在:Cr(OH)3+OH-=CrO2-+2H2O;Cr(OH)3+3H+=Cr3++3H2O
c Cr3+盐中加入NaOH溶液,先产生沉淀,后沉淀消失,溶液变成无色
d Cr(OH)3(固)在水中的存在叁个平衡
您最近一年使用:0次
9-10高二下·北京·期末
名校
4 . 一定温度下,在氢氧化钡的悬浊液中,存在氢氧化钡固体与其电离的离子间的溶解平衡关系:Ba(OH)2(固体) 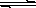 Ba2++2OH-。向此种悬浊液中加入少量的氧化钡粉末,下列叙述正确的是:
Ba2++2OH-。向此种悬浊液中加入少量的氧化钡粉末,下列叙述正确的是:
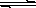 Ba2++2OH-。向此种悬浊液中加入少量的氧化钡粉末,下列叙述正确的是:
Ba2++2OH-。向此种悬浊液中加入少量的氧化钡粉末,下列叙述正确的是:| A.溶液中氢氧根离子浓度增大 | B.溶液中钡离子浓度减少 |
| C.溶液中钡离子数目减小 | D.pH减小 |
您最近一年使用:0次
2019-01-30更新
|
919次组卷
|
8卷引用:上海市奉贤区2012届高三5月综合练习(三模)化学试题
(已下线)上海市奉贤区2012届高三5月综合练习(三模)化学试题(已下线)2010年北京五中高二下学期期末考试化学试题(已下线)2010-2011学年山西省临汾一中高二上学期期末考试化学试卷(已下线)2013届浙江省慈溪中学高三第一次月考化学试卷(已下线)2012年人教版高中化学选修4 3.4难溶电解质的溶解平衡练习卷陕西省西安市第26中2017-2018学年第一学期高二期中考试化学试卷.安徽省肥东县高级中学2020-2021学年高二上学期期中考试化学试题陕西省榆林市第十二中学2020-2021学年高二下学期第一次月考化学试题
5 . 工业产生的废气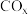 、
、 、
、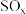 对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。
对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。
(1)光气 是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过
是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过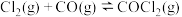 制备。图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
制备。图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
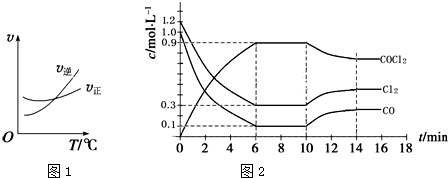
①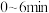 内,反应的平均速率
内,反应的平均速率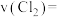
________ ;
② 改变的条件是
改变的条件是________ ,该反应平衡常数变化的趋势是________ (填“增大”、“减小”或“不变”)。
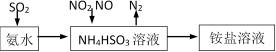
(2)利用氨水可以将 和
和 吸收,原理如下图所示:
吸收,原理如下图所示: 被吸收的离子方程式为
被吸收的离子方程式为________ 。
(3) 在自然界循环时可与
在自然界循环时可与 反应,
反应, 难溶于水,可溶于盐酸,请用平衡移动原理解释
难溶于水,可溶于盐酸,请用平衡移动原理解释 可溶于盐酸的原因
可溶于盐酸的原因________ 。
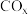 、
、 、
、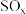 对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。
对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。(1)光气
 是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过
是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过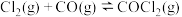 制备。图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
制备。图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
①
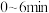 内,反应的平均速率
内,反应的平均速率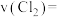
②
 改变的条件是
改变的条件是(2)利用氨水可以将
 和
和 吸收,原理如下图所示:
吸收,原理如下图所示: 被吸收的离子方程式为
被吸收的离子方程式为
(3)
 在自然界循环时可与
在自然界循环时可与 反应,
反应, 难溶于水,可溶于盐酸,请用平衡移动原理解释
难溶于水,可溶于盐酸,请用平衡移动原理解释 可溶于盐酸的原因
可溶于盐酸的原因
您最近一年使用:0次
名校
解题方法
6 . 二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要,完成下列填空:
(1)方法一:活性炭法2C(s)+2SO2(g) S2(g)+2CO2(g)
S2(g)+2CO2(g)
上述反应的化学平衡常数表达式为__ 、若在某密闭容器中进行上述反应,为了加快吸收SO2,可采取的措施有___ 。
(2)方法二:氨水脱硫法该法采用喷雾吸收法,雾化的氨水与烟气中的SO2直接接触吸收,一定温度下,往0.1mol·L-1氨水中加入少量NH4Cl固体,下列数值变小的是( )
A. B.c(NH3·H2O) C.
B.c(NH3·H2O) C.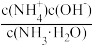 D.c(NH
D.c(NH )
)
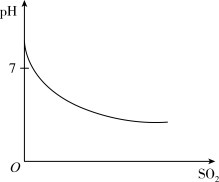
(3)方法三:钠碱循环法第一步是用Na2SO3水溶液吸收SO2,第二步是加热吸收溶液,可得到含高浓度SO2的水蒸气副产品。第一步吸收过程中pH值的变化如图所示,请根据图示,解释pH值变化的原因:__ 。
(4)方法四:双碱脱硫法先用烧碱吸收SO2,再利用CaO使NaOH碱液再生可循环使用,NaOH溶液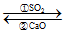 Na2SO3溶液。CaO在水中存在如下转化:CaO(s)+H2O(l)→Ca(OH)2(s)
Na2SO3溶液。CaO在水中存在如下转化:CaO(s)+H2O(l)→Ca(OH)2(s) Ca2+(aq)+2OH-(aq),从平衡移动的角度,简述过程②中NaOH再生的原理
Ca2+(aq)+2OH-(aq),从平衡移动的角度,简述过程②中NaOH再生的原理___ 。
(5)方法五:工业上石灰石膏法和碱法是常用的烟气脱硫法。其流程如图:
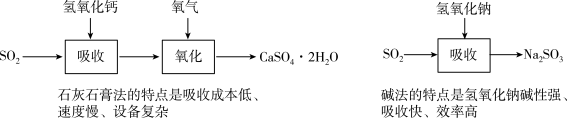
请在石灰石膏法和碱法的基础上,设计一个改进的、能实现物料循环脱硫方案___ (用物质转化流程图表示)。
(1)方法一:活性炭法2C(s)+2SO2(g)
 S2(g)+2CO2(g)
S2(g)+2CO2(g)上述反应的化学平衡常数表达式为
(2)方法二:氨水脱硫法该法采用喷雾吸收法,雾化的氨水与烟气中的SO2直接接触吸收,一定温度下,往0.1mol·L-1氨水中加入少量NH4Cl固体,下列数值变小的是
A.
 B.c(NH3·H2O) C.
B.c(NH3·H2O) C.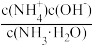 D.c(NH
D.c(NH )
)(3)方法三:钠碱循环法第一步是用Na2SO3水溶液吸收SO2,第二步是加热吸收溶液,可得到含高浓度SO2的水蒸气副产品。第一步吸收过程中pH值的变化如图所示,请根据图示,解释pH值变化的原因:

(4)方法四:双碱脱硫法先用烧碱吸收SO2,再利用CaO使NaOH碱液再生可循环使用,NaOH溶液
 Na2SO3溶液。CaO在水中存在如下转化:CaO(s)+H2O(l)→Ca(OH)2(s)
Na2SO3溶液。CaO在水中存在如下转化:CaO(s)+H2O(l)→Ca(OH)2(s) Ca2+(aq)+2OH-(aq),从平衡移动的角度,简述过程②中NaOH再生的原理
Ca2+(aq)+2OH-(aq),从平衡移动的角度,简述过程②中NaOH再生的原理(5)方法五:工业上石灰石膏法和碱法是常用的烟气脱硫法。其流程如图:

请在石灰石膏法和碱法的基础上,设计一个改进的、能实现物料循环脱硫方案
您最近一年使用:0次
7 . 常温下,以MnO2为原料制得的MnCl2溶液中常合有Cu2+、Pb2+等,通过添加过量的难溶电解质MnS,可使这些金属离子形成硫化物沉淀并过滤除去,下列说法正确的是
| A.过滤后的溶液中一定没有S2- |
| B.MnS难溶于水,可溶于MnCl2溶液中 |
| C.常温时,CuS、PbS比MnS更难溶 |
| D.加入MnS后生成CuS的离子方程式是Cu2++S2-→CuS↓ |
您最近一年使用:0次
8 . 在25℃时,有80g饱和Ba(OH)2溶液,向其中加入纯BaO粉末ag,反应后温度恢复到25℃,下列有关该溶液的说法正确的是( )
| A.溶液中c(Ba2+)将增大 | B.溶液的pH将增大 |
| C.溶液中Ba2+的物质的量将减少 | D.溶液中c(OH-)减少 |
您最近一年使用:0次
17-18高一上·上海·期末
名校
9 . 室温下,向饱和硫酸铜溶液中,投入不规则的胆矾,则
| A.胆矾的形状改变,质量不变 | B.体系中不再发生溶解过程 |
| C.溶液质量减小,浓度不变 | D.溶液中溶剂质量增大 |
您最近一年使用:0次
2012·上海虹口·二模
10 . 下列现象可以用勒夏特列原理解释的是
| A.高炉炼铁时焦炭和铁矿石要预先粉碎 |
| B.工业上在制盐酸的合成塔内往往输入过量氢气 |
| C.人们食用了酸性食品或碱性食品后,血液pH值仍稳定在7.4 ± 0.05 |
| D.在饱和硫酸铜溶液中放入胆矾晶体,几天后晶体外形发生改变,但质量未变 |
您最近一年使用:0次



