名校
1 . 有关AgCl沉淀的溶解平衡说法正确的是( )
| A.升高温度,AgCl沉淀的溶解度变小 |
| B.AgCl难溶于水,溶液中没有Ag+ 和Cl- |
| C.溶解平衡时,AgCl沉淀生成和溶解不断进行,但速率相等 |
| D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶度积Ksp变小 |
您最近一年使用:0次
2018-10-22更新
|
191次组卷
|
2卷引用:山西省晋中市祁县二中2018-2019学年高二下学期期中考试化学试题
真题
名校
2 . 根据下列图示所得出的结论不正确的是
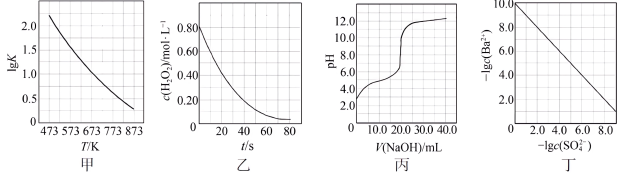

| A.图甲是CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0 |
| B.图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小 |
| C.图丙是室温下用0.1000 mol·L−1NaOH溶液滴定20.00 mL 0.1000 mol·L−1某一元酸HX的滴定曲线,说明HX是一元强酸 |
| D.图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+ )与c(SO42−)的关系曲线,说明溶液中c(SO42− )越大c(Ba2+ )越小 |
您最近一年使用:0次
2018-06-10更新
|
6775次组卷
|
31卷引用:【全国百强校】山西省临汾第一中学2017-2018学年高二下学期期末考试化学试题
【全国百强校】山西省临汾第一中学2017-2018学年高二下学期期末考试化学试题山西省临汾市2020届高三上学期第二次月考化学试题2018年全国普通高等学校招生统一考试化学(江苏卷)(已下线)2018届高三高考题及模拟题汇编 专题10 水溶液中的离子平衡湖北省随州市第二高级中学2018-2019学年高二9月起点考试(A班)化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【教学案】【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期期中考试化学试题【全国百强校】黑龙江省鹤岗市第一中学2019届高三上学期第三次月考化学试题江苏师范大学附属实验学校2019届高三上学期10月学情调研化学试题【全国百强校】河南省实验中学2019届高三上学期质量预测模拟(三)化学试题山东省日照青山学校2019届高三上学期第三次月考化学试题(已下线)2019高考备考二轮复习精品资料-专题9 化学反应速率与化学平衡(教学案)【全国百强校】四川省成都市成都外国语学校2018-2019学年高二下学期3月月考化学试题【区级联考】天津市河北区2019届高三一模考试化学试题江西省宜春市万载中学2019-2020学年高二上学期期中考试化学试题(衔接班)四川省眉山市2019-2020学年高二上学期期末考试化学(理科)试题江西省赣州市石城中学2020届高三上学期第二次月考化学试题福建省莆田第二十五中学2020届高三上学期期末考试化学试题【懂做原理题】2020届高三化学选修4二轮专题练—— 浓度商及其应用【精编23题】安徽省黄山市2019-2020学年高二上学期期末质量检测 化学(理)试题(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训四川省遂宁市船山区第二中学校2019-2020学年高二下学期期中考试化学试题北京市海淀区中关村中学2020届高三三模化学试题(已下线)小题必刷31 酸碱中和滴定及拓展应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷30 水的电离与溶液的酸碱性——2021年高考化学一轮复习小题必刷(通用版本)选择性必修1(SJ)专题3专题培优专练安徽省滁州市定远育才学校2022届高三上学期开学摸底考试化学试题江苏省马坝高级中学2022-2023学年高三上学期9月份质量检测化学试题浙江省2022-2023学年高三上学期选考科目适应性考试化学试题四川省眉山市彭山区第一中学2023-2024学年高二上学期12月月考化学试题四川省绵阳中学2023-2024学年高三上期测试(三)理科综合试题
真题
名校
3 . 用0.100 mol·L-1 AgNO3滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。下列有关描述错误的是
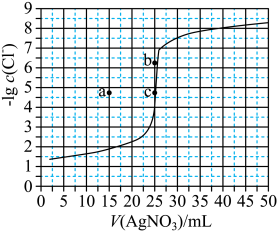
| A.根据曲线数据计算可知Ksp(AgCl)的数量级为10-10 |
| B.曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=Ksp(AgCl) |
| C.相同实验条件下,若改为0.0400 mol·L-1 Cl-,反应终点c移到a |
| D.相同实验条件下,若改为0.0500 mol·L-1 Br-,反应终点c向b方向移动 |
您最近一年使用:0次
2018-06-09更新
|
17989次组卷
|
54卷引用:山西省实验中学2018-2019学年高二上学期12月月考化学试题
山西省实验中学2018-2019学年高二上学期12月月考化学试题山西省山西大学附属中学、汾阳中学2020-2021学年高二上学期12月月考化学试题2018年全国普通高等学校招生统一考试化学(新课标III卷)(已下线)高考母题题源08 电解质溶液(已下线)2018届高三高考题及模拟题汇编 专题10 水溶液中的离子平衡湖北省随州市第二高级中学2018-2019学年高二9月起点考试(A班)化学试题【全国百强校】四川省棠湖中学2019届高三上学期期末考试理综-化学试题河南省周口市扶沟县高级中学2018-2019学年高二下学期第一次月考化学试题(已下线)专题8.4 难溶电解质的溶解平衡(讲)-《2020年高考一轮复习讲练测》西藏拉萨中学2019-2020学年高二上学期第三次月考理综化学试题(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》苏教版选修四化学反应原理专题3第四单元 难溶电解质的沉淀溶解平衡 同步检测试卷步步为赢 高二化学寒假作业:综合检测(二)2019年秋高三化学复习强化练习—— 难溶电解质的沉淀溶解平衡甘肃省会宁县第一中学2019-2020学年高二上学期期末考试化学试题湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题12 溶度积的应用复习题(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训河北省枣强中学2019-2020学年高二下学期第三次月考化学试题西藏自治区拉萨市拉萨中学2019-2020学年高二第五次月考理科综合化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3章 综合检测四川省江油中学2019-2020学年高二6月月考化学试题高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三章素养检测人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡(已下线)3.4+难溶电解质的溶解平衡-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)易错17 难溶电解质的溶解平衡及应用-备战2021年高考化学一轮复习易错题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过高考 3年真题强化闯关(已下线)小题必刷31 酸碱中和滴定及拓展应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷34 沉淀溶解平衡、溶度积常数及其应用——2021年高考化学一轮复习小题必刷(通用版本)海南省海南中学2021届高三第五次月考化学试题江西省抚州市金溪县第一中学2020-2021学年高二上学期第二次月考化学试题(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)广东省汕头市第一中学2020-2021学年高二上学期期末考试化学试题选择性必修1(SJ)专题3专题培优专练(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时41 酸碱中和滴定及拓展应用-2022年高考化学一轮复习小题多维练(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考向27 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点微专题(已下线)第5讲 沉淀溶解平衡-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)(已下线)3.4.1 难溶电解质的沉淀溶解平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)河南省信阳市2021-2022学年高二上学期期末考试化学试题福建省福州第八中学2021-2022学年高三上学期第三次质量检测化学试题(已下线)专题6 Ksp专练(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)福建师范大学附属中学2021-2022学年高三下学期开学考试化学试题江西省抚州市金溪县第一中学2021-2022学年高二下学期第二次月考化学试题湖南省长沙市第一中学2021-2022学年高三下学期月考(七)化学试题(已下线)专题06 水溶液中的离子平衡(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型142 有关沉淀溶解平衡图像新疆维吾尔自治区喀什第二中学2022-2023学年高二上学期1月期末考试化学试题北京市第二中学2023-2024学年高二上学期第二学段 段考化学试题
4 . 已知p(A)=-lgc(A),三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
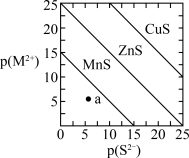

| A.a点无MnS沉淀生成 |
| B.CuS和MnS的悬浊液中,c(Cu2+)/c(Mn2+)=10-20 |
| C.向MnS悬浊液中加入少量CuCl2固体,c(Mn2+) 减小 |
| D.向含等浓度ZnCl2和CuCl2的溶液中逐滴加入饱和Na2S溶液,先析出的是ZnS |
您最近一年使用:0次
2018-03-27更新
|
365次组卷
|
2卷引用:山西省晋城市2018届高三上学期第一次模拟考试化学试题
名校
5 . 在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-。根据溶液中平衡时相关离子浓度的关系图,下列说法正确的是
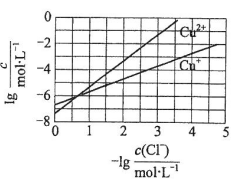

| A.Ksp(CuCl)的数量级为10-5 |
| B.加入Cu越多,Cu+浓度越高,除Cl-效果越好 |
| C.若有32g Cu参加反应,转移电子的数目为NA |
| D.除Cl-反应为Cu+Cu2++2 Cl-=2CuCl |
您最近一年使用:0次
名校
6 . 向饱和石灰水中投入0.56g氧化钙,并恢复到原来的温度,下列说法正确的是
| A.溶液的pH增大 | B.溶液中c(Ca2+)不变 |
| C.OH-数目不变 | D.析出的Ca(OH)2质量为0.74g |
您最近一年使用:0次
2017-12-20更新
|
227次组卷
|
4卷引用:山西省太原市第五中学2017-2018学年高二12月月考(理)化学试题
名校
7 . 下列说法不正确的是
| A.Na与H2O的反应是熵增的放热反应,该反应能自发进行 |
| B.向2支盛有2 mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI溶液,一支试管中产生黄色沉淀,另一支无明显现象,则可证明Ksp(AgI)<Ksp(AgCl) |
C.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)  Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 |
| D.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 |
您最近一年使用:0次
2017-12-20更新
|
120次组卷
|
2卷引用:山西省太原市第五中学2017-2018学年高二12月月考(理)化学试题
名校
8 . 20℃时,将足量的BaSO4固体溶于50mL水中,充分搅拌,慢慢加入Na2CO3固体,搅拌,溶液中随c(CO32-)增大时c(Ba2+)变化曲线如下图。则下列说正确的是
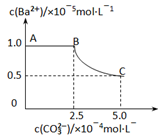

| A.20℃时Ksp(BaSO4)>Ksp(BaCO3) |
| B.加入Na2CO3固体立即有BaCO3固体生成 |
| C.BaCO3的Ksp=2.5×10-10 |
| D.曲线BC段内,c(CO32-):c(SO42-)=25 |
您最近一年使用:0次
2017-12-13更新
|
554次组卷
|
4卷引用:山西省康杰中学2018届高三第二次月考化学试卷
名校
9 . 硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
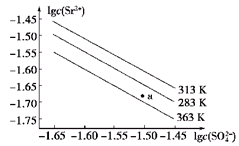

| A.283 K时,图中a点对应的溶液是饱和溶液 |
| B.温度一定时,Ksp(SrSO4)随c(SO42—)的增大而减小 |
| C.283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液 |
| D.三个不同温度中,313 K时Ksp(SrSO4)最大 |
您最近一年使用:0次
名校
10 . 25℃时,用0.1000 mol·L−1的AgNO3溶液分别滴定体积均为V0mL的且浓度均为0.1000mol·L−1的KCl、KBr及KI溶液,其滴定曲线入下图,已知25℃时,AgCl、AgBr及AgI溶度积常数依次为l.8×10-10、5.0×10-13、8.3×10-17,下列说法正确的是
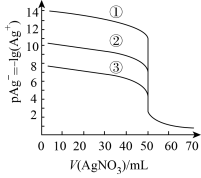

| A.V0= 45.00 |
| B.滴定曲线①表示KCl的滴定曲线 |
| C.滴定KCl时,可加入少量的KI作指示剂 |
| D.当AgNO3溶液滴定至60.00mL时,溶液中c(I-)<c(Br-)<c(Cl-) |
您最近一年使用:0次
2017-11-05更新
|
1070次组卷
|
6卷引用:山西实验中学、南海桂城中学2018届高三上学期联考化学试题
山西实验中学、南海桂城中学2018届高三上学期联考化学试题河北省定州中学2017-2018学年高二(承智班)上学期期中考试化学试题(已下线)黄金30题系列 高二化学(选修4) 小题易丢分陕西省高新中学2019届高三上学期月考化学试题(已下线)第八章 水溶液中的离子反应与平衡 第53讲 沉淀溶解平衡图像的分析广东省深圳市光明区2023-2024学年高二上学期1月期末学业水平调研化学试题



