10. 氨为重要化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
a.CH
4(g)+H
2O(g)

CO(g)+3H
2(g)
△H=+216.4KJ/mol
b.CO(g)+H
2O(g)

CO
2(g)+H
2(g)
△H=-41.2kJ/mol
则反应CH
4(g)+2H
2O(g)

CO
2(g)+4H
2(g)
△H=
______。
(2)起始时投入氮气和氢气分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度关系如图。
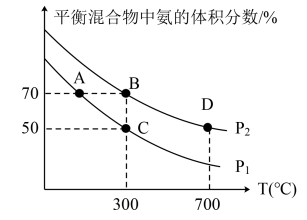
①恒压时,反应一定达到平衡状态的标志是
______(填序号):
A.N
2和H
2的转化率相等
B.反应体系密度保持不变
C.

的比值为3:2
D.

=2
②P
1______P
2(填“>”、“<”、“=”,下同):反应平衡常数:B点
______D点;
③C点H
2的转化率
______;(数值保留0.1%)在A、B两点条件下,该反应从开始到平衡时生成氢气平均速率:
v(A)
______v(B)(填“>”、“<”、“=”)。
(3)已知25℃时由Na
2SO
3和NaHSO
3形成的混合溶液恰好呈中性,则该混合溶液中各离子浓度的大小顺序为
______________(已知25℃时,H
2SO
3的电离平衡常数Ka
1=1×10
-2,Ka
2=1×10
-7)