某同学在实验室探究NaHCO3的性质:常温下,配制0.10 mol/ L NaHCO3溶液,测其pH为8.4;取少量该溶液滴加CaCl2溶液至pH=7,滴加过程中产生白色沉淀,但无气体放出。下列说法不正确的是
| A.NaHCO3溶液呈碱性的原因是HCO3-的水解程度大于电离程度 |
| B.反应的过程中产生的白色沉淀为CaCO3 |
| C.反应后的溶液中存在:c(Na+)+2c(Ca2+)=c(HCO3-)+2c(CO32-)+c(Cl-) |
| D.加入CaCl2促进了HCO3-的水解 |
更新时间:2019-04-02 16:36:33
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】探究铝片与Na2CO3溶液的反应。
下列说法错误的是
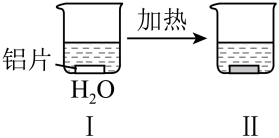 |  | |
| 均无明显现象 | 铝片表面产生细小气泡 | 加热后出现白色浑浊,产生大量气泡(经检验为H2和CO2) |
A.Na2CO3溶液中存在水解平衡:CO +H2O +H2O HCO HCO +OH- +OH- |
| B.对比I、III说明Na2CO3溶液能破坏铝表面的保护膜 |
C.H2逸出有利于CO 水解平衡向正反应方向移动 水解平衡向正反应方向移动 |
D.推测出现白色浑浊的原因:Al3++3HCO =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列溶液中有关物质的量浓度关系正确的是
A.0.1mol·L-1的NaHA溶液,其 |
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液: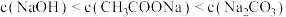 |
C.等物质的量的CH3COOH和CH3COONa溶于水: |
D.pH=2的HA溶液与pH=12的MOH溶液任意比混合: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 比较 和 和 氧化性的强弱 氧化性的强弱 | 向 溶液中滴入硫酸酸化的 溶液中滴入硫酸酸化的 溶液 溶液 | 溶液由浅绿色变为黄色说明氧化性:H2O2>Fe3+ |
| B | 判断Ka(CH3COOH)与Ka(HCOOH)大小关系 | 室温下,用 计测量等浓度的 计测量等浓度的 和 和 溶液的 溶液的 | 若前者大于后者,说明Ka(CH3COOH)>Ka(HCOOH) |
| C | 检验溶液是否含 | 向溶液中加入稀氢氧化钠溶液,用湿润的红色石蕊试纸靠近管口 | 若试纸未变蓝,则说明不含 |
| D | 探究 与 与 反应的限度 反应的限度 | 取1mL KI溶液于试管中,加入1mL KI溶液于试管中,加入1mL FeCl3溶液,充分反应后滴入5滴15% FeCl3溶液,充分反应后滴入5滴15% 溶液 溶液 | 若溶液变血红色,则 与 与 的反应有一定限度 的反应有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法错误的有几句
①NaHCO3溶液加水稀释, 的比值保持增大
的比值保持增大
②浓度均为0.1mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO )+c(HCO
)+c(HCO )]
)]
③在0.1mol·L-1氨水中滴加0.lmol·L-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol·L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO )均增大
)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
①NaHCO3溶液加水稀释,
 的比值保持增大
的比值保持增大②浓度均为0.1mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO
 )+c(HCO
)+c(HCO )]
)]③在0.1mol·L-1氨水中滴加0.lmol·L-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol·L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO
 )均增大
)均增大⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
| A.4 | B.3 | C.2 | D.1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室用0.1mol/L的NaOH溶液滴定 的
的 溶液。溶液中含氮微粒a、b的分布系数δ、NaOH溶液体积V(NaOH)与pH的关系如图所示。[已知
溶液。溶液中含氮微粒a、b的分布系数δ、NaOH溶液体积V(NaOH)与pH的关系如图所示。[已知 的分布系数
的分布系数 ]下列叙述错误的是
]下列叙述错误的是

 的
的 溶液。溶液中含氮微粒a、b的分布系数δ、NaOH溶液体积V(NaOH)与pH的关系如图所示。[已知
溶液。溶液中含氮微粒a、b的分布系数δ、NaOH溶液体积V(NaOH)与pH的关系如图所示。[已知 的分布系数
的分布系数 ]下列叙述错误的是
]下列叙述错误的是 
| A.x点对应溶液的pH约为5 |
B.p点对应的溶液中,  |
C.微粒b为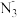 该滴定可选酚酞作指示剂 该滴定可选酚酞作指示剂 |
D.滴定到q点时,溶液中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】25℃时,向500 mL0.2 mol/L NaOH溶液中通入SO2气体(忽略反应过程中溶液的体积变化),设反应过程中 =x,已知H2SO3的电离平衡常数:Ka1=1.2×10-2,Ka2=5.6×10-8。下列说法正确的是
=x,已知H2SO3的电离平衡常数:Ka1=1.2×10-2,Ka2=5.6×10-8。下列说法正确的是
 =x,已知H2SO3的电离平衡常数:Ka1=1.2×10-2,Ka2=5.6×10-8。下列说法正确的是
=x,已知H2SO3的电离平衡常数:Ka1=1.2×10-2,Ka2=5.6×10-8。下列说法正确的是| A.x=1时,c(SO32-)+c(HSO3-)=0.2 mol/L |
| B.x<1时,溶液可能为酸性 |
C.x= 时,c(SO32-)+c(HSO3-)+c(OH-)=c(Na+)+c(H+) 时,c(SO32-)+c(HSO3-)+c(OH-)=c(Na+)+c(H+) |
D.x< 时,随通入SO2量增大, 时,随通入SO2量增大,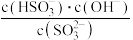 逐渐减小 逐渐减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
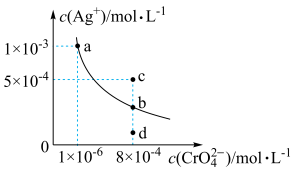
【推荐1】常温下,将0.025molBaSO4粉末置于盛有蒸馏水的烧杯中形成1L悬浊液,然后向烧杯中加入Na2CO3固体(忽略溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是


| A.曲线MP表示c(Ba2+)的变化 |
| B.BaSO4在BaCl2溶液中的Ksp随着BaCl2溶液浓度增大而减小 |
C.若要使反应BaSO4+CO  BaCO3+SO BaCO3+SO 正向进行,需满足 正向进行,需满足 <4×10-2 <4×10-2 |
D.BaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小关系为c(CO )>c(SO )>c(SO )>c(Ba2+)>c(OH-) )>c(Ba2+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知BaCO3和BaSO4均为难溶电解质,其溶度积分别为Ksp(BaCO3)=5.1×10-9 mol2·L-2,Ksp(BaSO4)=1.1×10-10mol2·L-2,则下列说法中正确的是
| A.BaSO4可做钡餐而BaCO3不能是因为Ksp(BaSO4)<Ksp(BaCO3) |
| B.在制腈纶纤维的1 L溶液中含SO42-为1.0×10-3mol,则加入0.01 mol BaCl2不能使SO42-完全沉淀 |
| C.在清理有关仪器的BaSO4沉淀时,常加入饱和Na2CO3溶液,使BaSO4转化为BaCO3再用酸处理 |
| D.用稀H2SO4洗涤BaSO4效果比用水好,BaCO3也能用此法处理 |
您最近一年使用:0次