名校
1 . 已知25℃物质的溶度积常数为:FeS:Ksp=6.3×10-18;CuS:Ksp=1.3×10-36;ZnS:Ksp=1.6×10-24。下列说法错误的是
| A.相同温度下,CuS的溶解度小于ZnS的溶解度 |
| B.除去工业废水中的Cu2+,可以选用FeS做沉淀剂 |
| C.足量CuSO4溶解在0.1mol/L的H2S溶液中,Cu2+能达到的最小浓度为1.3×10-35mol/L |
| D.在ZnS的饱和溶液中,加入FeCl2溶液,一定不产生FeS沉淀 |
您最近一年使用:0次
2022-09-16更新
|
153次组卷
|
2卷引用:陕西省黄陵中学2021-2022学年高二上学期期中考试化学试题
2 . 已知:AgX(X=Cl、Br)溶液中,p(Ag+)=-1gc(Ag+),p(X-)=-lgc(X-)。t℃时,p(X-)与p(Ag+)的相互关系如图。下列说法不正确的是
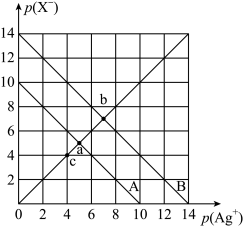

| A.A线表示的是AgBr |
| B.t℃时,c点浓度溶液中会有AgCl固体析出 |
| C.取a、b两点处溶液等体积混合,向溶液中加入足量浓硝酸银溶液,生成的沉淀n(AgBr)>n(AgCl) |
D.t℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)的平衡常数K=104 AgBr(s)+Cl-(aq)的平衡常数K=104 |
您最近一年使用:0次
解题方法
3 . 已知常温下,AgBr的Ksp=4.9×10﹣13 mol2•L﹣2、AgI的Ksp=8.3×10﹣17mol2•L﹣2。
(1)现向含有AgI的饱和溶液中:
①加入AgNO3固体,则c(I﹣)_______ (填“变大”“变小”或“不变”,下同)。
②若改加更多的AgI固体,则c(Ag+)_______ 。
③若改加AgBr固体,则c(I﹣)_______ ,c(Ag+)_______ 。
(2)现向含有NaBr、KI均为0.002mol•L﹣1的溶液中加入等体积、浓度为4×10﹣3mol•L﹣1的AgNO3溶液,则产生的沉淀是_______ (填化学式);若向其中再加入适量的NaI固体,则可发生沉淀转化的总反应的离子方程式为_______ 。
(1)现向含有AgI的饱和溶液中:
①加入AgNO3固体,则c(I﹣)
②若改加更多的AgI固体,则c(Ag+)
③若改加AgBr固体,则c(I﹣)
(2)现向含有NaBr、KI均为0.002mol•L﹣1的溶液中加入等体积、浓度为4×10﹣3mol•L﹣1的AgNO3溶液,则产生的沉淀是
您最近一年使用:0次
名校
4 . 将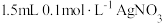 溶液和
溶液和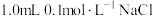 溶液混合,得到浊液a,过滤得到滤液b和白色沉淀c。已知:
溶液混合,得到浊液a,过滤得到滤液b和白色沉淀c。已知: ,
, 。下列分析错误的是
。下列分析错误的是
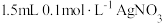 溶液和
溶液和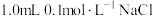 溶液混合,得到浊液a,过滤得到滤液b和白色沉淀c。已知:
溶液混合,得到浊液a,过滤得到滤液b和白色沉淀c。已知: ,
, 。下列分析错误的是
。下列分析错误的是A.浊液a中存在沉淀溶解平衡: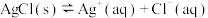 |
B.滤液b中不含 |
C.向滤液b中滴加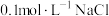 溶液,会出现白色沉淀 溶液,会出现白色沉淀 |
D.向沉淀c中滴加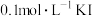 溶液,沉淀变为黄色 溶液,沉淀变为黄色 |
您最近一年使用:0次
2022-08-18更新
|
150次组卷
|
2卷引用:河北省武强中学2021-2022学年高二上学期12月联考化学试题
名校
5 . 下列用途或转化,不能用沉淀溶解平衡原理解释的是
A. 溶液可使PbS转化为CuS 溶液可使PbS转化为CuS |
B.向 饱和溶液中加入少量纯碱,有白色沉淀生成 饱和溶液中加入少量纯碱,有白色沉淀生成 |
C.Fe可除去 溶液中的 溶液中的 杂质 杂质 |
D.向 悬浊液中加入稀盐酸后,悬浊液变澄清 悬浊液中加入稀盐酸后,悬浊液变澄清 |
您最近一年使用:0次
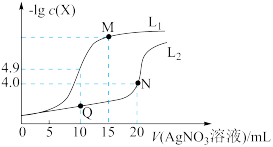
6 . t℃时,将0.1 mol·L-1AgNO3溶液分别滴加到10. 00 mL0.1 mol·L-1KCl、10.00 ml0.1 mol· L-1K2CrO4溶液中,AgNO3溶液体积(V)与-lg c(X)(X为Cl-或 )的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
 )的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
| A.曲线L2表示-lg c(Cl-)与V(AgNO3溶液)的变化关系 |
| B.t℃时,铬酸银的溶度积常数为4.0 ×10-12 |
| C.若仅将c(K2CrO4)改为0.05 mol·L-1,则曲线L2中N点移到Q点 |
D.M点溶液中:c( )>c(K+ )>c(Ag+ )>c(OH- )>c(H+ ) )>c(K+ )>c(Ag+ )>c(OH- )>c(H+ ) |
您最近一年使用:0次
2022-08-10更新
|
147次组卷
|
2卷引用:山西省怀仁市第一中学2021-2022学年高二上学期期中理科综合化学试题
名校
7 . 烟气中的 会给环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放。回答下列问题:
会给环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放。回答下列问题:
方法1(双碱法):用NaOH吸收 ,并用CaO使NaOH再生,即NaOH溶液
,并用CaO使NaOH再生,即NaOH溶液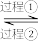
 溶液。
溶液。
(1)过程①的离子方程式为_______ 。
(2)常温下,用NaOH溶液吸收 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡_______ (填“向左”“向右”或“不”)移动。该溶液中由水电离出的
_______  ;
; 溶液显
溶液显_______ (填“酸”、“碱”或“中”)性。(常温下 的电离平衡常数
的电离平衡常数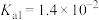 ,
, )
)
(3)CaO在水中存在如下转化: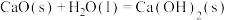 ,
,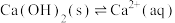
 ,从化学反应原理的角度解释过程②NaOH再生的原理:
,从化学反应原理的角度解释过程②NaOH再生的原理:_______ 。
(4)理论上,该工艺中NaOH只作为启动碱,实际主要消耗的是生石灰。实际吸收过程中,由于存在一定氧气,会发生副反应:_______ (填化学方程式),因副产物_______ (填化学式)在工艺中较难循环再生成NaOH,需要不断向系统中补充NaOH。
方法2:用氨水除去。
(5)已知常温时 的
的 ,若氨水的浓度为
,若氨水的浓度为 ,溶液中
,溶液中
_______  。将
。将 通入该氨水中,当溶液恰好呈中性时,溶液中
通入该氨水中,当溶液恰好呈中性时,溶液中
_______ 。
 会给环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放。回答下列问题:
会给环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放。回答下列问题:方法1(双碱法):用NaOH吸收
 ,并用CaO使NaOH再生,即NaOH溶液
,并用CaO使NaOH再生,即NaOH溶液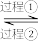
 溶液。
溶液。(1)过程①的离子方程式为
(2)常温下,用NaOH溶液吸收
 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡
 ;
; 溶液显
溶液显 的电离平衡常数
的电离平衡常数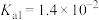 ,
, )
)(3)CaO在水中存在如下转化:
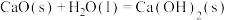 ,
,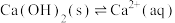
 ,从化学反应原理的角度解释过程②NaOH再生的原理:
,从化学反应原理的角度解释过程②NaOH再生的原理:(4)理论上,该工艺中NaOH只作为启动碱,实际主要消耗的是生石灰。实际吸收过程中,由于存在一定氧气,会发生副反应:
方法2:用氨水除去。
(5)已知常温时
 的
的 ,若氨水的浓度为
,若氨水的浓度为 ,溶液中
,溶液中
 。将
。将 通入该氨水中,当溶液恰好呈中性时,溶液中
通入该氨水中,当溶液恰好呈中性时,溶液中
您最近一年使用:0次
名校
8 . 在FeS悬浊液中,存在平衡FeS(s) ⇌Fe2+(aq)+S2-(aq)。欲使FeS固体质量减少,Fe2+浓度不变,可向悬浊液中加入的试剂是
| A.CuSO4溶液 | B.盐酸 | C.蒸馏水 | D.Na2S |
您最近一年使用:0次
2022-04-14更新
|
759次组卷
|
5卷引用:辽宁省沈阳市第一二〇中学2021-2022学年高二上学期第二次质量检测化学试题
辽宁省沈阳市第一二〇中学2021-2022学年高二上学期第二次质量检测化学试题四川省资阳市外国语实验学校2021-2022学年高二下学期期中考试化学试题(已下线)3.4.1 沉淀溶解平衡-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)【定心卷】3.4.1 难溶电解质的沉淀溶解平衡随堂练习-人教版2023-2024学年选择性必修1上海市华东师范大学第三附属中学2023-2024学年高二上学期期中考试(等级考) 化学试题
名校
9 .  、
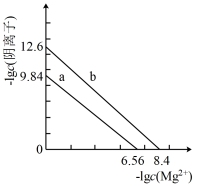
、 都是造成水体污染的因素,可以利用沉淀法除去。如图a、b分别是Mg3(AsO4)2、Mg3(PO4)2的沉淀溶解平衡曲线。下列说法错误的是
都是造成水体污染的因素,可以利用沉淀法除去。如图a、b分别是Mg3(AsO4)2、Mg3(PO4)2的沉淀溶解平衡曲线。下列说法错误的是
 、
、 都是造成水体污染的因素,可以利用沉淀法除去。如图a、b分别是Mg3(AsO4)2、Mg3(PO4)2的沉淀溶解平衡曲线。下列说法错误的是
都是造成水体污染的因素,可以利用沉淀法除去。如图a、b分别是Mg3(AsO4)2、Mg3(PO4)2的沉淀溶解平衡曲线。下列说法错误的是
| A.Ksp[Mg3(AsO4)2]=10-19.68 |
B.若Mg3(AsO4)2(s)+2 (aq) (aq) Mg3(PO4)2(s)+2 Mg3(PO4)2(s)+2 (aq)成立,则平衡常数K=104.52 (aq)成立,则平衡常数K=104.52 |
C.向浓度相等的Na3AsO4、Na3PO4的废水中同时滴加相同浓度的Mg(NO3)2溶液, 先沉淀 先沉淀 |
D.要使废水中 、 、 离子浓度不大于10-6mol·L-1,则Mg2+浓度至少为10-2.56mol·L-1 离子浓度不大于10-6mol·L-1,则Mg2+浓度至少为10-2.56mol·L-1 |
您最近一年使用:0次
10 . 已知相同温度下,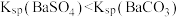 。某温度下,饱和溶液中
。某温度下,饱和溶液中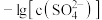 、
、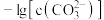 与
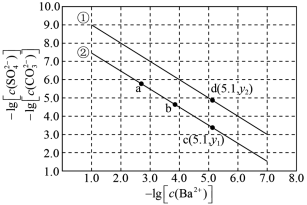
与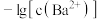 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
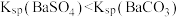 。某温度下,饱和溶液中
。某温度下,饱和溶液中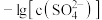 、
、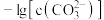 与
与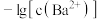 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
| A.曲线①表示硫酸钡的沉淀溶解曲线 |
B.该温度下: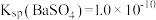 |
| C.加适量BaCl2固体可使溶液由b点变到c点 |
| D.曲线①中的y2 = 4.9 |
您最近一年使用:0次



