名校
解题方法
1 . 绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
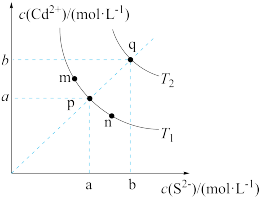
| A.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动 |
| B.图中各点对应的Ksp的关系为Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q) |
| C.图中a和b分别为T1、T2温度下CdS在水中的溶解度 |
| D.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动 |
您最近一年使用:0次
2021-03-10更新
|
319次组卷
|
2卷引用:黑龙江省大庆市铁人中学2020-2021学年高二上学期期末考试化学试题
解题方法
2 . 海洋是一个十分巨大的资源宝库,海水中含量最多的是H、O两种元素,还含有Na、Cl、Mg、Br、Ca、S等元素。海水资源的利用主要包括海水淡化、海水晒盐,从海水中制取镁、钾、溴等化工产品。从海水中提取镁的步骤是将石灰乳加入海水沉淀池中,得到氢氧化镁沉淀,再将氢氧化镁与盐酸反应,得到的溶液蒸发结晶,获得六水合氯化镁晶体(MgCl2•6H2O)进一步操作得到无水氯化镁,电解熔融氯化镁可获得单质镁。海水淡化是解决淡水资源短缺的有效途径之一,其方法主要有蒸馏法、电渗析法和离子交换法等。下列有关海水提镁的说法正确的是
| A.得到Mg(OH)2沉淀的化学反应方程式为:2NaOH+MgCl2=Mg(OH)2↓+2NaCl |
B.加入盐酸,Mg(OH)2(s) Mg2+(aq)+2OH-(aq)平衡正向移动 Mg2+(aq)+2OH-(aq)平衡正向移动 |
| C.在空气中加热灼烧MgCl2•6H2O可得到无水氯化镁 |
| D.电解熔融氯化镁时金属镁在阳极析出 |
您最近一年使用:0次
2021-02-24更新
|
413次组卷
|
2卷引用:江苏省六市(南通、淮安、泰州、徐州、镇江、宿迁)2021届高三一模化学试卷
3 . 某温度下, 的溶解平衡曲线如图,下列说法错误的是
的溶解平衡曲线如图,下列说法错误的是
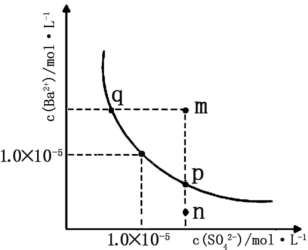
 的溶解平衡曲线如图,下列说法错误的是
的溶解平衡曲线如图,下列说法错误的是
A.该温度下 的溶度积 的溶度积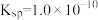 | B.m点有 沉淀析出 沉淀析出 |
C.加入 固体可使n点移动到p点 固体可使n点移动到p点 | D.升高温度可使p点移动到q点 |
您最近一年使用:0次
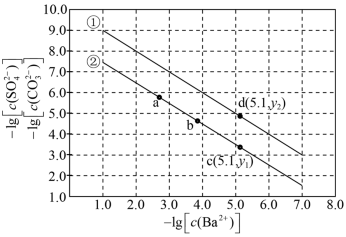
4 . 已知相同温度下,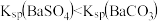 。某温度下,饱和溶液中
。某温度下,饱和溶液中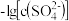 、
、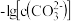 与
与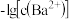 的关系如图所示。下列说法
的关系如图所示。下列说法错误 的是
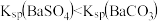 。某温度下,饱和溶液中
。某温度下,饱和溶液中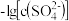 、
、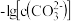 与
与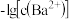 的关系如图所示。下列说法
的关系如图所示。下列说法
| A.曲线①中y2=4.9 |
B.该温度下: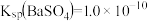 |
C.加适量 固体可使溶液由b点变到c点 固体可使溶液由b点变到c点 |
D.曲线②中a点: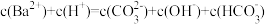 |
您最近一年使用:0次
5 . 下列有关电解质溶液的说法正确的是
| A.向0.1 mol•L-1CH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)减小 |
| B.盐酸滴定氢氧化钠的实验中,用甲基橙作指示剂时,滴定终点的pH为7 |
C.向盐酸中加入氨水至中性,溶液中c(NH )/c(Cl-)>1 )/c(Cl-)>1 |
| D.将AgCl与AgBr的饱和溶液等体积混合,再加入足量AgNO3溶液,生成的沉淀AgCl多 |
您最近一年使用:0次
6 . 室温下,通过下列实验探究NaHSO3溶液的性质:
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测定某NaHSO3溶液的pH,测得pH约为6 |
| 2 | 向某NaHSO3溶液中加入过量的Ba(OH)2溶液,产生白色沉淀 |
| 3 | 向某NaHSO3溶液中加入等体积等浓度的烧碱溶液,测得溶液pH约为9 |
| 4 | 向某苏打溶液中滴加几滴NaHSO3溶液,未观察到明显实验现象 |
A.NaHSO3溶液中存在c(OH-)=c(H+)-c(SO )+c(HSO )+c(HSO ) ) |
B.实验2反应静置后的上层清液中有c(Ba2+)×c(SO )>Ksp(BaSO3) )>Ksp(BaSO3) |
C.实验3得到的溶液中有c(Na+)=c(SO )+c(HSO )+c(HSO )+c(H2SO3) )+c(H2SO3) |
D.实验4中反应的离子方程式为CO +HSO +HSO =HCO =HCO +SO +SO |
您最近一年使用:0次
7 . 下列说法不正确的是
| A.反应MgO(s)+C(s)=Mg(s)+CO(g)在室温下不能自发进行,则该反应的∆H>0 |
| B.向有AgCl固体的饱和溶液中加少许水,c(Ag+)和Ksp(AgCl)都不变 |
C.0.1 mol·L-1CH3COOH溶液加水稀释后,溶液中 的值减小 的值减小 |
| D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去 |
您最近一年使用:0次
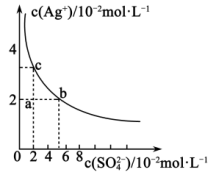
8 . 某温度下, 在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
 在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
A. 点表示 点表示 的不饱和溶液,加入 的不饱和溶液,加入 固体可能使溶液由 固体可能使溶液由 点变到 点变到 点 点 |
B. 点表示 点表示 的不饱和溶液,蒸发可以使溶液由 的不饱和溶液,蒸发可以使溶液由 点变到 点变到 点 点 |
C.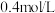 的 的 溶液与 溶液与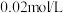 的 的 溶液等体积混合有 溶液等体积混合有 沉淀生成 沉淀生成 |
D. 的溶度积常数 的溶度积常数 为 为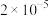 |
您最近一年使用:0次
2021-01-10更新
|
250次组卷
|
2卷引用:辽宁省沈阳市郊联体2020-2021学年高二上学期期末考试化学试题
名校
9 . 下列说法不正确的是
| A.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)⇌Mg2+(aq)+2OH-,该固体可溶于NH4Cl溶液 |
| B.向ZnS沉淀上滴加CuSO4溶液沉淀变为黑色,可推知同温下Ksp(ZnS)<Ksp(CuS) |
| C.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色,反应的离子方程式为:2AgCl(s)+S2-(aq)⇌Ag2S(s)+2Cl-(aq) |
| D.向2mL浓度均为1.2 mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01 mol·L-1的AgNO3溶液,振荡沉淀呈黄色,说明Ksp(AgCl)>Ksp(AgI) |
您最近一年使用:0次
2021-01-07更新
|
394次组卷
|
10卷引用:四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题
四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题浙江省山河联盟2021-2022学年高二上学期12月考试化学试题(已下线)3.4.2 沉淀溶解平衡原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)湖南省长沙市南雅中学2020-2021学年高二上学期第三次月考化学试题浙江省舟山市舟山中学2022-2023学年高二上学期阶段性质量监测化学试题重庆市荣昌永荣中学校2021-2022学年高二上学期期末考试化学试题河北定州中学2023-2024学年高二上学期12月月考化学试题上海市控江中学2023-2024学年高二上学期等级班阶段测验卷二 化学试题山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题山东省百师联盟2023-2024学年高二上学期12月大联考化学试题
名校
解题方法
10 . 已知t ℃时,Ksp(AgCl)=4×10-10,该温度下AgBr在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
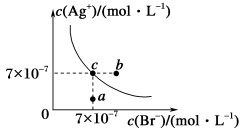

| A.图中a点对应的是t ℃时AgBr的不饱和溶液 |
| B.向AgBr饱和溶液中加入NaBr固体,可使溶液由c点变为b点 |
| C.t ℃时,AgBr的Ksp为4.9×10-13 |
D.t ℃时,AgCl(s)+Br-(aq)  AgBr(s)+Cl-(aq)的平衡常数K≈816 AgBr(s)+Cl-(aq)的平衡常数K≈816 |
您最近一年使用:0次
2021-01-06更新
|
398次组卷
|
3卷引用:福建省莆田第一中学2020-2021学年高二上学期期末考试化学试题



