室温下,通过下列实验探究NaHSO3溶液的性质:
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测定某NaHSO3溶液的pH,测得pH约为6 |
| 2 | 向某NaHSO3溶液中加入过量的Ba(OH)2溶液,产生白色沉淀 |
| 3 | 向某NaHSO3溶液中加入等体积等浓度的烧碱溶液,测得溶液pH约为9 |
| 4 | 向某苏打溶液中滴加几滴NaHSO3溶液,未观察到明显实验现象 |
A.NaHSO3溶液中存在c(OH-)=c(H+)-c(SO )+c(HSO )+c(HSO ) ) |
B.实验2反应静置后的上层清液中有c(Ba2+)×c(SO )>Ksp(BaSO3) )>Ksp(BaSO3) |
C.实验3得到的溶液中有c(Na+)=c(SO )+c(HSO )+c(HSO )+c(H2SO3) )+c(H2SO3) |
D.实验4中反应的离子方程式为CO +HSO +HSO =HCO =HCO +SO +SO |
更新时间:2021-12-23 14:58:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
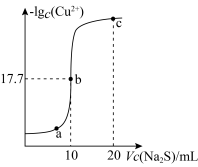
【推荐1】某温度下,向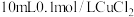 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中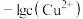 与
与 溶液体积
溶液体积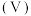 的关系如图所示,已知:
的关系如图所示,已知: ,
,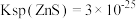
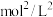 。下列有关说法正确的是
。下列有关说法正确的是
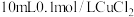 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中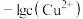 与
与 溶液体积
溶液体积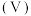 的关系如图所示,已知:
的关系如图所示,已知: ,
,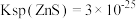
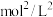 。下列有关说法正确的是
。下列有关说法正确的是 
| A.a、b、c三点中,水的电离程度最大的为b点 |
B. 溶液中: 溶液中: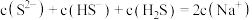 |
C.向 、 、 浓度均为 浓度均为 的混合溶液中逐滴加入 的混合溶液中逐滴加入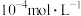 的 的 溶液, 溶液, 先沉淀 先沉淀 |
D.该温度下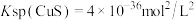 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列溶液中各微粒的浓度关系不正确 的是
| A.0.1 mol·L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) |
B.1 L 0.1 mol·L-1 CuSO4·(NH4)2SO4·6H2O的溶液中:c(SO )>c(NH )>c(NH )>c(Cu2+)>c(H+)>c(OH-) )>c(Cu2+)>c(H+)>c(OH-) |
C.0.1 mol·L-1 NaHCO3溶液中:c(H+)+c(H2CO3)=c(CO )+c(OH-) )+c(OH-) |
| D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,下列有关溶液中微粒的物质的量浓度关系正确的是
A.在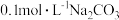 溶液中: 溶液中: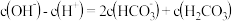 |
B.向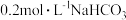 溶液中加入等体积 溶液中加入等体积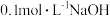 溶液: 溶液: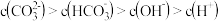 |
C. 的 的 和 和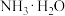 的混合溶液中: 的混合溶液中: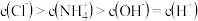 |
D.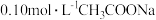 溶液中通入HCl气体至 溶液中通入HCl气体至 : : |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】二甲胺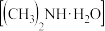 为一元弱碱,在水中的电离方式与氨相似。已知:
为一元弱碱,在水中的电离方式与氨相似。已知: 时,
时, 的电离常数
的电离常数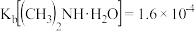 。
。 时,用
时,用 的稀硫酸滴定
的稀硫酸滴定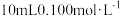 的二甲胺溶液,溶液中
的二甲胺溶液,溶液中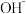 的物质的量浓度的负对数
的物质的量浓度的负对数 与所加稀硫酸的体积
与所加稀硫酸的体积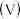 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
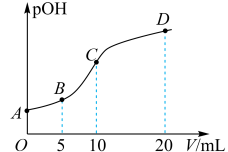
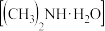 为一元弱碱,在水中的电离方式与氨相似。已知:
为一元弱碱,在水中的电离方式与氨相似。已知: 时,
时, 的电离常数
的电离常数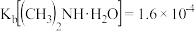 。
。 时,用
时,用 的稀硫酸滴定
的稀硫酸滴定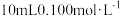 的二甲胺溶液,溶液中
的二甲胺溶液,溶液中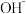 的物质的量浓度的负对数
的物质的量浓度的负对数 与所加稀硫酸的体积
与所加稀硫酸的体积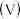 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是 
A.已知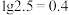 ,则A点溶液的pH约为 ,则A点溶液的pH约为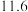 |
B.C点溶液中存在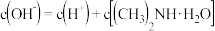 |
C.B点溶液中存在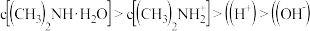 |
D.A、B、C、D四点溶液中,水电离出来的 : : |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关电解质溶液的说法正确的是
| A.向0.1 mol•L-1CH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)减小 |
| B.盐酸滴定氢氧化钠的实验中,用甲基橙作指示剂时,滴定终点的pH为7 |
C.向盐酸中加入氨水至中性,溶液中c(NH )/c(Cl-)>1 )/c(Cl-)>1 |
| D.将AgCl与AgBr的饱和溶液等体积混合,再加入足量AgNO3溶液,生成的沉淀AgCl多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列解释事实的方程式不正确 的是
A.硫酸型酸雨的形成涉及反应:2H2SO3+O2 2H2SO4 2H2SO4 |
B.SO2的水溶液显酸性:SO2+H2O  H2SO3 H2SO3 2H++ SO32- 2H++ SO32- |
C.常温下,0.1mol/L醋酸溶液pH≈3:CH3COOH CH3COO-+ H+ CH3COO-+ H+ |
| D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)⇌Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知:①AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。
②室温下,Ksp(AgCl)=2.0×10-10,Ksp(Ag2S)=2.0×10-48。
向AgCl的悬浊液中加入一定量的Na2S溶液并振荡,白色固体向黑色固体转化。下列说法正确的是
②室温下,Ksp(AgCl)=2.0×10-10,Ksp(Ag2S)=2.0×10-48。
向AgCl的悬浊液中加入一定量的Na2S溶液并振荡,白色固体向黑色固体转化。下列说法正确的是
| A.Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+2c(S2-) |
| B.向AgCl悬浊液加入足量氨水,溶液变澄清。反应的离子方程式为:AgCl+4NH3•H2O=[Ag(NH3)4]++Cl-+4H2O |
C.反应2AgCl+S2- Ag2S+2Cl-正向进行,需满足 Ag2S+2Cl-正向进行,需满足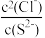 <2×1028 <2×1028 |
D.将转化后的体系静置,上层清液中离子存在关系:c(Ag+)=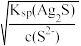 且c(Ag+)> 且c(Ag+)>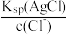 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知:pM=-lgc(Mn+ ),且假设c(Mn+)≤10-6 mol·L -1时,认为该金属离子已沉淀完全。常温下,金属离子(Mn+)浓度的负对数pM随溶液pH变化的关系如图所示。下列说法正确的是
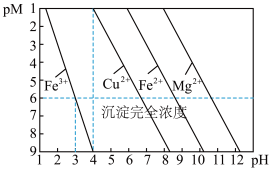

| A.常温下,Ksp[Cu(OH)2]> Ksp[Mg(OH)2] |
| B.可以通过调节溶液pH的方法分步沉淀Cu2+和Fe2+ |
| C.除去Cu2+中少量Fe3+,可控制溶液3≤pH<4 |
| D.pM与Ksp之间的关系式为pM=lgKsp- nlgc(OH- ) |
您最近一年使用:0次
【推荐2】下列图示与对应的叙述相符的是
A.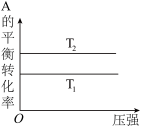 由图可以判断:若 由图可以判断:若 ,反应 ,反应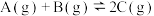 的 的 |
B.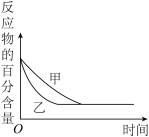 图表示压强对可逆反应 图表示压强对可逆反应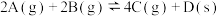 的影响,乙的压强比甲大 的影响,乙的压强比甲大 |
C.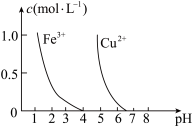 根据图,若除去 根据图,若除去 溶液中的 溶液中的 ,可向溶液中加入适量NaOH溶液,调节 ,可向溶液中加入适量NaOH溶液,调节 |
D.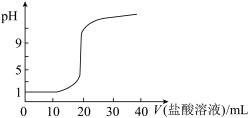 图表示用 图表示用 的盐酸滴定20mL 的盐酸滴定20mL  溶液,pH随加入盐酸体积的变化 溶液,pH随加入盐酸体积的变化 |
您最近一年使用:0次

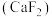 是氟元素的主要来源,可用酸浸法从矿石中提取。将过量
是氟元素的主要来源,可用酸浸法从矿石中提取。将过量 粉末置于水中得到悬浊液,再向其中通入
粉末置于水中得到悬浊液,再向其中通入 气体,发生反应:
气体,发生反应: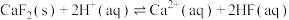 。溶液中
。溶液中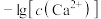 和
和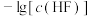 和pH的关系可用曲线X或Y表示(溶液体积变化忽略不计)。下列说法正确的是
和pH的关系可用曲线X或Y表示(溶液体积变化忽略不计)。下列说法正确的是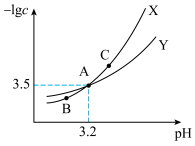
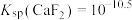
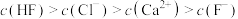

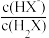 的变化关系
的变化关系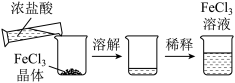 配制FeCl3溶液
配制FeCl3溶液 酯水解程度比较
酯水解程度比较 探究石灰石与稀盐酸在密闭环境下的反应
探究石灰石与稀盐酸在密闭环境下的反应 卤化银沉淀的转化
卤化银沉淀的转化

