名校
1 . 难溶电解质在水中达到沉淀溶解平衡时,下列说法中错误的是
| A.沉淀的速率和溶解的速率相等 |
| B.难溶电解质在水中形成饱和溶液 |
| C.再加入难溶电解质,溶液中各离子的浓度不变 |
| D.难溶电解质溶解形成的阴、阳离子的浓度相等 |
您最近一年使用:0次
2021-11-13更新
|
912次组卷
|
8卷引用:河南省洛阳市2021-2022学年高二上期期中考试化学试题
2 . 在t℃时,AgI在水中的沉淀溶解平衡曲线如图所示。又知t℃时AgBr的Ksp=5×10-11,下列说法不正确的是
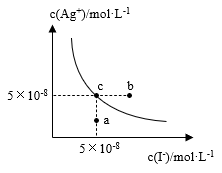

| A.在t℃时,AgI的Ksp=2.5×10-15 |
| B.图中b点有碘化银晶体析出 |
| C.向c点溶液中加入适量蒸馏水,可使溶液由c点到a点 |
D.在t℃时,反应AgBr(s)+I-(aq) AgI(s)+ Br-(aq)的平衡常数K= 20000 AgI(s)+ Br-(aq)的平衡常数K= 20000 |
您最近一年使用:0次
2021-05-27更新
|
190次组卷
|
4卷引用:河北省正中实验中学2020-2021学年高二第一学期期末考试化学试题.
名校
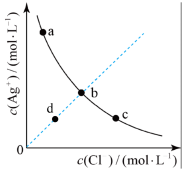
3 . 一定温度下,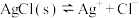 体系中,
体系中, 和
和 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
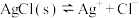 体系中,
体系中, 和
和 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.a、b、c三点对应的 相等 相等 |
| B.d点的溶液为AgCl的不饱和溶液 |
| C.向该平衡体系中加入NaCl固体,不会有AgCl沉淀析出 |
D.AgCl溶于水形成的饱和溶液中,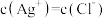 |
您最近一年使用:0次
2021-08-01更新
|
912次组卷
|
5卷引用:选择性必修1(SJ)专题3第四单元 沉淀溶解平衡
选择性必修1(SJ)专题3第四单元 沉淀溶解平衡(已下线)第3章 水溶液中的离子平衡(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)(已下线)3.4.1 难溶电解质的沉淀溶解平衡(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)3.4.1沉淀溶解平衡原理 课后云南省楚雄第一中学2022-2023学年高二下学期期末考试化学试题
解题方法
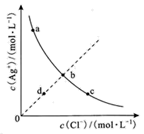
4 . 一定温度下,AgCl(s) Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl−)的关系如图所示。下列说法错误的是
Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl−)的关系如图所示。下列说法错误的是
 Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl−)的关系如图所示。下列说法错误的是
Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl−)的关系如图所示。下列说法错误的是
| A.a、b、c三点对应的Kw相等 |
| B.往d点的溶液中加入AgNO3溶液,可能会变到a点 |
| C.AgCl在a点的溶解度一定比c点的大 |
| D.该温度下,AgBr的溶解平衡曲线可能与线段bd相交 |
您最近一年使用:0次
2021-10-18更新
|
379次组卷
|
3卷引用:广东省“六校联盟”2021-2022学年高三上学期第二次联考化学试题
广东省“六校联盟”2021-2022学年高三上学期第二次联考化学试题(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)河北省衡水市第十四中学(西校区)2021-2022学年高二上学期二调考试化学试题
5 . 已知相同温度下,Ksp(BaSO4)<Ksp(BaCO3)。某温度下,饱和溶液中−lg[c(SO )]、−lg[c(CO
)]、−lg[c(CO )]与−lg[c(Ba2+)]的关系如图所示。
)]与−lg[c(Ba2+)]的关系如图所示。
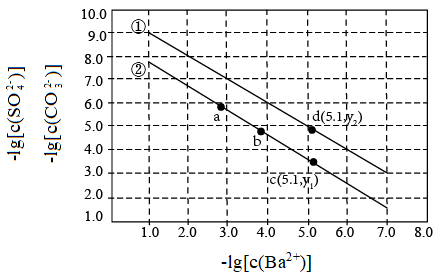
下列说法错误的是
 )]、−lg[c(CO
)]、−lg[c(CO )]与−lg[c(Ba2+)]的关系如图所示。
)]与−lg[c(Ba2+)]的关系如图所示。
下列说法错误的是
| A.曲线①中y2=4.9 |
B.曲线②中a点:2c(Ba2+)+c(H+)=2c(CO )+c(OH−)+c(HCO )+c(OH−)+c(HCO ) ) |
| C.加适量BaCl2固体可使溶液由c点变到b点 |
| D.该温度下:Ksp(BaSO4)=1.0×10—10 |
您最近一年使用:0次
6 . 铬酸银(Ag2CrO4)微溶于水。常用作分析试剂,有机合成催化剂,电镀, 卤化物滴定确定终点的指示剂等。在 t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。又知AgCl的Ksp=1.8×10−10.下列说法不正确的是


| A.t℃时,Y点和Z点时Ag2CrO4的Ksp相等 |
| B.饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点 |
| C.t℃时,Ag2CrO4的Ksp为 1×10−8 |
D.t℃时,将 0.01mol·L−1AgNO3溶液滴入20mL0.01mol·L−1KCl和 0.01mol·L−1K2CrO4的混合溶液中,CrO 先沉淀 先沉淀 |
您最近一年使用:0次
名校
解题方法
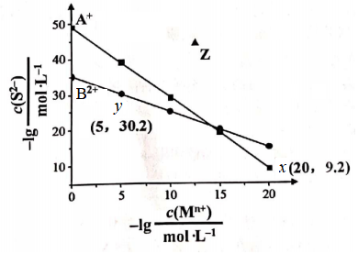
7 . 已知常温下两种难溶硫化物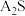 、BS在水中的沉淀溶解平衡曲线如图所示。已知阴、阳离子浓度的单位为
、BS在水中的沉淀溶解平衡曲线如图所示。已知阴、阳离子浓度的单位为 ,下列说法不正确的是
,下列说法不正确的是
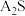 、BS在水中的沉淀溶解平衡曲线如图所示。已知阴、阳离子浓度的单位为
、BS在水中的沉淀溶解平衡曲线如图所示。已知阴、阳离子浓度的单位为 ,下列说法不正确的是
,下列说法不正确的是
A.Z点为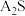 的分散系:v(沉淀)<v(溶解) 的分散系:v(沉淀)<v(溶解) |
B.向含BS沉淀的过饱和溶液中加入一定量的 固体,Ksp(BS)不变 固体,Ksp(BS)不变 |
C.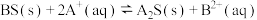 反应趋于完全 反应趋于完全 |
D. |
您最近一年使用:0次
2021-07-12更新
|
220次组卷
|
2卷引用:河南省驻马店市2020-2021学年高二下学期期末考试化学试题
名校
8 . 用Ksp表示难溶物的溶度积。下列有关沉淀溶解平衡的说法中,正确的是
| A.在AgCl的沉淀溶解平衡体系中,加入蒸馏水,Ksp增大 |
| B.在CaCO3的沉淀溶解平衡体系中,加入稀盐酸,平衡不移动 |
| C.温度升高,沉淀物的Ksp一定增大 |
| D.25℃时,Ksp(AgCl)> Ksp(AgI),向AgCl的悬浊液中加入KI固体,有黄色沉淀生成 |
您最近一年使用:0次
2021-04-16更新
|
177次组卷
|
3卷引用:河北省衡水市第十四中学2020-2021学年高二下学期一调考试化学试题
解题方法
9 . 有关电解质的说法正确的是
| A.电离常数大的酸溶液中c(H+)一定比电离常数小的酸溶液中的c(H+)大 |
B.升高CH3COONa溶液的温度,溶液中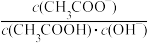 增大 增大 |
| C.0.1 mol∙L−1CH3COONa溶液和0.1 mol∙L−1NaCl溶液,前者阴离子总浓度略大 |
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中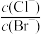 不变 不变 |
您最近一年使用:0次
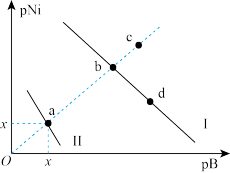
10 . 已知25℃时,Ksp(NiS)=1.0×10-21,Ksp(NiCO3)=1.0×10-7;pNi=-lgc(Ni2+),pB=-lgc(S2-)或-lgc(CO )。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液,产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法
)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液,产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误 的是
 )。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液,产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法
)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液,产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法
| A.常温下NiCO3的溶解度大于NiS的溶解度 |
| B.对于曲线I,加热b点溶液,b点向c点移动 |
| C.向d点对应的溶液中加入对应阴离子的钠盐,d点向b点移动 |
| D.x对应的值为10.5 |
您最近一年使用:0次



