名校
1 . 已知: (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
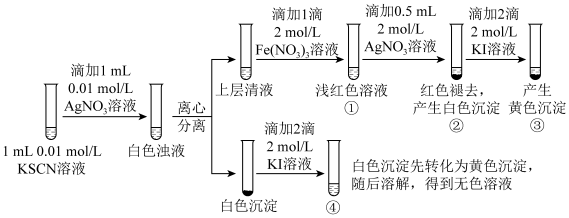
下列说法中,不正确 的是
 (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
下列说法中,
A.①中现象能说明 与 与 生成的白色浊液中存在沉淀溶解平衡 生成的白色浊液中存在沉淀溶解平衡 |
B.②中现象产生的原因是发生了反应: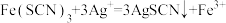 |
| C.③中产生黄色沉淀的现象能证明AgI的溶解度比AgSCN的溶解度小 |
D.④中黄色沉淀溶解的原因可能是AgI与KI溶液中的 进一步发生了反应 进一步发生了反应 |
您最近一年使用:0次
2021-11-15更新
|
697次组卷
|
3卷引用:北京市北师大附属实验中学2021-2022学年高二上学期期中考试化学试题
北京市北师大附属实验中学2021-2022学年高二上学期期中考试化学试题辽宁省大连市第八中学2021-2022学年高三上学期12月月考化学试题(已下线)第21讲 难溶电解质的沉淀溶解平衡(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
2 . 为探究Fe3+能去否除银镜反应后试管壁上银镜进行了如下实验。
(常温下溶解度:AgCl :1.9×10-4g;Ag2SO4:0.796g)
下列说法不正确的是
序号 | 操作 | 现象 |
实验① | 将2mL 2mo/L Fe(NO3)3溶液(pH=1)加入有银镜的试管中 | 银镜消失 |
实验② | 将2mL 1mol/LFe2(SO4)3溶液(pH=1)加入有银镜的试管中 | 银镜减少,未消失 |
实验③ | 将2mL 2mol/L FeCl3溶液(pH=1)加入有银镜的试管中 | 银镜消失 |
下列说法不正确的是
| A.①中可能发生反应:Fe3++Ag=Fe2++Ag+ |
| B.实验①可以证明本条件下氧化性Fe3+>Ag+ |
| C.实验②和③的试管中可能有白色沉淀生成 |
D.实验②和③现象的差异与溶液中Cl-和 有关 有关 |
您最近一年使用:0次
3 . 下列说法中,正确的是
| A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH会增大 |
B.AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl-(aq) ,往其中加入少量NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小 Ag+(aq)+Cl-(aq) ,往其中加入少量NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小 |
| C.向等浓度KCl、KI的混合溶液中,滴加AgNO3溶液,先产生黄色沉淀,证明此条件下Ksp(AgCl)>Ksp(AgI) |
D.硬水含有较多Ca2+、Mg2+、 、 、 加热煮沸可以完全除去其中的Ca2+、Mg2+ 加热煮沸可以完全除去其中的Ca2+、Mg2+ |
您最近一年使用:0次
2021-01-06更新
|
147次组卷
|
2卷引用:云南省玉溪市通海县第二中学2021-2022学年高二上学期12月月考化学试题
4 . NaNbO3是一种很好的压电和介电材料,一种以铌铁矿(主要成分为SiO2、Nb2O3、MnO2和少量的FeO、CaO、MgO)为原料的制取工艺流程如下:
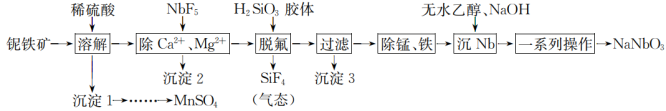
回答下列问题:
(1)为了加速“溶解”,可采取的措施有_______ (写出两种)该过程中MnO2与FeO反应生成MnSO4和Fe2(SO4)3的离子方程式为_______ 。
(2)“除Ca2+、Mg2+时,若溶液酸度过高,沉淀不完全,其原因是_______ ;当溶液中c(Ca2+)= 1×10-6mol·L-1时,溶液中c(Mg2+ )的最大值为_______ mol·L-1 (已知Ksp(CaF2)=2.5×10-11,Ksp(MgF2)= 6.4×10-9)
(3)“脱氟”过程发生反应的化学方程式为_______ 。
(4)“一系列操作”包括过滤、洗涤、干燥,其中证明NaNbO3洗涤干净的操作是_______ 。
(5)电解MnSO4溶液可制备Mn和MnO2,阳极电极反应式为_______ 。

回答下列问题:
(1)为了加速“溶解”,可采取的措施有
(2)“除Ca2+、Mg2+时,若溶液酸度过高,沉淀不完全,其原因是
(3)“脱氟”过程发生反应的化学方程式为
(4)“一系列操作”包括过滤、洗涤、干燥,其中证明NaNbO3洗涤干净的操作是
(5)电解MnSO4溶液可制备Mn和MnO2,阳极电极反应式为
您最近一年使用:0次
解题方法
5 . 下列实验操作能达到实验目的的是
| 选项 | 操作 | 目的 |
| A | 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取NaClO溶液滴于试纸的中部,与标准比色卡对比 | 测定NaClO溶液的pH |
| B | 向含有酚酞的Na2CO3溶液中滴入BaCl2溶液,观察溶液颜色的变化 | 证明Na2CO3溶液中存在水解平衡 |
| C | 在含等物质的量浓度Na2CO3、Na2SO4的混合溶液中,滴加少量BaCl2溶液 | 探究Ksp(BaCO3)和Ksp(BaSO4)的相对大小 |
| D | 将Fe(NO3)2样品溶于稀盐酸后,滴加KSCN溶液,观察溶液是否变红 | 检验Fe(NO3)2样品是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 下列操作、现象和结论都正确的是
| 操作 | 现象 | 结论 | |
| A | 在AgCl浊液中滴加少量KI稀溶液 | 产生黄色沉淀 | Ksp(AgC1)>Ksp(AgI) |
| B | 在酸性KMnO4溶液中滴加HOCH2CH=CH2(丙烯醇) | 溶液褪色 | 证明丙烯醇中含有碳碳双键 |
| C | 在NaAlO2溶液中滴加NaHCO3溶液 | 产生白色沉淀,同时有气泡产生 | 生成的气体为氢气 |
| D | 在淀粉的水解液中滴加KI溶液 | 溶液不变色 | 淀粉溶液已完全水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-08更新
|
225次组卷
|
2卷引用:河北省名校联盟2021-2022学年高三上学期一轮复习考试化学试题
解题方法
7 . 某化学实验小组探究氢氧化镁在氯化铵溶液中的溶解实验。已知:常温时,Ksp[Mg(OH)2]=4×10-12,Kb(NH3·H2O)=1.75×10-5,Ka(CH3COOH)=1.75×10-5。
I.氢氧化镁粉末的溶解
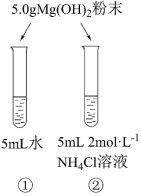
(1)常温下,实验①中有少量的氢氧化镁粉末溶解,向溶液①中滴加酚酞,溶液变为粉红色,则pH=_______ (已知:1g2=0.3)。
(2)实验②中氢氧化镁粉末大量溶解,实验②中反应的离子方程式为_______ ,此反应的平衡常数K=_______ (结果保留两位有效数字)。微热实验②中试管,有刺激性气味气体产生,检验此气体的方法为_______ 。
II.探究氢氧化镁粉末在氯化铵溶液中的溶解原因。
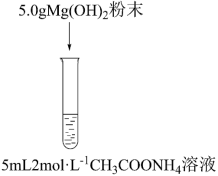
(3)猜想1:NH4Cl溶液中的NH 结合Mg(OH)2溶液中的OH-,使得溶解平衡正移。
结合Mg(OH)2溶液中的OH-,使得溶解平衡正移。
猜想2:_______ 。
将猜想2补充完整,为证明上述猜想,甲同学设计实验③,发现氢氧化镁粉末大量溶解。通过实验③可证明_______ (填“猜想1”或“猜想2”)成立。
(4)乙同学认为实验③中的CH3COO-也可能参与反应,故设计实验④证明上述结论。实验④为_______ (填实验方案)。
I.氢氧化镁粉末的溶解
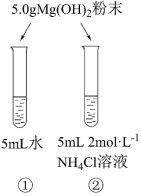
(1)常温下,实验①中有少量的氢氧化镁粉末溶解,向溶液①中滴加酚酞,溶液变为粉红色,则pH=
(2)实验②中氢氧化镁粉末大量溶解,实验②中反应的离子方程式为
II.探究氢氧化镁粉末在氯化铵溶液中的溶解原因。

(3)猜想1:NH4Cl溶液中的NH
 结合Mg(OH)2溶液中的OH-,使得溶解平衡正移。
结合Mg(OH)2溶液中的OH-,使得溶解平衡正移。猜想2:
将猜想2补充完整,为证明上述猜想,甲同学设计实验③,发现氢氧化镁粉末大量溶解。通过实验③可证明
(4)乙同学认为实验③中的CH3COO-也可能参与反应,故设计实验④证明上述结论。实验④为
您最近一年使用:0次
8 . Ⅰ.金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如图所示。
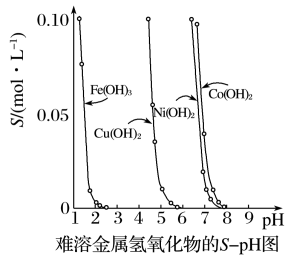
(1)pH=3时溶液中铜元素的主要存在形式是___ (写化学式)。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为___ 。
A.3左右 B.4左右 C.2左右
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,___ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是___ 。
(4)已知一些难溶物的溶度积常数如表:
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的___ 除去它们。
A.NaOH B.FeS C.Na2S
Ⅱ.某小组同学进行如图实验探究:
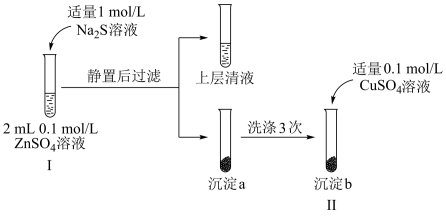
(5)预通过实验Ⅰ和实验Ⅱ证明Ksp(ZnS)<Ksp(CuS),实验Ⅰ中加入1mol•L-1Na2S的体积范围为:___ 。
(6)试管Ⅱ中观察到白色沉淀转化为黑色沉淀。请结合化学用语,从平衡移动的角度进行解释___ 。
(7)若将沉淀a洗涤3次后,加适量0.1mol/LFeSO4溶液,是否能看到白色沉淀转化为黑色沉淀,请结合计算予以说明___ 。

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.3左右 B.4左右 C.2左右
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,
(4)已知一些难溶物的溶度积常数如表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的
A.NaOH B.FeS C.Na2S
Ⅱ.某小组同学进行如图实验探究:

(5)预通过实验Ⅰ和实验Ⅱ证明Ksp(ZnS)<Ksp(CuS),实验Ⅰ中加入1mol•L-1Na2S的体积范围为:
| 难溶电解质 | 颜色 | Ksp的数值(18~25℃) |
| ZnS | 白色 | 1.6×10-24 |
| CuS | 黑色 | 1.3×10-36 |
| FeS | 黑色 | 6.3×10-18 |
(6)试管Ⅱ中观察到白色沉淀转化为黑色沉淀。请结合化学用语,从平衡移动的角度进行解释
(7)若将沉淀a洗涤3次后,加适量0.1mol/LFeSO4溶液,是否能看到白色沉淀转化为黑色沉淀,请结合计算予以说明
您最近一年使用:0次
解题方法
9 . 含钙物质在生产生活中发挥着重要作用,如 、
、 等。
等。
(1)菠菜成分测定中常用 为沉淀剂。菠菜中含有的草酸以
为沉淀剂。菠菜中含有的草酸以 、
、 、
、 存在,三种微粒之和称为总草酸。某研究小组测定菠菜中总草酸含量,进行如下实验。
存在,三种微粒之和称为总草酸。某研究小组测定菠菜中总草酸含量,进行如下实验。
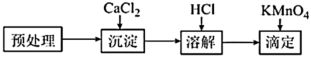
①在“预处理”步骤,将菠菜碾碎后预处理,得含总草酸的溶液( ),该步骤
),该步骤依次 需要的装置有_______ 。
②在“沉淀”步骤,调节 至溶液弱碱性,再滴加足量
至溶液弱碱性,再滴加足量 溶液,产生白色沉淀,过滤得到
溶液,产生白色沉淀,过滤得到 固体。“调节溶液至弱碱性”的目的是
固体。“调节溶液至弱碱性”的目的是_______ 。
草酸溶液中微粒的物质的量分数随溶液 变化如图所示:
变化如图所示:
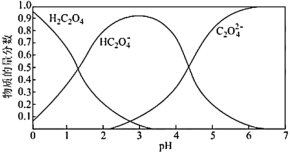
③在“溶解”步骤,稀 溶解
溶解 ,所得溶液
,所得溶液 ,该步骤主要反应的离子方程式是:
,该步骤主要反应的离子方程式是:_______ 。
④在“滴定”步骤,用 标准溶液滴定
标准溶液滴定 次,判断达到滴定终点的现象是
次,判断达到滴定终点的现象是_______ 。
(2) 的饱和石灰水,加热至
的饱和石灰水,加热至 ,发现溶液变浑浊,且加热过程中并未见水分蒸发,现探究溶液变浑浊的原因。
,发现溶液变浑浊,且加热过程中并未见水分蒸发,现探究溶液变浑浊的原因。
提出猜想。
猜想a: 的溶解度随温度升高而减小,升温的过程中析出
的溶解度随温度升高而减小,升温的过程中析出 。
。
猜想b:温度变化的过程中, 变质,使溶液变浑浊。
变质,使溶液变浑浊。
设计实验,验证猜想。
提供 下的
下的 饱和溶液Ⅰ、
饱和溶液Ⅰ、 下的
下的 饱和溶液Ⅱ。
饱和溶液Ⅱ。
①查阅资料: 时,
时,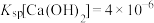 ,
,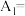
_______  。
。
②上述实验结果是 ,是否可以证明猜想a成立,
,是否可以证明猜想a成立,_______ (填“是”或“否”)。
③进一步验证猜想b,补充实验3,填写在答题卡上_______ 。
(3)实验总结。
根据实验 的结果,可以判断猜想b成立。猜想b成立的判断依据是
的结果,可以判断猜想b成立。猜想b成立的判断依据是_______ 。
 、
、 等。
等。(1)菠菜成分测定中常用
 为沉淀剂。菠菜中含有的草酸以
为沉淀剂。菠菜中含有的草酸以 、
、 、
、 存在,三种微粒之和称为总草酸。某研究小组测定菠菜中总草酸含量,进行如下实验。
存在,三种微粒之和称为总草酸。某研究小组测定菠菜中总草酸含量,进行如下实验。
①在“预处理”步骤,将菠菜碾碎后预处理,得含总草酸的溶液(
 ),该步骤
),该步骤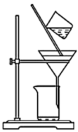 | 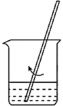 | 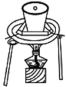 | 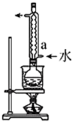 |
| A | B | C | D |
 至溶液弱碱性,再滴加足量
至溶液弱碱性,再滴加足量 溶液,产生白色沉淀,过滤得到
溶液,产生白色沉淀,过滤得到 固体。“调节溶液至弱碱性”的目的是
固体。“调节溶液至弱碱性”的目的是草酸溶液中微粒的物质的量分数随溶液
 变化如图所示:
变化如图所示:
③在“溶解”步骤,稀
 溶解
溶解 ,所得溶液
,所得溶液 ,该步骤主要反应的离子方程式是:
,该步骤主要反应的离子方程式是:④在“滴定”步骤,用
 标准溶液滴定
标准溶液滴定 次,判断达到滴定终点的现象是
次,判断达到滴定终点的现象是(2)
 的饱和石灰水,加热至
的饱和石灰水,加热至 ,发现溶液变浑浊,且加热过程中并未见水分蒸发,现探究溶液变浑浊的原因。
,发现溶液变浑浊,且加热过程中并未见水分蒸发,现探究溶液变浑浊的原因。提出猜想。
猜想a:
 的溶解度随温度升高而减小,升温的过程中析出
的溶解度随温度升高而减小,升温的过程中析出 。
。猜想b:温度变化的过程中,
 变质,使溶液变浑浊。
变质,使溶液变浑浊。设计实验,验证猜想。
提供
 下的
下的 饱和溶液Ⅰ、
饱和溶液Ⅰ、 下的
下的 饱和溶液Ⅱ。
饱和溶液Ⅱ。| 实验序号 | 试样 | 测试温度/℃ |  |
 | Ⅰ: 的 的 饱和溶液 饱和溶液 | 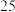 |  |
 | Ⅱ: 的 的 饱和溶液 饱和溶液 | 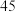 |  |
 | _______ | _______ | 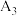 |
 时,
时,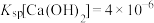 ,
,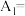
 。
。②上述实验结果是
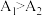 ,是否可以证明猜想a成立,
,是否可以证明猜想a成立,③进一步验证猜想b,补充实验3,填写在答题卡上
(3)实验总结。
根据实验
 的结果,可以判断猜想b成立。猜想b成立的判断依据是
的结果,可以判断猜想b成立。猜想b成立的判断依据是
您最近一年使用:0次
解题方法
10 . 下列实验操作规范且能达到目的的是
| 目的 | 操作 | |
| A | 取20.00mL盐酸 | 在50mL酸式滴定管中装入盐酸,调整初始读数为30.00mL后,将剩余盐酸放入锥形瓶 |
| B | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
| C | 测定NaClO溶液的pH | 用洁净的玻璃棒蘸取溶液点在干燥的pH试纸上 |
| D | 证明:Ksp(AgCl)>Ksp(AgI) | 在含AgNO3、AgCl的悬浊液中滴入少量NaI溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



