1 . 完成以下题目
(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe3+,提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,则Cu(OH)2开始沉淀时溶液的pH为________ ,Fe3+完全沉淀时溶液的pH为________ ,通过计算确定上述方案________ (填“可行”或“不可行”)(已知lg5=0.7)
(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe3+,提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的
| A.NaOH | B.CuO | C.NH3•H2O | D.Cu(OH)2 |
您最近一年使用:0次
名校
2 . 下列实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 在对甲基苯酚中滴少量酸性 溶液 溶液 | 证明羟基具有还原性 |
| B | 向紫色石蕊溶液中通入 至过量 至过量 | 验证 具有漂白性 具有漂白性 |
| C | 在医用酒精中加小块钠 | 证明乙醇会与钠反应 |
| D | 在AgCl浊液、AgI浊液中分别加入过量的同浓度浓氨水(白色沉淀溶解,黄色沉淀几乎不溶解) | 证明:Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-21更新
|
159次组卷
|
2卷引用:江西省部分学校2023-2024学年高三下学期二轮复习联考验收化学试卷
名校
3 . 下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 乙烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红 | 生成的有机物具有酸性 |
| B | 46 g乙醇与足量Na反应生成1 g H2 | 乙醇分子中氢氧键比碳氢键更易断裂 |
| C | 酰胺在酸或碱存在并加热时可水解 | 氨基酸有两性,能发生反应生成肽键 |
| D | FeS去除工业废水中的Hg2+、Cu2+ | FeS具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列方案设计、现象和结论正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究1-溴丁烷的消去反应 | 向圆底烧瓶中加入2.0gNaOH和15mL乙醇,搅拌,微热。将产生的气体通入酸性KMnO4溶液中 | 酸性KMnO4溶液褪色,说明1-溴丁烷发生消去反应生成1-丁烯 |
| B | 证明Ksp(CuS)<Ksp(ZnS) | 在2mL0.01mol/L的Na2S溶液中先滴入几滴0.01mol/LZnSO4溶液,再滴入0.01mol/LCuSO4溶液 | 先有白色沉淀生成,又出现黑色沉淀,说明Ksp(CuS)<Ksp(ZnS) |
| C | 探究Fe2+、Br-的还原性强弱 | 向FeBr2溶液中加入过量氯水,再加CCl4萃取 | 若CCl4层无色,则Fe2+的还原性强于Br- |
| D | 证明溴乙烷中还有溴元素 | 取少量溴乙烷与NaOH溶液共热,一段时间后,向反应液中加入足量硝酸,再滴入几滴AgNO3溶液 | 产生淡黄色沉淀,证明溴乙烷中含有溴元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 下列说法正确的是
| A.工业上常用MnS作沉淀剂除去废水中的Cu2+,证明Ksp(MnS)>Ksp(CuS) |
| B.将FeCl2溶液滴加到酸性KMnO4溶液中,紫色褪去,证明Fe2+具有还原性 |
| C.红热的炭插入浓硝酸中产生红棕色气体,证明炭与浓硝酸反应生成NO2气体 |
| D.苯、液溴与铁粉混合,生成气体通入AgNO3溶液中,若得到淡黄色沉淀则证明苯与液溴发生取代反应 |
您最近一年使用:0次
2023-02-21更新
|
267次组卷
|
2卷引用:江西省宜春市宜丰中学2022-2023学年高三下学期3月月考化学试题
6 . 化学与日常生活紧密相关,下列项目与所述化学知识的描述,有误的是
选项 | 项目 | 化学知识 |
A | 橡胶进行硫化 | 形成交联结构,增强橡胶的强度、弹性、韧性等 |
B | 酒精可用于消毒 | 酒精具有强氧化性 |
C | 氯化钙用作融雪剂 | 氯化钙溶解放热,加速冰雪的融化,且盐水凝固点比水更低 |
D | 含氟牙膏用于预防龋齿 | 牙膏中的氟化物与牙齿发生反应后,产物更难溶于水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 下列实验能达到预期目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 向溶液X中滴加浓盐酸,将产生气体通入品红溶液,溶液褪色 | 证明溶液X中含有 或 或 |
| B | 室温下,向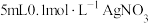 溶液中加入几滴 溶液中加入几滴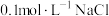 溶液出现白色沉淀,再滴加几滴 溶液出现白色沉淀,再滴加几滴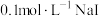 溶液,出现黄色沉淀 溶液,出现黄色沉淀 | 证明相同温度下: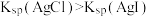 |
| C | 常温下,测得相同浓度溶液的 : : | 证明常温下的水解程度: |
| D | 将 溶液滴入酸性 溶液滴入酸性 溶液中,紫红色褪去 溶液中,紫红色褪去 | 证明 有还原性 有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-09-02更新
|
1369次组卷
|
4卷引用:江西省新余市2022-2023学年高二上学期期末质量检测化学试题
名校
解题方法
8 . 下列“实验现象”和“结论”的因果关系有错误的是。
| 选项 | 操作 | 现象 | 结论 |
| A | 相同温度下,测定等浓度的 和 和 溶液的pH 溶液的pH | 前者pH比后者大 | 非金属性:S>C |
| B | 火柴梗上滴少量的浓硫酸 | 火柴梗变黑 | 浓硫酸具有强氧化性 |
| C | 将20℃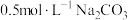 溶液加热到60℃,用pH传感器测定pH 溶液加热到60℃,用pH传感器测定pH | 溶液的pH逐渐减小 |  改变与水解平衡移动共同作用的结果 改变与水解平衡移动共同作用的结果 |
| D | 取一支试管装入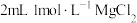 溶液,先滴加 溶液,先滴加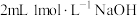 溶液,再滴加几滴 溶液,再滴加几滴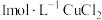 溶液 溶液 | 先生成白色沉淀,后沉淀变为蓝色 | 溶度积: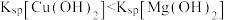 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-09更新
|
106次组卷
|
2卷引用:江西省赣州市全南中学2023-2024学年高三上学期开学考试化学试题
名校
9 . 室温下进行下列实验,根据实验操作和现象,所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 乙醇钠的水溶液呈强碱性 | C2H5O-结合H+的能力强 |
| B | 将某黄色溶液滴在KI淀粉试纸上,试纸变蓝 | 原溶液中一定含有Cl2 |
| C | 分别向等物质的量浓度的苯酚钠溶液和碳酸钠溶液中滴加酚酞,后者红色更深 | 酸性:碳酸强于苯酚 |
| D | 向盛有2mL一定浓度的Na3[Ag(S2O3)2]溶液的试管中,滴入5滴2mol•L-1的KI溶液,产生黄色沉淀 | [Ag(S2O3)2]3-具有较强的还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 实验室用绿矾(FeSO4·7H2O,M=278g/mol)制备补血剂甘氨酸亚铁[(NH2CH2COO)2Fe,M=204g/mol]。
①甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
②柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验步骤:
1.配制220mL0.800mol·L-1FeSO4溶液,取200mL于烧杯中,并向其中缓慢加入200mL2.000mol·L-1NH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀FeCO3。
ii.实验装置如图所示(夹持和加热仪器略去),将i得到的沉淀和甘氨酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。

iii.反应结束后过滤,将滤液进行蒸发浓缩,加入无水乙醇,过滤、洗涤并干燥,得到产品24.480g。
回答下列问题:
(1)配制FeSO4溶液,用到的玻璃仪器除量筒、烧杯、胶头滴管之外,还必须使用的仪器有________ 。需要用电子天平(精确到0.001g)称量绿矾________ g。
(2)实验i中生成沉淀的化学方程式为________ ,洗涤沉淀的操作是________ 。
(3)A中反应的离子方程式为________ ,表明C中空气被排尽的实验现象是________ 。
(4)C装置中加入柠檬酸溶液的作用是防止Fe2+被氧化和________ 。
(5)步骤ⅲ中加入无水乙醇的作用是________ 。
(6)该实验产率为________ 。
①甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
②柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验步骤:
1.配制220mL0.800mol·L-1FeSO4溶液,取200mL于烧杯中,并向其中缓慢加入200mL2.000mol·L-1NH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀FeCO3。
ii.实验装置如图所示(夹持和加热仪器略去),将i得到的沉淀和甘氨酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。

iii.反应结束后过滤,将滤液进行蒸发浓缩,加入无水乙醇,过滤、洗涤并干燥,得到产品24.480g。
回答下列问题:
(1)配制FeSO4溶液,用到的玻璃仪器除量筒、烧杯、胶头滴管之外,还必须使用的仪器有
(2)实验i中生成沉淀的化学方程式为
(3)A中反应的离子方程式为
(4)C装置中加入柠檬酸溶液的作用是防止Fe2+被氧化和
(5)步骤ⅲ中加入无水乙醇的作用是
(6)该实验产率为
您最近一年使用:0次



