名校
1 . 一种从废旧锂电池(主要含 ,及少量Al、Cu中制备钴酸钾(
,及少量Al、Cu中制备钴酸钾( )的工艺流程如下;
)的工艺流程如下;
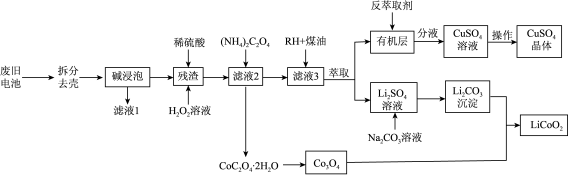
查阅资料: 具有很强的氧化性
具有很强的氧化性
(1)“碱浸泡”用来除去废旧电池中的Al,为提高该物质的去除率可采取的措施有___________ (任写一条)。
(2)向“残渣"中加入稀硫酸和 ,写出
,写出 参与反应的化学方程式
参与反应的化学方程式___________ 。
(3)向“滤液2”中加入沉淀剂时,若不采用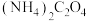 而采用
而采用 ,产物中会混有
,产物中会混有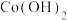 ,试分析原因
,试分析原因___________ 。
(4)RH蒸取 的原理可表示为:
的原理可表示为: 。实验室进行萃取实验用到的玻璃仪器是
。实验室进行萃取实验用到的玻璃仪器是___________ ;向有机层中加入反萃取剂___________ (填化学式)可将 反萃取至水层。
反萃取至水层。
(5)某 样品中可能含有的杂质为
样品中可能含有的杂质为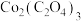 、
、 ,采用
,采用 滴定法测定该样品的组成,实验步骤如下:
滴定法测定该样品的组成,实验步骤如下:
Ⅰ.取m g样品于锥形瓶中,加入稀 溶解,水浴加热至75℃,用c
溶解,水浴加热至75℃,用c  的
的 溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗
溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗 溶液
溶液 mL。
mL。
Ⅱ.向上述溶液中加入适量还原剂将 完全还原为
完全还原为 ,加入稀
,加入稀 后,在75℃继续用c
后,在75℃继续用c 
 溶液滴定至溶液出现粉红色且30s内不褪色,又消耗
溶液滴定至溶液出现粉红色且30s内不褪色,又消耗 溶液
溶液 mL。
mL。
样品中所含 (
( )的质量分数表达式为
)的质量分数表达式为___________ 。若盛装 溶液的滴定管没有润洗,则测得样品中Co元素含量
溶液的滴定管没有润洗,则测得样品中Co元素含量___________ 。(填“偏高”、“偏低”、“无影响”)
 ,及少量Al、Cu中制备钴酸钾(
,及少量Al、Cu中制备钴酸钾( )的工艺流程如下;
)的工艺流程如下;
查阅资料:
 具有很强的氧化性
具有很强的氧化性(1)“碱浸泡”用来除去废旧电池中的Al,为提高该物质的去除率可采取的措施有
(2)向“残渣"中加入稀硫酸和
 ,写出
,写出 参与反应的化学方程式
参与反应的化学方程式(3)向“滤液2”中加入沉淀剂时,若不采用
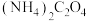 而采用
而采用 ,产物中会混有
,产物中会混有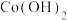 ,试分析原因
,试分析原因(4)RH蒸取
 的原理可表示为:
的原理可表示为: 。实验室进行萃取实验用到的玻璃仪器是
。实验室进行萃取实验用到的玻璃仪器是 反萃取至水层。
反萃取至水层。(5)某
 样品中可能含有的杂质为
样品中可能含有的杂质为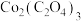 、
、 ,采用
,采用 滴定法测定该样品的组成,实验步骤如下:
滴定法测定该样品的组成,实验步骤如下:Ⅰ.取m g样品于锥形瓶中,加入稀
 溶解,水浴加热至75℃,用c
溶解,水浴加热至75℃,用c  的
的 溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗
溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗 溶液
溶液 mL。
mL。Ⅱ.向上述溶液中加入适量还原剂将
 完全还原为
完全还原为 ,加入稀
,加入稀 后,在75℃继续用c
后,在75℃继续用c 
 溶液滴定至溶液出现粉红色且30s内不褪色,又消耗
溶液滴定至溶液出现粉红色且30s内不褪色,又消耗 溶液
溶液 mL。
mL。样品中所含
 (
( )的质量分数表达式为
)的质量分数表达式为 溶液的滴定管没有润洗,则测得样品中Co元素含量
溶液的滴定管没有润洗,则测得样品中Co元素含量
您最近一年使用:0次
名校
解题方法
2 . MnO2是重要化工原料,由软锰矿制备MnO2的一种工艺流程如下:

资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH:
③该工艺条件下,MnO2与H2SO4不反应。
(1)溶出
①溶出前,软锰矿需研磨,目的是___________ 。
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:
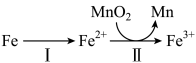
i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是___________ 。
ii.若I中Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2,而实际比值(0.9)小于2,原因是___________ 。
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2后加入NH3·H2O,调溶液pH,说明试剂加入顺序及调节pH的原因:___________ 。
(3)电解
Mn2+纯化液经电解得MnO2,生成1molMnO2电子转移的数目为___________ 。
(4)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,如热至充分反应,生成CO2,再滴加cmol/L KMnO4溶液至剩余Na2C2O4恰好完全反应,消耗KMnO4溶液的体积为dL,产品纯度为___________ (用质量分数表示)。[已知:MnO2及 均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]

资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH:
| Fe3+ | A13+ | Mn2+ | Fe2+ | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
(1)溶出
①溶出前,软锰矿需研磨,目的是
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:

i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是
ii.若I中Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2,而实际比值(0.9)小于2,原因是
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2后加入NH3·H2O,调溶液pH,说明试剂加入顺序及调节pH的原因:
(3)电解
Mn2+纯化液经电解得MnO2,生成1molMnO2电子转移的数目为
(4)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,如热至充分反应,生成CO2,再滴加cmol/L KMnO4溶液至剩余Na2C2O4恰好完全反应,消耗KMnO4溶液的体积为dL,产品纯度为
 均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
您最近一年使用:0次
2023-12-15更新
|
175次组卷
|
3卷引用:江西省上饶市广丰一中2023-2024学年高二上学期12月考试化学试卷
名校
解题方法
3 . 对电镀污泥(含Cu,Ca,Ni,Fe的氢氧化物)进行无害化和资源化处理,从其中回收金属、并制备硫酸镍的工艺流程如下图所示:
已知:氯酸不稳定,易发生歧化反应,可生成 气体。
气体。
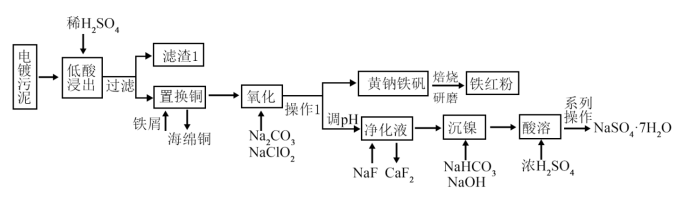
(1)“低酸浸出”工序提高浸出率的措施为___________ (只写一条即可),实验室配制500mL 1.84mol/L该低酸溶液应量取质量分数为98%,密度为 的浓硫酸
的浓硫酸___________ mL。
(2)“氧化”工序中被氧化的元素为___________ (填元素符号),“氧化”工序中加入试剂 调pH的原因为
调pH的原因为___________ (结合离子方程式解释原因),写出氧化工序生成黄钠铁矾 的离子方程式
的离子方程式___________ 。
(3)控制净化液的pH不能过低,否则会导致 沉淀不完全,原因为
沉淀不完全,原因为___________ [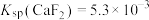 ,
,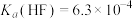 ]。
]。
(4)酸溶后的“系列操作”为___________ ,过滤、洗涤、干燥,该结晶工序得到的废液可以返回___________ 工序循环利用。
已知:氯酸不稳定,易发生歧化反应,可生成
 气体。
气体。
(1)“低酸浸出”工序提高浸出率的措施为
 的浓硫酸
的浓硫酸(2)“氧化”工序中被氧化的元素为
 调pH的原因为
调pH的原因为 的离子方程式
的离子方程式(3)控制净化液的pH不能过低,否则会导致
 沉淀不完全,原因为
沉淀不完全,原因为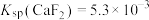 ,
,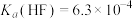 ]。
]。(4)酸溶后的“系列操作”为
您最近一年使用:0次
2021-10-17更新
|
41次组卷
|
2卷引用:江西省抚州市临川区第十中学2022届高三月考化学试卷
4 . 含锌催化剂(主要为ZnO、同时含有少量Fe、Cu、Pb等氧化物)用于合成氨工业和有机合成工业。为充分利用资源,通过如下工艺流程回收锌并制备纳米氧化锌。
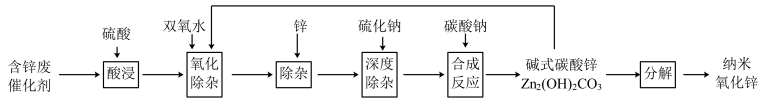
(1)90℃酸浸中,硫酸质量分数控制在30%左右,原因是___________ 。
(2)氧化除杂阶段主要是除去铁,氧化时发生的离子方程式是_______ 。调节pH发生的离子方程式为________ 。
(3)加入锌除去的杂质离子是________ ,深度除杂的目的是__________ 。
(4)由碱式碳酸锌分解得到纳米氧化锌的方法是__________ 。
(5)酸浸中,硫酸的量是理论用量的90%,硫酸不能过量的主要原因是___________ 。

(1)90℃酸浸中,硫酸质量分数控制在30%左右,原因是
(2)氧化除杂阶段主要是除去铁,氧化时发生的离子方程式是
(3)加入锌除去的杂质离子是
(4)由碱式碳酸锌分解得到纳米氧化锌的方法是
(5)酸浸中,硫酸的量是理论用量的90%,硫酸不能过量的主要原因是
您最近一年使用:0次
5 . I.通过计算回答下列有关沉淀溶解平衡的问题。
向50mL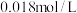 的
的 溶液中加入50mL
溶液中加入50mL 的
的 溶液,生成沉淀。已知该温度下
溶液,生成沉淀。已知该温度下 的
的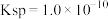 ,忽略溶液混合的体积变化,已知
,忽略溶液混合的体积变化,已知 ,请回答:
,请回答:
(1)两溶液充分混合后溶液的
_______ 。
(2)完全沉淀后,溶液中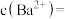
_______ 。
Ⅱ.亚氯酸钠( )常用于纺织、造纸等行业,在工业生产中十分重要,现有一份含有杂质的亚氯酸钠样品,欲测量亚氯酸钠的纯度。
)常用于纺织、造纸等行业,在工业生产中十分重要,现有一份含有杂质的亚氯酸钠样品,欲测量亚氯酸钠的纯度。
准确称取所得亚氯酸钠样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液配成250mL待测溶液。移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用cmol/L 标准溶液滴定至终点,重复2次,测得消耗
标准溶液滴定至终点,重复2次,测得消耗 标准溶液的平均值为VmL。(已知:杂质不参与反应,
标准溶液的平均值为VmL。(已知:杂质不参与反应,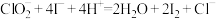 、
、 )
)
(1)达到滴定终点时的现象为_______ 。
(2)下列滴定过程中测量结果偏高的是( )
A.滴定前滴定管尖嘴有气泡,滴定终点时尖嘴气泡消失
B.滴定管用蒸馏水洗净后没有用标准液润洗
C.滴定前仰视滴定管刻度,滴定后俯视滴定管刻度
D.锥形瓶用蒸馏水洗净后未干燥
(3)该样品中 的质量分数为
的质量分数为_______ (用含m、c、V的代数式表示)。
向50mL
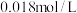 的
的 溶液中加入50mL
溶液中加入50mL 的
的 溶液,生成沉淀。已知该温度下
溶液,生成沉淀。已知该温度下 的
的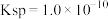 ,忽略溶液混合的体积变化,已知
,忽略溶液混合的体积变化,已知 ,请回答:
,请回答:(1)两溶液充分混合后溶液的

(2)完全沉淀后,溶液中
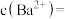
Ⅱ.亚氯酸钠(
 )常用于纺织、造纸等行业,在工业生产中十分重要,现有一份含有杂质的亚氯酸钠样品,欲测量亚氯酸钠的纯度。
)常用于纺织、造纸等行业,在工业生产中十分重要,现有一份含有杂质的亚氯酸钠样品,欲测量亚氯酸钠的纯度。准确称取所得亚氯酸钠样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液配成250mL待测溶液。移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用cmol/L
 标准溶液滴定至终点,重复2次,测得消耗
标准溶液滴定至终点,重复2次,测得消耗 标准溶液的平均值为VmL。(已知:杂质不参与反应,
标准溶液的平均值为VmL。(已知:杂质不参与反应,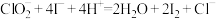 、
、 )
)(1)达到滴定终点时的现象为
(2)下列滴定过程中测量结果偏高的是
A.滴定前滴定管尖嘴有气泡,滴定终点时尖嘴气泡消失
B.滴定管用蒸馏水洗净后没有用标准液润洗
C.滴定前仰视滴定管刻度,滴定后俯视滴定管刻度
D.锥形瓶用蒸馏水洗净后未干燥
(3)该样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
名校
6 . 亚硝酰氯(ClNO)是有机物合成中的重要试剂,红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种氢化物和两种氧化物。某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度:
(1)实验室可用下图装置制备亚硝酰氯(ClNO);
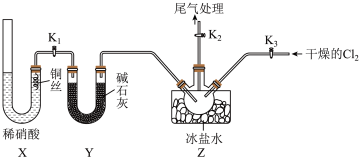
①X装置的优点为_________________________ 。
②检验装置气密性并装入药品,打开k2,然后再打开________ (填“k1”“k2”或“k3”),
通入一段时间气体,(其目的为________________________________________ ),然后进行其它操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中ClNO可能发生反应的化学方程式为__________________ 。
(2)亚硝酰氯(ClNO)的纯度测定:取Z中所得液体m g溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用c mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。(已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12),则亚硝酰氯(ClNO)的质量分数为_________ (用代数式表示)。
(1)实验室可用下图装置制备亚硝酰氯(ClNO);

①X装置的优点为
②检验装置气密性并装入药品,打开k2,然后再打开
通入一段时间气体,(其目的为
③若无装置Y,则Z中ClNO可能发生反应的化学方程式为
(2)亚硝酰氯(ClNO)的纯度测定:取Z中所得液体m g溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用c mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。(已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12),则亚硝酰氯(ClNO)的质量分数为
您最近一年使用:0次
2020-10-10更新
|
221次组卷
|
3卷引用:江西省南昌市第二中学2021届高三上学期第三次考试化学试题
名校
解题方法
7 . 以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如表。
表1.几种砷酸盐的Ksp
表2.工厂污染物排放浓度及允许排放标准
回答下列问题:
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=________ mol·L-1。
(2)写出难溶物Ca3(AsO4)2的Ksp表达式:
Ksp[Ca3(AsO4)2]=________ ,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4 mol·L-1,c(AsO43-)最大是______ mol·L-1。
(3)工厂排放出的酸性废水中的三价砷(H3AsO3为弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4为弱酸),写出该反应的离子方程式:_______________________ 。
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为__________ ;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为_______________________ 。
表1.几种砷酸盐的Ksp
| 难溶物 | Ksp | |
| Ca3(AsO4)2 | 6.8×10-19 | |
| AlAsO4 | 1.6×10-16 | |
| FeAsO4 | 5.7×10-21 | |
表2.工厂污染物排放浓度及允许排放标准
| 污染物 | H2SO4 | As |
| 浓度 | 28.42 g·L-1 | 1.6 g·L-1 |
| 排放标准 | pH 6~9 | 0.5 mg·L-1 |
回答下列问题:
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=
(2)写出难溶物Ca3(AsO4)2的Ksp表达式:
Ksp[Ca3(AsO4)2]=
(3)工厂排放出的酸性废水中的三价砷(H3AsO3为弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4为弱酸),写出该反应的离子方程式:
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为
您最近一年使用:0次
2019-12-03更新
|
182次组卷
|
7卷引用:江西赣州市2022~2023学年高二上学期期末考试化学试题
江西赣州市2022~2023学年高二上学期期末考试化学试题(已下线)2011届江苏省南通市高三第一次调研测试化学试卷(已下线)2012届江苏省阜宁、大丰、栟茶高级中学高三第二次调研联考化学试卷(已下线)2013届江苏省泗阳致远中学高三实验班第一次模拟考试化学试卷(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》安徽省太和第一中学2020-2021学年高二上学期期中考试化学(普通班)试题河南省中原名校2021-2022学年高二上学期期末联考化学试题
名校
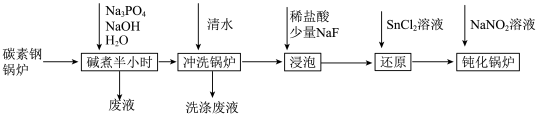
8 . 工业锅炉内壁的水垢,不仅浪费燃料,而且容易引发安全隐患。某碳素钢锅炉水垢(主要成分有CaCO3、CaSO4、Mg(OH)2、Fe2O3、SiO2等)碱煮法清除的流程如下:
已知:20℃时几种难溶物的溶度积常数如下表(单位省略):
回答下列问题:
(1)“碱煮”环节,加入Na3PO4的主要目的是将CaSO4转化为Ca3(PO4)2,请写出该离子方程式______________________ 。
(2)“浸泡过程中,稀盐酸会溶解Fe2O3。溶解后的Fe2O3会加速锅炉腐蚀,故需“还原”处理。
①锅炉被加速腐蚀的原因是______________________ ;
②浸泡液还原”处理时,Sn2+转化为Sn4+,则反应中氧化剂与还原剂的物质的量之比为______________________ 。
(3)“钝化”处理的目的是在锅炉表面形成Fe3O4保护膜,同时生成可直接参与大气循环的气体。
①反应的离子方程式为_________________________________ ;
②为检验锅炉“钝化”处理后是否形成致密的保护膜,可往锅炉内壁刷上硫酸铜溶液。若观察到______________________ (填现象),则保护膜致密性欠佳。
(4)柠檬酸(用H3R表示)可用作清除锅炉水垢的酸洗剂,溶液中H3R、H2R-、HR2-、R3-的含量与pH的关系如图所示。由此可推知,0.1 mol ·L-1 Na2HR溶液中各种阴离子浓度由大到小的排列顺序为______________________ 。

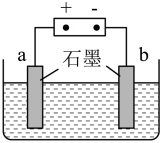
(5)用如图装置对锅炉用水(含Ca2+、Mg2+、HCO3-)进行预处理,可有效防止水垢形成。电解时,Ca2+形成沉淀的电极反应式为______________________ 。

已知:20℃时几种难溶物的溶度积常数如下表(单位省略):
| 难溶物 | CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 | Ca3(PO4)2 |
| Ksp | 2.8×10-9 | 7.1×10-5 | 5.6×10-12 | 6.8×10-6 | 2.1×10-33 |
(1)“碱煮”环节,加入Na3PO4的主要目的是将CaSO4转化为Ca3(PO4)2,请写出该离子方程式
(2)“浸泡过程中,稀盐酸会溶解Fe2O3。溶解后的Fe2O3会加速锅炉腐蚀,故需“还原”处理。
①锅炉被加速腐蚀的原因是
②浸泡液还原”处理时,Sn2+转化为Sn4+,则反应中氧化剂与还原剂的物质的量之比为
(3)“钝化”处理的目的是在锅炉表面形成Fe3O4保护膜,同时生成可直接参与大气循环的气体。
①反应的离子方程式为
②为检验锅炉“钝化”处理后是否形成致密的保护膜,可往锅炉内壁刷上硫酸铜溶液。若观察到
(4)柠檬酸(用H3R表示)可用作清除锅炉水垢的酸洗剂,溶液中H3R、H2R-、HR2-、R3-的含量与pH的关系如图所示。由此可推知,0.1 mol ·L-1 Na2HR溶液中各种阴离子浓度由大到小的排列顺序为

(5)用如图装置对锅炉用水(含Ca2+、Mg2+、HCO3-)进行预处理,可有效防止水垢形成。电解时,Ca2+形成沉淀的电极反应式为

您最近一年使用:0次
2019-03-06更新
|
1212次组卷
|
3卷引用:江西省赣州市信丰中学2020-2021学年高三上学期第五次月考化学试题
9 . 选考[化学与技术]根据废水中所含有害物质的不同,工业上有多种废水的处理方法。
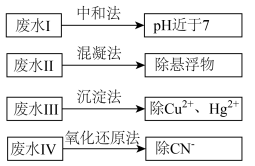
(1)废水I若采用CO2处理,离子方程式是___________ 。
(2)废水Ⅱ常用明矾处理。实践中发现废水中的c(HCO )越大,净水效果越好,这是因为
)越大,净水效果越好,这是因为___________ 。
(3)③废水Ⅲ中的汞元素存在如下转化(在空格上填相应的化学式):Hg2++___________ ═CH3Hg++___________ ;我国规定,Hg2+的排放标准不能超过0.05mg/L。对于含Hg2+的污水,可加入沉淀剂___________ (填写化学式),使Hg2+除去,降低污染。
(4)④废水Ⅳ常用Cl2氧化CN-成CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式为___________ 。
化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化剂的量,换算成氧的含量(以mg/L计)。某研究性学习小组测定某水样的化学需氧量(COD),过程如下:
Ⅰ.取V1 mL水样于锥形瓶,加入10.00mL 0.2500mol/L K2Cr2O7溶液。
Ⅱ.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热。
Ⅲ.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定。终点时消耗硫酸亚铁铵溶液V2 mL。
(5)I中,量取K2Cr2O7,溶液的仪器是___________ 。
(6)Ⅲ中,发生的反应为:Cr2O +6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=
+6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=___________ (用含c、V1、V2的表达式表示)。

(1)废水I若采用CO2处理,离子方程式是
(2)废水Ⅱ常用明矾处理。实践中发现废水中的c(HCO
 )越大,净水效果越好,这是因为
)越大,净水效果越好,这是因为(3)③废水Ⅲ中的汞元素存在如下转化(在空格上填相应的化学式):Hg2++
(4)④废水Ⅳ常用Cl2氧化CN-成CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式为
化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化剂的量,换算成氧的含量(以mg/L计)。某研究性学习小组测定某水样的化学需氧量(COD),过程如下:
Ⅰ.取V1 mL水样于锥形瓶,加入10.00mL 0.2500mol/L K2Cr2O7溶液。
Ⅱ.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热。
Ⅲ.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定。终点时消耗硫酸亚铁铵溶液V2 mL。
(5)I中,量取K2Cr2O7,溶液的仪器是
(6)Ⅲ中,发生的反应为:Cr2O
 +6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=
+6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=
您最近一年使用:0次



