1 . 工业上以铬铁矿( ,含Al,Si氧化物等杂质)为主要原料制备重铬酸钾的工艺流程如图。回答下列问题:
,含Al,Si氧化物等杂质)为主要原料制备重铬酸钾的工艺流程如图。回答下列问题: (铁、铬分别为
(铁、铬分别为 、
、 价)转化为
价)转化为 和
和 ,同时A1、Si氧化物转化为可溶性钠盐。
,同时A1、Si氧化物转化为可溶性钠盐。
(1)“焙烧”过程与 有关的化学反应中,氧化剂和还原剂物质的量之比为
有关的化学反应中,氧化剂和还原剂物质的量之比为___________ 。“浸取”过程所得滤渣的用途有___________ (合理即可)。
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度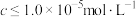 时,可认为已除尽。
时,可认为已除尽。___________ ;从平衡移动的角度解释“酸化”过程加入 的原因
的原因___________ 。
(3)“冷却结晶”时,相关化学反应方程式为___________ 。
(4) 价铬的化合物毒性较大,需将
价铬的化合物毒性较大,需将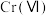 转化为毒性较低的
转化为毒性较低的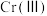 ;工业上可采用电解法处理酸性含铬废水:以铁板做阴、阳极,电解含铬(Ⅵ)废水,示意如图。
;工业上可采用电解法处理酸性含铬废水:以铁板做阴、阳极,电解含铬(Ⅵ)废水,示意如图。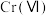 :向含铬(Ⅵ)废水中加入适量
:向含铬(Ⅵ)废水中加入适量 溶液发生反应,生成在乙醚中较稳定存在的
溶液发生反应,生成在乙醚中较稳定存在的 价的含铬氧化物
价的含铬氧化物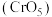 ,1mol
,1mol 中含过氧键
中含过氧键 的数量是
的数量是___________ 。
②电解开始时,A极上主要发生的电极反应式为___________ 。
③电解产生的 将
将 还原为
还原为 同时产生
同时产生 ,其离子方程式为
,其离子方程式为___________ 。
 ,含Al,Si氧化物等杂质)为主要原料制备重铬酸钾的工艺流程如图。回答下列问题:
,含Al,Si氧化物等杂质)为主要原料制备重铬酸钾的工艺流程如图。回答下列问题: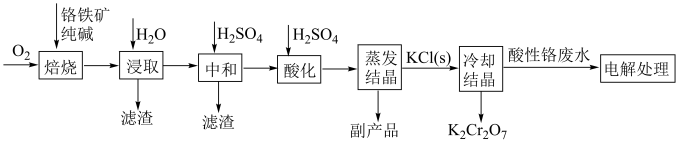
 (铁、铬分别为
(铁、铬分别为 、
、 价)转化为
价)转化为 和
和 ,同时A1、Si氧化物转化为可溶性钠盐。
,同时A1、Si氧化物转化为可溶性钠盐。(1)“焙烧”过程与
 有关的化学反应中,氧化剂和还原剂物质的量之比为
有关的化学反应中,氧化剂和还原剂物质的量之比为(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度
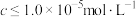 时,可认为已除尽。
时,可认为已除尽。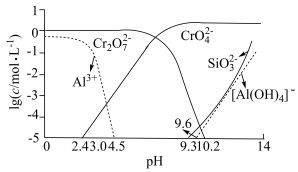
 的原因
的原因(3)“冷却结晶”时,相关化学反应方程式为
(4)
 价铬的化合物毒性较大,需将
价铬的化合物毒性较大,需将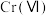 转化为毒性较低的
转化为毒性较低的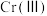 ;工业上可采用电解法处理酸性含铬废水:以铁板做阴、阳极,电解含铬(Ⅵ)废水,示意如图。
;工业上可采用电解法处理酸性含铬废水:以铁板做阴、阳极,电解含铬(Ⅵ)废水,示意如图。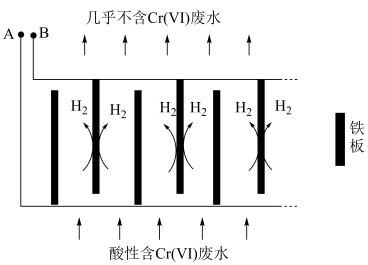
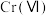 :向含铬(Ⅵ)废水中加入适量
:向含铬(Ⅵ)废水中加入适量 溶液发生反应,生成在乙醚中较稳定存在的
溶液发生反应,生成在乙醚中较稳定存在的 价的含铬氧化物
价的含铬氧化物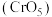 ,1mol
,1mol 中含过氧键
中含过氧键 的数量是
的数量是②电解开始时,A极上主要发生的电极反应式为
③电解产生的
 将
将 还原为
还原为 同时产生
同时产生 ,其离子方程式为
,其离子方程式为
您最近半年使用:0次
2024-04-11更新
|
270次组卷
|
2卷引用:2024届四川省雅安市、遂宁市、眉山市高三第二次诊断性考试理科综合试题-高中化学
名校
2 . 生活因化学更美好,以下生活用途和化学原理错误的是
| 选项 | 生活用途 | 化学原理 |
| A | 明矾可用作净水剂和消毒剂 | 铝离子水解生成氢氧化铝胶体 |
| B | 含氟牙膏可以预防龋齿 | 沉淀的转化 |
| C | 轮船在船壳水线以下装锌块 | 牺牲阳极法 |
| D | 泡沫灭火器可以灭火 | 盐类的水解 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 . 下列物质用途的描述正确的是
| A.明矾溶液用作铜绿去除剂,利用了其水解显酸性 |
| B.淀粉溶液用作碘量法滴定的指示剂,利用了其不饱和性 |
C. 用作除去含 用作除去含 废水的沉淀剂,利用了其还原性 废水的沉淀剂,利用了其还原性 |
D. 用作自来水的消毒剂,利用了其毒性 用作自来水的消毒剂,利用了其毒性 |
您最近半年使用:0次
名校
解题方法
4 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
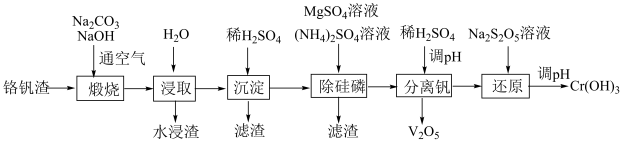
已知:最高价铬酸根在酸性介质中以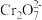 存在,在碱性介质中以
存在,在碱性介质中以 存在。
存在。
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ 。(填化学式)。
(2)水浸渣中主要有 和
和___________ 。
(3)“除硅磷”步骤中,使硅、磷分别以 和
和 的形式沉淀,该步需要控制溶液的
的形式沉淀,该步需要控制溶液的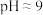 以达到最好的除杂效果,其原因是
以达到最好的除杂效果,其原因是___________ 。
(4)“还原”步骤中加入焦亚硫酸钠( )溶液。
)溶液。
①写出 还原
还原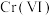 的离子方程式:
的离子方程式:___________ 。
②若用过氧化氢还原 过程中还会生成较稳定的蓝色的过氧化铬(
过程中还会生成较稳定的蓝色的过氧化铬( ,
, 为+6价)。
为+6价)。 分子中存在过氧键,其结构式可表示为
分子中存在过氧键,其结构式可表示为___________ 。
(5)为研究净水剂聚合硫酸铁 组成,某化学兴趣小组取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的
组成,某化学兴趣小组取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的 溶液,得到白色沉淀
溶液,得到白色沉淀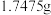 。另一份溶液,先将
。另一份溶液,先将 还原为
还原为 ,再用
,再用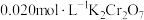 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 。求
。求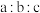 值
值___________ 。(写出计算过程)(已知: 。)
。)

已知:最高价铬酸根在酸性介质中以
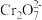 存在,在碱性介质中以
存在,在碱性介质中以 存在。
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有
 和
和(3)“除硅磷”步骤中,使硅、磷分别以
 和
和 的形式沉淀,该步需要控制溶液的
的形式沉淀,该步需要控制溶液的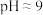 以达到最好的除杂效果,其原因是
以达到最好的除杂效果,其原因是(4)“还原”步骤中加入焦亚硫酸钠(
 )溶液。
)溶液。①写出
 还原
还原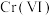 的离子方程式:
的离子方程式:②若用过氧化氢还原
 过程中还会生成较稳定的蓝色的过氧化铬(
过程中还会生成较稳定的蓝色的过氧化铬( ,
, 为+6价)。
为+6价)。 分子中存在过氧键,其结构式可表示为
分子中存在过氧键,其结构式可表示为(5)为研究净水剂聚合硫酸铁
 组成,某化学兴趣小组取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的
组成,某化学兴趣小组取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的 溶液,得到白色沉淀
溶液,得到白色沉淀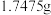 。另一份溶液,先将
。另一份溶液,先将 还原为
还原为 ,再用
,再用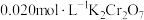 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 。求
。求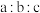 值
值 。)
。)
您最近半年使用:0次
解题方法
5 . 废旧铅蓄电池拆解获得铅膏(主要由PbSO4、PbO2、PbO形成的悬浊液),对其回收利用可减少环境污染。流程如下:

(1)“还原”步骤为了加快速率可采取的一项措施是_________________ 。该步骤PbO2发生反应的化学方程式为_________________ 。
(2)已知25℃ ,
, ,
,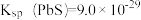 ,“脱硫”步骤选择最合适的试剂为
,“脱硫”步骤选择最合适的试剂为_________________ 。
a.(NH4)2CO3b.(NH4)2S c.NH4NO3
利用选出的脱硫试剂写出“脱硫”步骤的离子方程式________________ ;指出该步骤获得滤液的一种农业生产上的用途________________ 。
(3)“酸浸”步骤HBF4是一种强酸,试解释其酸性强于HF的原因________________ ,该步骤PbO发生反应的离子方程式为________________ 。
(4)电解时,酸度不宜过大的原因是________________ ;若电解时阳极有微量PbO2生成,写出生成PbO2的电极反应式________________ 。

(1)“还原”步骤为了加快速率可采取的一项措施是
(2)已知25℃
 ,
, ,
,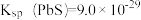 ,“脱硫”步骤选择最合适的试剂为
,“脱硫”步骤选择最合适的试剂为a.(NH4)2CO3b.(NH4)2S c.NH4NO3
利用选出的脱硫试剂写出“脱硫”步骤的离子方程式
(3)“酸浸”步骤HBF4是一种强酸,试解释其酸性强于HF的原因
(4)电解时,酸度不宜过大的原因是
您最近半年使用:0次
6 . 下列有关物质的性质和用途具有因果关系的是
| 选项 | 性质 | 用途 |
| A | 小苏打溶液呈碱性 | 小苏打常用作食品膨松剂 |
| B | Zn的金属性比Fe强 | 在轮船船体镶嵌锌块,防止轮船腐蚀 |
| C | FeS不溶于水 | 用FeS除去废水中的Hg2+ |
| D | 重金属盐可以使蛋白质变性 | 在煮沸的豆浆中加入石膏粉制豆腐 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-03-18更新
|
88次组卷
|
2卷引用:河北省石家庄市辛集中学、衡水中学2023-2024高三上学期期末联考化学试题
解题方法
7 . 某小组同学探究盐对Fe3+ +3SCN- Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。
实验I:探究KCl对Fe3+和SCN-平衡体系的影响
将已用稀盐酸酸化的0.005 mol·L-1 FeCl3溶液和0.01 mol·L-1 KSCN溶液等体积混合,静置至体系平衡,得红色溶液X,分别取3 mL溶液X放入比色皿中,分别滴加0.1 mL的试剂①~④,并测定各溶液的透光率随时间的变化,结果如图所示。
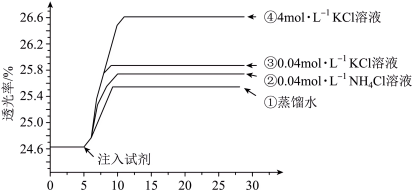
已知:i.Cl-与Fe3+能发生络合反应:Fe3+ +4C1- [FeCl4]-(黄色);
[FeCl4]-(黄色);
ii.Fe3+与NO 不能形成配位化合物;
不能形成配位化合物;
iii.溶液的透光率与溶液颜色深浅有关,颜色越深,透光率越低,忽略[FeCl4]-对透光率的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量筒、玻璃棒、容量瓶外,还需要___________ ,用稀盐酸酸化FeCl3溶液的目的是___________ 。
(2)注入试剂①后溶液透光率升高,甲同学认为是溶液稀释导致颜色变浅,乙同学认为还可能是稀释的过程中,Fe3+ +3SCN- Fe(SCN)3平衡向
Fe(SCN)3平衡向___________ (填“正”或“逆”)反应方向移动。
(3)注入试剂④后的溶液透光率比注入试剂①后高,结合平衡移动原理分析其原因___________ 。
(4)注入试剂③后的溶液透光率比注入试剂②后高,可能是___________ 导致的(答出一种影响因素即可,不需详细说明理由)。
实验II:探究不同盐对Fe3+和SCN-平衡体系的影响
取2 mL溶液X,分别加入下列试剂进行实验,一段时间后测得各溶液的透光率如下表。
(5)丙同学发现A3>A2>A1,查阅资料认为可能的原因:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。推断盐效应较强的金属阳离子为___________ (填离子符号),试分析该离子盐效应对Fe3+和SCN-平衡体系有影响的原因___________ 。
(6)拓展应用:盐效应对多种平衡体系有影响。
分析c(Na2SO4)在0~0.20 mol·L-1范围内,PbSO4溶解度发生变化的原因:___________ 。
(7)FeCl3用途十分广泛,请写出一种其在生活中的用途___________ 。
 Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。实验I:探究KCl对Fe3+和SCN-平衡体系的影响
将已用稀盐酸酸化的0.005 mol·L-1 FeCl3溶液和0.01 mol·L-1 KSCN溶液等体积混合,静置至体系平衡,得红色溶液X,分别取3 mL溶液X放入比色皿中,分别滴加0.1 mL的试剂①~④,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:i.Cl-与Fe3+能发生络合反应:Fe3+ +4C1-
 [FeCl4]-(黄色);
[FeCl4]-(黄色);ii.Fe3+与NO
 不能形成配位化合物;
不能形成配位化合物;iii.溶液的透光率与溶液颜色深浅有关,颜色越深,透光率越低,忽略[FeCl4]-对透光率的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量筒、玻璃棒、容量瓶外,还需要
(2)注入试剂①后溶液透光率升高,甲同学认为是溶液稀释导致颜色变浅,乙同学认为还可能是稀释的过程中,Fe3+ +3SCN-
 Fe(SCN)3平衡向
Fe(SCN)3平衡向(3)注入试剂④后的溶液透光率比注入试剂①后高,结合平衡移动原理分析其原因
(4)注入试剂③后的溶液透光率比注入试剂②后高,可能是
实验II:探究不同盐对Fe3+和SCN-平衡体系的影响
取2 mL溶液X,分别加入下列试剂进行实验,一段时间后测得各溶液的透光率如下表。
| 序号 | 加入试剂 | 溶液透光率 |
| 1 | 1 mL蒸馏水 | A1 |
| 2 | 1 mL 3 mol·L-1 KNO3 | A2 |
| 3 | 1 mL 3 mol·L-1 NaNO3 | A3 |
(5)丙同学发现A3>A2>A1,查阅资料认为可能的原因:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。推断盐效应较强的金属阳离子为
(6)拓展应用:盐效应对多种平衡体系有影响。
| c(Na2SO4)/(mol·L-1) | 0 | 0.01 | 0.02 | 0.04 | 0.10 | 0.20 |
| PbSO4溶解度/mg | 4.5 | 0.48 | 0.42 | 0.39 | 0.48 | 0.69 |
(7)FeCl3用途十分广泛,请写出一种其在生活中的用途
您最近半年使用:0次
2024高三·全国·专题练习
8 . 下列物质性质、用途描述正确的是
| A.利用Cu(OH)2的氧化性,检测“糖尿”中的葡萄糖 |
| B.利用FeS的还原性,将废水中的Cu2+转化为沉淀 |
| C.利用Cl2的漂白性,除去废水中的色素 |
| D.利用Na的还原性,用作核反应堆的传热介质 |
您最近半年使用:0次
解题方法
9 . 生活因化学更美好,以下生活用途和化学原理错误的是
选项 | 生活用途 | 化学原理 |
| A | 明矾可用作净水剂和消毒剂 | 铝离子水解生成氢氧化铝胶体 |
| B | 含氟牙膏可以预防龋齿 | 沉淀的转化 |
| C | 电热水器内胆连接镁棒防止腐蚀 | 牺牲阳极法 |
| D | 泡沫灭火器可以灭火 | 盐类的水解 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
10 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅等的氧化物,从铬钒渣中分离提取铬和钒的一种流程如图所示。下列说法正确的是
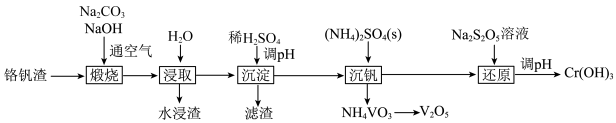
已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
② 。
。

已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
②
 。
。A.“煅烧”后的含铬化合物是 |
B.“滤渣”中只含有 |
C.“沉钒”时 固体可增大 固体可增大 的浓度,有利于沉淀的生成 的浓度,有利于沉淀的生成 |
D.“还原”工序中氧化剂和还原剂的物质的量之比为 |
您最近半年使用:0次
2023-12-03更新
|
366次组卷
|
2卷引用:山东省菏泽市2023-2024学年高三上学期期中化学试题



