1 . 下列有关物质的性质与用途具有对应关系的是
| A.油脂在酸性条件下水解,可用于制肥皂 |
| B.茶多酚有氧化性,可作食品保鲜剂 |
C. 溶液呈酸性,可用于去除铁锈 溶液呈酸性,可用于去除铁锈 |
D. ,可用饱和 ,可用饱和 溶液将水垢中的 溶液将水垢中的 转化为 转化为 |
您最近半年使用:0次
名校
解题方法
2 . 表中实验操作、现象与结论对应关系均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 等体积pH=2的两种酸HX和HY分别与足量的锌反应 | HX溶液中放出的H2多 | HX的酸性比HY强 |
| B | 用广泛pH试纸测定1mol/LNaHSO3溶液的酸碱性 | 测得pH=3.2 | NaHSO3溶液呈酸性,证明HSO 在水中的电离程度小于水解程度 在水中的电离程度小于水解程度 |
| C | 在KSCN与FeCl3的混合液中再加入KCl固体 | 溶液颜色变浅 | 增大生成物浓度,平衡逆向移动 |
| D | 向浓度均为0.1mol/L的NaCl和NaI的混合溶液中滴加少量0.1mol/L的AgNO3溶液 | 产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-03-16更新
|
675次组卷
|
8卷引用:湖南省永州市宁远县第一中学2022-2023学年高二上学期期中考试化学试题
湖南省永州市宁远县第一中学2022-2023学年高二上学期期中考试化学试题广东省江门市培英高级中学2022-2023学年高二上学期期中考试化学试题广东省梅州市兴宁市沐彬中学2021-2022学年高二下学期期中考试化学试题辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校五校协作体2020-2021学年高二上学期期末化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期期末考试化学试题江西省临川第二中学2022-2023学年高二上学期第三次月考化学试题湖南省衡阳县2022-2023学年高二上学期期末考试化学试题江西省宜春市宜丰中学2023-2024学年高二上学期10月月考化学试题
3 . 下列物质用途的描述正确的是
| A.明矾溶液用作铜绿去除剂,利用了其水解显酸性 |
| B.淀粉溶液用作碘量法滴定的指示剂,利用了其不饱和性 |
C. 用作除去含 用作除去含 废水的沉淀剂,利用了其还原性 废水的沉淀剂,利用了其还原性 |
D. 用作自来水的消毒剂,利用了其毒性 用作自来水的消毒剂,利用了其毒性 |
您最近半年使用:0次
名校
解题方法
4 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅等的氧化物,从铬钒渣中分离提取铬和钒的一种流程如图所示。下列说法正确的是
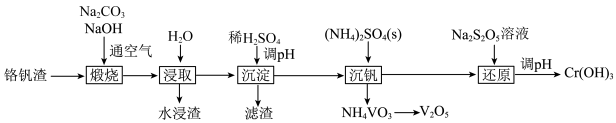
已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
② 。
。

已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
②
 。
。A.“煅烧”后的含铬化合物是 |
B.“滤渣”中只含有 |
C.“沉钒”时 固体可增大 固体可增大 的浓度,有利于沉淀的生成 的浓度,有利于沉淀的生成 |
D.“还原”工序中氧化剂和还原剂的物质的量之比为 |
您最近半年使用:0次
2023-12-03更新
|
366次组卷
|
2卷引用:山东省菏泽市2023-2024学年高三上学期期中化学试题
名校
5 . 下列物质的用途或事实与盐类的水解无关的是
A.用 溶液处理锅炉水垢中的 溶液处理锅炉水垢中的 |
B.明矾[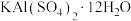 ]用于净水 ]用于净水 |
C.用热饱和 溶液清洗试管壁上附着的植物油 溶液清洗试管壁上附着的植物油 |
D.由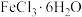 制取无水 制取无水 固体时,需在HCl气流中蒸发 固体时,需在HCl气流中蒸发 |
您最近半年使用:0次
2023-11-29更新
|
311次组卷
|
3卷引用:北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题
名校
6 . 盐类的水解在生产、生活中应用广泛。下列物质的用途与盐类水解无关 的是
A. 溶液用于除去铁锈 溶液用于除去铁锈 |
B. 溶液用作泡沫灭火剂原料 溶液用作泡沫灭火剂原料 |
C. 溶液用于吸收工业废气中的 溶液用于吸收工业废气中的 |
D. 溶液用于处理锅炉中的 溶液用于处理锅炉中的 水垢 水垢 |
您最近半年使用:0次
2023-06-28更新
|
142次组卷
|
2卷引用:江苏省镇江第一中学2023-2024学年高二上学期期中考试化学试题
7 . 草酸钴用途广泛,可用于指示剂和催化剂制备。一种利用水钴矿[主要成分为 ,含少量
,含少量 、
、 、
、 、
、 、
、 等]制取
等]制取 工艺流程如下:
工艺流程如下: 、
、 、
、 、
、 、
、 、
、 、
、 等;
等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)浸出过程中加入 的目的是将
的目的是将__________ 还原(填离子符号)。
(2) 在浸出液中发生反应的离子方程式为
在浸出液中发生反应的离子方程式为___________ 。若不慎加入过量 ,可能会生成有毒气体是
,可能会生成有毒气体是__________ (写化学式)。
(3)加 能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除
能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除 外,还有的成分是
外,还有的成分是__________ (填化学式),试用离子方程式和必要的文字简述其原理:________________ 。
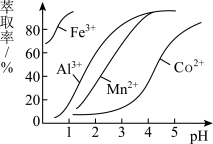
(4)萃取剂对金属离子的萃取率与pH的关系如图所示。滤液II中加入萃取剂的作用是__________ ;使用萃取剂适宜的
__________ (填序号)左右:
(5)滤液I“除钙、镁”是将溶液中 与
与 转化为
转化为 、
、 沉淀。已知
沉淀。已知 、
、 。当加入过量NaF后,所得滤液
。当加入过量NaF后,所得滤液
__________ 。
 ,含少量
,含少量 、
、 、
、 、
、 、
、 等]制取
等]制取 工艺流程如下:
工艺流程如下: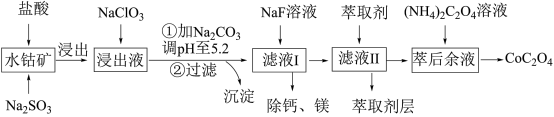
 、
、 、
、 、
、 、
、 、
、 、
、 等;
等;②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 |
|
|
|
|
|
完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入
 的目的是将
的目的是将(2)
 在浸出液中发生反应的离子方程式为
在浸出液中发生反应的离子方程式为 ,可能会生成有毒气体是
,可能会生成有毒气体是(3)加
 能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除
能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除 外,还有的成分是
外,还有的成分是(4)萃取剂对金属离子的萃取率与pH的关系如图所示。滤液II中加入萃取剂的作用是

(5)滤液I“除钙、镁”是将溶液中
 与
与 转化为
转化为 、
、 沉淀。已知
沉淀。已知 、
、 。当加入过量NaF后,所得滤液
。当加入过量NaF后,所得滤液
您最近半年使用:0次
解题方法
8 . Na2CO3和NaHCO3是中学化学中常见的物质,在生产生活中有重要的用途。
(1)常温下,0.1 mol·L-1碳酸钠溶液pH约为12,原因是_______ (用离子方程式表示)。
(2)若在FeCl3溶液中加入碳酸氢钠浓溶液,观察到红褐色沉淀和无色气体,用离子方程式解释产生该现象的原因_______ 。
(3)工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3,再经过处理最终得到Pb。
①PbCO3的溶解度_______ (填“大于”或“小于”)PbSO4。
②用离子方程式解释Na2CO3的作用:_______ 。
③用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,Na2CO3溶液中的PbSO4转化率较大,请解释其中的原因_______ 。
(1)常温下,0.1 mol·L-1碳酸钠溶液pH约为12,原因是
(2)若在FeCl3溶液中加入碳酸氢钠浓溶液,观察到红褐色沉淀和无色气体,用离子方程式解释产生该现象的原因
(3)工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3,再经过处理最终得到Pb。
①PbCO3的溶解度
②用离子方程式解释Na2CO3的作用:
③用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,Na2CO3溶液中的PbSO4转化率较大,请解释其中的原因
您最近半年使用:0次
名校
解题方法
9 . 将黄铁矿(主要成分 ,含杂质
,含杂质 等)在空气中焙烧,产生红渣以及气体a,再经过一系列处理制备铵铁蓝
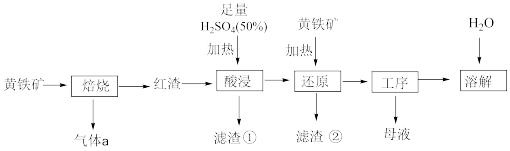
等)在空气中焙烧,产生红渣以及气体a,再经过一系列处理制备铵铁蓝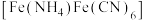 颜料,工艺流程如下:
颜料,工艺流程如下:

已知: 不与
不与 反应。
反应。
(1)写出黄铁矿焙烧的化学方程式___________ ;为提高焙烧的效率,可以采取的措施为___________ 。
A.进一步粉碎矿石 B.通入适当过量的空气 C.降低焙烧的温度
写出气体a的一种用途___________ 。
(2)在“还原”过程中,不会生成S单质,写出该过程中反应的离子方程式___________ 。
(3)在“沉铁”过程中会产生白色沉淀 ,该物质中
,该物质中 的化合价为
的化合价为___________ ,则“氧化”过程中加入 的作用是
的作用是___________ 。
(4) 用作油漆、涂料等的红色颜料,若用“还原”过程中得到的滤液制备
用作油漆、涂料等的红色颜料,若用“还原”过程中得到的滤液制备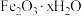 和
和 ,所加的物质为
,所加的物质为___________ 和___________ (填化学式,不引入新的杂质)。
(5)在“洗涤”过程中检验沉淀是否洗涤干净的方法是___________ 。
 ,含杂质
,含杂质 等)在空气中焙烧,产生红渣以及气体a,再经过一系列处理制备铵铁蓝
等)在空气中焙烧,产生红渣以及气体a,再经过一系列处理制备铵铁蓝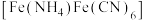 颜料,工艺流程如下:
颜料,工艺流程如下:

已知:
 不与
不与 反应。
反应。(1)写出黄铁矿焙烧的化学方程式
A.进一步粉碎矿石 B.通入适当过量的空气 C.降低焙烧的温度
写出气体a的一种用途
(2)在“还原”过程中,不会生成S单质,写出该过程中反应的离子方程式
(3)在“沉铁”过程中会产生白色沉淀
 ,该物质中
,该物质中 的化合价为
的化合价为 的作用是
的作用是(4)
 用作油漆、涂料等的红色颜料,若用“还原”过程中得到的滤液制备
用作油漆、涂料等的红色颜料,若用“还原”过程中得到的滤液制备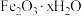 和
和 ,所加的物质为
,所加的物质为(5)在“洗涤”过程中检验沉淀是否洗涤干净的方法是
您最近半年使用:0次
名校
解题方法
10 . 铬及其化合物在生产生活中具有十分广泛的用途。工业上以铬铁矿[主要成分是 ,Cr元素为+3价,含少量
,Cr元素为+3价,含少量 、
、 、
、 等杂质]为原料制取铬酸钠(
等杂质]为原料制取铬酸钠( )晶体,其工艺流程如图:
)晶体,其工艺流程如图:

已知:+3价Cr在酸性溶液中性质稳定,当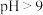 时以
时以 形式存在且易被氧化。
形式存在且易被氧化。
(1)如 可写成
可写成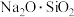 ,则
,则 可写成
可写成_______ 。
(2)若省略“过滤2”步骤,产品中可能混有_______ (写化学式)。
(3)流程中两次使用了 进行氧化,第二次氧化时反应的离子方程式为
进行氧化,第二次氧化时反应的离子方程式为_______ 。
(4)制取铬酸钠后的酸性废水中含有 ,必须经过处理与净化才能排放。在废水中加入焦炭和铁屑,与酸性
,必须经过处理与净化才能排放。在废水中加入焦炭和铁屑,与酸性 溶液形成原电池,使
溶液形成原电池,使 转化为
转化为 ,再用石灰乳对
,再用石灰乳对 进行沉降,该电池的正极反应式为
进行沉降,该电池的正极反应式为_______ ,沉降 的离子方程式为
的离子方程式为_______ 。
(5)金属铬在溶液中有多种存在形式, 和
和 在溶液中可相互转化。室温下,初始浓度为
在溶液中可相互转化。室温下,初始浓度为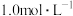 的
的 溶液中
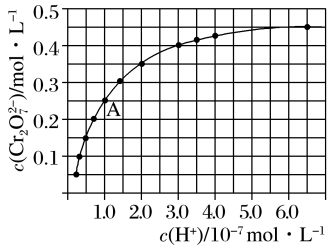
溶液中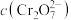 随
随 的变化如图所示,用离子方程式表示
的变化如图所示,用离子方程式表示 溶液中的转化反应
溶液中的转化反应_______ ,根据A点数据计算出该转化反应的平衡常数为_______ ,温度升高,溶液中 的平衡转化率减小,则该反应的
的平衡转化率减小,则该反应的
_______ (填“>”“<”或“=”)0。
 ,Cr元素为+3价,含少量
,Cr元素为+3价,含少量 、
、 、
、 等杂质]为原料制取铬酸钠(
等杂质]为原料制取铬酸钠( )晶体,其工艺流程如图:
)晶体,其工艺流程如图:
已知:+3价Cr在酸性溶液中性质稳定,当
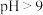 时以
时以 形式存在且易被氧化。
形式存在且易被氧化。(1)如
 可写成
可写成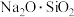 ,则
,则 可写成
可写成(2)若省略“过滤2”步骤,产品中可能混有
(3)流程中两次使用了
 进行氧化,第二次氧化时反应的离子方程式为
进行氧化,第二次氧化时反应的离子方程式为(4)制取铬酸钠后的酸性废水中含有
 ,必须经过处理与净化才能排放。在废水中加入焦炭和铁屑,与酸性
,必须经过处理与净化才能排放。在废水中加入焦炭和铁屑,与酸性 溶液形成原电池,使
溶液形成原电池,使 转化为
转化为 ,再用石灰乳对
,再用石灰乳对 进行沉降,该电池的正极反应式为
进行沉降,该电池的正极反应式为 的离子方程式为
的离子方程式为(5)金属铬在溶液中有多种存在形式,
 和
和 在溶液中可相互转化。室温下,初始浓度为
在溶液中可相互转化。室温下,初始浓度为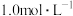 的
的 溶液中
溶液中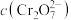 随
随 的变化如图所示,用离子方程式表示
的变化如图所示,用离子方程式表示 溶液中的转化反应
溶液中的转化反应 的平衡转化率减小,则该反应的
的平衡转化率减小,则该反应的

您最近半年使用:0次
2022-12-16更新
|
271次组卷
|
2卷引用:辽宁省大连市滨城联盟2022-2023学年高三上学期期中(‖)考试化学试题







