Na2CO3和NaHCO3是中学化学中常见的物质,在生产生活中有重要的用途。
(1)常温下,0.1 mol·L-1碳酸钠溶液pH约为12,原因是_______ (用离子方程式表示)。
(2)若在FeCl3溶液中加入碳酸氢钠浓溶液,观察到红褐色沉淀和无色气体,用离子方程式解释产生该现象的原因_______ 。
(3)工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3,再经过处理最终得到Pb。
①PbCO3的溶解度_______ (填“大于”或“小于”)PbSO4。
②用离子方程式解释Na2CO3的作用:_______ 。
③用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,Na2CO3溶液中的PbSO4转化率较大,请解释其中的原因_______ 。
(1)常温下,0.1 mol·L-1碳酸钠溶液pH约为12,原因是
(2)若在FeCl3溶液中加入碳酸氢钠浓溶液,观察到红褐色沉淀和无色气体,用离子方程式解释产生该现象的原因
(3)工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3,再经过处理最终得到Pb。
①PbCO3的溶解度
②用离子方程式解释Na2CO3的作用:
③用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,Na2CO3溶液中的PbSO4转化率较大,请解释其中的原因
更新时间:2022-10-26 15:19:56
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】冷冻氨碳捕集技术,要先用氨吸收CO2生成盐,然后在高温下使CO2再生。
吸收CO2的主要化学反应:
2NH3(aq)+CO2(g)+H2O(l) (NH4)2CO3(aq)+99.3kJ
(NH4)2CO3(aq)+99.3kJ
NH3(aq)+CO2(g)+H2O(l) NH4HCO3(aq)+26.4kJ
NH4HCO3(aq)+26.4kJ
2NH3(aq)+CO2(g) NH2COONH4(aq)+135.9kJ
NH2COONH4(aq)+135.9kJ
(1)吸收CO2时宜选用___________ ,(选填“低温”或“高温”)理由___________ 、___________ 。(列举两点)
再生的CO2可直接用于合成乙醇。
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g)
CH3CH2OH(g)+3H2O(g)
(2)该反应的化学平衡常数表达式K=___________ 。
(3)在恒温恒容的密闭容器中反应,可以判断已达平衡状态的是___________ 。(选填编号)
a.2v(CO2)正=3v(H2O)逆
b.容器中总压强不变
c.容器中混合气体的密度不变
d.容器中CO2的体积分数不变
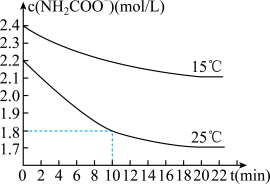
干燥的NH3和CO2可生成较纯净的氨基甲酸铵(NH2COONH4),氨基甲酸铵易水解,产物是碳酸氢铵和一种弱碱。取二份氨基甲酸铵溶液,测定15℃、25℃时水解反应速率,得到c(NH2COO﹣)随时间变化趋势如图所示。
(4)写出氨基甲酸铵水解的离子方程式___________ 。
(5)根据图中信息回答:25℃,0~10min内NH2COO﹣的平均水解速率v(NH2COO﹣)=___________ 。判断NH2COO﹣的水解速率随温度升高而增大的理由是___________ 。
吸收CO2的主要化学反应:
2NH3(aq)+CO2(g)+H2O(l)
 (NH4)2CO3(aq)+99.3kJ
(NH4)2CO3(aq)+99.3kJNH3(aq)+CO2(g)+H2O(l)
 NH4HCO3(aq)+26.4kJ
NH4HCO3(aq)+26.4kJ2NH3(aq)+CO2(g)
 NH2COONH4(aq)+135.9kJ
NH2COONH4(aq)+135.9kJ(1)吸收CO2时宜选用
再生的CO2可直接用于合成乙醇。
2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(g)
CH3CH2OH(g)+3H2O(g)(2)该反应的化学平衡常数表达式K=
(3)在恒温恒容的密闭容器中反应,可以判断已达平衡状态的是
a.2v(CO2)正=3v(H2O)逆
b.容器中总压强不变
c.容器中混合气体的密度不变
d.容器中CO2的体积分数不变
干燥的NH3和CO2可生成较纯净的氨基甲酸铵(NH2COONH4),氨基甲酸铵易水解,产物是碳酸氢铵和一种弱碱。取二份氨基甲酸铵溶液,测定15℃、25℃时水解反应速率,得到c(NH2COO﹣)随时间变化趋势如图所示。

(4)写出氨基甲酸铵水解的离子方程式
(5)根据图中信息回答:25℃,0~10min内NH2COO﹣的平均水解速率v(NH2COO﹣)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】10 ℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
甲同学认为,该溶液的pH升高的原因是 的水解程度增大,故碱性增强,该反应的离子方程式为
的水解程度增大,故碱性增强,该反应的离子方程式为 +H2O
+H2O H2CO3+OH-。
H2CO3+OH-。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于NaHCO3。
丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则_______ (填“甲”或“乙”)判断正确。试剂X是_______ 。
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10 ℃,若溶液的pH___________ (填“高于”“低于”或“等于”)8.3,则___________ (填“甲”或“乙”)判断正确。
(3)查阅资料,发现NaHCO3的分解温度为150 ℃,丙断言_______ (填“甲”或“乙”)判断是错误的,理由是___________ 。
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50 ℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
 的水解程度增大,故碱性增强,该反应的离子方程式为
的水解程度增大,故碱性增强,该反应的离子方程式为 +H2O
+H2O H2CO3+OH-。
H2CO3+OH-。乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于NaHCO3。
丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10 ℃,若溶液的pH
(3)查阅资料,发现NaHCO3的分解温度为150 ℃,丙断言
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】已知:25℃时, 、
、 、
、 。
。
(1)常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:

①曲线I代表___________ 溶液(填“ ”或“
”或“ ”)。
”)。
②a、b两点对应的溶液中,水的电离程度a___________ b(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
③向上述 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
___________  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
④酸度( )也可表示溶液的酸碱性,。
)也可表示溶液的酸碱性,。 。常温下,
。常温下, 的硝酸溶液
的硝酸溶液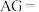
___________ 。
(2)25℃时,往 溶液中加入
溶液中加入 溶液。
溶液。
①当 ,生成
,生成 ,
, 水解的离子方程式为
水解的离子方程式为___________ 。
②当 ,溶液显
,溶液显___________ 性(填“酸”、“碱”或“中”),原因是___________ (结合数据计算说明)。
③等浓度等体积的 、
、 混合,溶液中
混合,溶液中
___________ 。
 、
、 、
、 。
。(1)常温下,将pH和体积均相同的
 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
①曲线I代表
 ”或“
”或“ ”)。
”)。②a、b两点对应的溶液中,水的电离程度a
 ”、“
”、“ ”或“
”或“ ”)。
”)。③向上述
 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。④酸度(
 )也可表示溶液的酸碱性,。
)也可表示溶液的酸碱性,。 。常温下,
。常温下, 的硝酸溶液
的硝酸溶液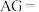
(2)25℃时,往
 溶液中加入
溶液中加入 溶液。
溶液。①当
 ,生成
,生成 ,
, 水解的离子方程式为
水解的离子方程式为②当
 ,溶液显
,溶液显③等浓度等体积的
 、
、 混合,溶液中
混合,溶液中
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】以含锂电解铝废渣(主要含 AlF3、 NaF、LiF、CaO ) 和浓硫酸为原料,制备电池级碳酸锂,同时得副产品冰晶石,其工艺流程如下:
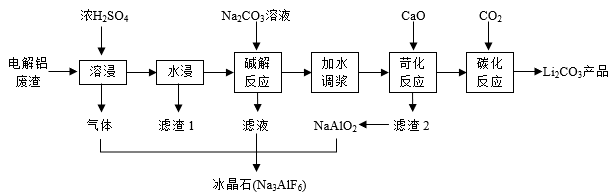
已知 LiOH 易溶于水,Li2CO3微溶于水。回答下列问题:
(1)电解铝废渣与浓硫酸反应产生的气体化学式为_________________ 。滤渣 2 的主要成分是(写化学式) __________________________ 。
(2)碱解反应中, 同时得到气体和沉淀反应的离子方程式为_____________________ 。
(3)一般地说 K>105时,该反应进行得就基本完全了。苛化反应中存在如下平衡:Li2CO3(s)+Ca2+(aq)⇌2Li+(aq)+ CaCO3(s)通过计算说明该反应是否进行完全________ (已知 Ksp(Li2CO3) = 8.64×10-4、Ksp(CaCO3)= 2.5×10-9)。
(4)碳化反应后的溶液得到 Li2CO3的具体实验操作有:加热浓缩、__________ 、过滤、洗涤、干燥。
(5)上述流程得到副产品冰晶石的化学方程式为_________________________________ 。

已知 LiOH 易溶于水,Li2CO3微溶于水。回答下列问题:
(1)电解铝废渣与浓硫酸反应产生的气体化学式为
(2)碱解反应中, 同时得到气体和沉淀反应的离子方程式为
(3)一般地说 K>105时,该反应进行得就基本完全了。苛化反应中存在如下平衡:Li2CO3(s)+Ca2+(aq)⇌2Li+(aq)+ CaCO3(s)通过计算说明该反应是否进行完全
(4)碳化反应后的溶液得到 Li2CO3的具体实验操作有:加热浓缩、
(5)上述流程得到副产品冰晶石的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】在一定条件下,金属单质X和非金属单质Y能够反应,生成化合物Z,Z能与水发生水解反应生成气体G和白色沉淀P(如下框图所示),已知气体G与空气之密度比约为1.17。请填空:

(1)组成单质X和Y的元素分别属第____________ 族和第___________ 族;
(2)Z与水发生水解反应方程式_____________________ ;
(3)每生成1mol的化合物Z,反应中转移_________________ mol的电子。

(1)组成单质X和Y的元素分别属第
(2)Z与水发生水解反应方程式
(3)每生成1mol的化合物Z,反应中转移
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸铈铵 (
( )微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。某工厂用含铈矿石[主要成分为
)微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。某工厂用含铈矿石[主要成分为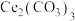 ]制备硫酸铈铵的工艺流程如图所示:
]制备硫酸铈铵的工艺流程如图所示:

已知:① 。
。
②硫酸铈铵的熔点为130℃,沸点为330℃。
回答下列问题:
(1)含铈矿石进行的“一系列操作”包含用硫酸酸浸,其中铈浸出率与温度的关系如图1所示,铈浸出率与硫酸浓度的关系如图2所示。工业生产应选择的适宜温度是___________ ℃,适宜的硫酸浓度是___________  。
。

(2)步骤一中发生反应的离子方程式为___________ 。
(3)步骤三中,反应生成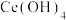 的化学方程式为
的化学方程式为___________ 。
(4)步骤三在0~30℃反应完全后又升温至90℃的目的是___________ 。
(5)步骤四反应完全后的溶液经___________ 、___________ 过滤,得到晶体,最后用___________ 洗涤2-3次后,得到高纯硫酸铈铵晶体。
(6)测定产品纯度。称取wg产品全部溶于水,配制成250mL溶液,准确量取25.00mL配制的溶液于锥形瓶中,以苯代邻氨基苯甲酸为指示剂,用 溶液滴定(滴定反应为
溶液滴定(滴定反应为
 ),起始读数为
),起始读数为 ,终点时溶液恰好由紫红色变为亮黄色,此时滴定管的读数为
,终点时溶液恰好由紫红色变为亮黄色,此时滴定管的读数为 ,则该产品的纯度为
,则该产品的纯度为___________ %(用含w、 、
、 的代数式表示)。
的代数式表示)。
 (
( )微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。某工厂用含铈矿石[主要成分为
)微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。某工厂用含铈矿石[主要成分为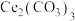 ]制备硫酸铈铵的工艺流程如图所示:
]制备硫酸铈铵的工艺流程如图所示:
已知:①
 。
。②硫酸铈铵的熔点为130℃,沸点为330℃。
回答下列问题:
(1)含铈矿石进行的“一系列操作”包含用硫酸酸浸,其中铈浸出率与温度的关系如图1所示,铈浸出率与硫酸浓度的关系如图2所示。工业生产应选择的适宜温度是
 。
。
(2)步骤一中发生反应的离子方程式为
(3)步骤三中,反应生成
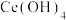 的化学方程式为
的化学方程式为(4)步骤三在0~30℃反应完全后又升温至90℃的目的是
(5)步骤四反应完全后的溶液经
(6)测定产品纯度。称取wg产品全部溶于水,配制成250mL溶液,准确量取25.00mL配制的溶液于锥形瓶中,以苯代邻氨基苯甲酸为指示剂,用
 溶液滴定(滴定反应为
溶液滴定(滴定反应为
 ),起始读数为
),起始读数为 ,终点时溶液恰好由紫红色变为亮黄色,此时滴定管的读数为
,终点时溶液恰好由紫红色变为亮黄色,此时滴定管的读数为 ,则该产品的纯度为
,则该产品的纯度为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】过量的碳排放会引起严重的温室效应,导致海洋升温、海水酸化,全球出现大规模珊瑚礁破坏,保护珊瑚礁刻不容缓。
(1)海水中含有的离子主要有Na+、Mg2+、Ca2+、K+、Cl–、CO32–和HCO3–。其中,导致海水呈弱碱性的微粒有______ 。
(2)珊瑚礁是珊瑚虫在生长过程中吸收海水中物质而逐渐形成的石灰石外壳。形成珊瑚礁的主要反应为Ca2+ + 2HCO3- CaCO3↓+ CO2↑+ H2O。
CaCO3↓+ CO2↑+ H2O。
① 请结合化学用语分析该反应能够发生的原因:______ 。
② 与珊瑚虫共生的藻类通过光合作用促进了珊瑚礁的形成;而海洋温度升高会使共生藻类离开珊瑚礁,导致珊瑚礁被破坏。请分析珊瑚礁的形成和破坏会受到共生藻类影响的原因:______ 。
(3)研究人员提出了一种封存大气中二氧化碳的思路:将二氧化碳和大量的水注入地下深层的玄武岩(主要成分为CaSiO3)中,使其转化为碳酸盐晶体。玄武岩转化为碳酸盐的化学方程式为______ 。
(4)“尾气CO2直接矿化磷石膏联产工艺”涉及低浓度CO2减排和工业固废磷石膏处理两大工业环保技术领域,其部分工艺流程如下图所示。
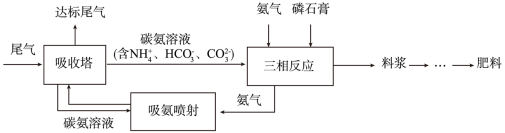
已知:磷石膏是在磷酸生产中用硫酸处理磷矿时产生的固体废渣,其主要成分为CaSO4·2H2O。
①吸收塔中发生的反应可能有______ (写出任意2个反应的离子方程式)。
②料浆的主要成分是______ (写化学式)。
(1)海水中含有的离子主要有Na+、Mg2+、Ca2+、K+、Cl–、CO32–和HCO3–。其中,导致海水呈弱碱性的微粒有
(2)珊瑚礁是珊瑚虫在生长过程中吸收海水中物质而逐渐形成的石灰石外壳。形成珊瑚礁的主要反应为Ca2+ + 2HCO3-
 CaCO3↓+ CO2↑+ H2O。
CaCO3↓+ CO2↑+ H2O。① 请结合化学用语分析该反应能够发生的原因:
② 与珊瑚虫共生的藻类通过光合作用促进了珊瑚礁的形成;而海洋温度升高会使共生藻类离开珊瑚礁,导致珊瑚礁被破坏。请分析珊瑚礁的形成和破坏会受到共生藻类影响的原因:
(3)研究人员提出了一种封存大气中二氧化碳的思路:将二氧化碳和大量的水注入地下深层的玄武岩(主要成分为CaSiO3)中,使其转化为碳酸盐晶体。玄武岩转化为碳酸盐的化学方程式为
(4)“尾气CO2直接矿化磷石膏联产工艺”涉及低浓度CO2减排和工业固废磷石膏处理两大工业环保技术领域,其部分工艺流程如下图所示。

已知:磷石膏是在磷酸生产中用硫酸处理磷矿时产生的固体废渣,其主要成分为CaSO4·2H2O。
①吸收塔中发生的反应可能有
②料浆的主要成分是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】LiMn2O4作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3,含有少量Si、Fe、Ni、Al等元素)制备LiMn2O4的流程如图:

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为________ 。为提高溶矿速率,可采取的措施________ (举1例)。
(2)加入少量MnO2的作用是________ 。不宜使用H2O2替代MnO2,原因是________ 。
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=________ mol•L-1;用石灰乳调节至pH≈7,除去的金属离子是________ 。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有________ 。
(5)煅烧窑中,生成LiMn2O4反应的化学方程式是________ 。

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为
(2)加入少量MnO2的作用是
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有
(5)煅烧窑中,生成LiMn2O4反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上电解精炼铜的阳极泥是重要的二次资源,从中间产物分金渣(主要成分为:AgCl、 Ag2S、PbSO4、 BaSO4)中获取高纯银的流程如图所示:
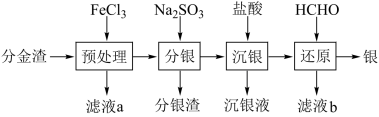
已知:在上述反应的温度下Ksp(AgCl)=1.8×10-10,Ksp(Ag2s)=6.38×10-50,
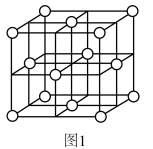
(1)银的一种晶胞如图1所示,银原子周围距离最近且相等的银原子为_______ 。
(2)“预处理”加入FeCl3溶液将Ag2S转化为AgCl。若将AgCl放在KI溶液中振荡,则有部分AgCl转化为AgI。 AgI有α、β、γ三种晶型,其中α- AgI在电场作用下,Ag+不需要克服太大的阻力,就可以发生迁移。因此α- AgI晶体在电池中,可作为_______ 。
(3)已知: Ag+ +2SO = [Ag(SO3)2]3-, K = 1.0 ×108.68,“分银”时,AgCl与Na2SO3反应生成[Ag(SO3)2]3-,该反应的平衡常数K=
= [Ag(SO3)2]3-, K = 1.0 ×108.68,“分银”时,AgCl与Na2SO3反应生成[Ag(SO3)2]3-,该反应的平衡常数K=_______ 。
(4)“分银”时,[Ag(SO3)2]3-的浓度与溶液pH的关系如图2; SO 及其与H+形成的微粒的浓度分数α随溶液pH变化的关系如图3。
及其与H+形成的微粒的浓度分数α随溶液pH变化的关系如图3。
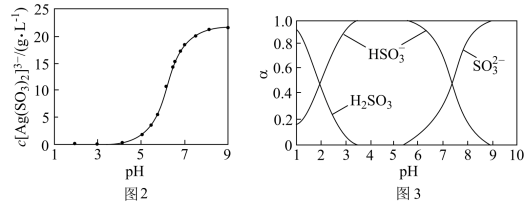
“沉银”时的终点pH需控制在3.5-5.5范围内,不能过低的原因是_______ 。
(5)“还原"时HCHO转化为HCOOH,其化学方程式为_______ 。
(6)已如Ag+ +SCN- =AgSCN↓ (白色),实验室可通过如下过程测定所制银样品的纯度(杂质不参与反应):
①称取制备的银样品1.000g,加适量稀硝酸溶解,定容到100mL容量瓶中。
②准确称取25.00 mL溶液置于锥形瓶中,般化后滴入几滴铁铵矾[NH4Fe(SO4)2]溶液作指示剂,再用0.1000 mol / L NH4SCN标准溶液滴定,滴定终点的实验现象为溶液变为(血)红色。
③重复②的操作两次,所用NH4SCN标准溶液的平均体积为22. 00mL。则样品中银的质量分数为_______ 。(写出计算过程)

已知:在上述反应的温度下Ksp(AgCl)=1.8×10-10,Ksp(Ag2s)=6.38×10-50,
(1)银的一种晶胞如图1所示,银原子周围距离最近且相等的银原子为

(2)“预处理”加入FeCl3溶液将Ag2S转化为AgCl。若将AgCl放在KI溶液中振荡,则有部分AgCl转化为AgI。 AgI有α、β、γ三种晶型,其中α- AgI在电场作用下,Ag+不需要克服太大的阻力,就可以发生迁移。因此α- AgI晶体在电池中,可作为
(3)已知: Ag+ +2SO
 = [Ag(SO3)2]3-, K = 1.0 ×108.68,“分银”时,AgCl与Na2SO3反应生成[Ag(SO3)2]3-,该反应的平衡常数K=
= [Ag(SO3)2]3-, K = 1.0 ×108.68,“分银”时,AgCl与Na2SO3反应生成[Ag(SO3)2]3-,该反应的平衡常数K=(4)“分银”时,[Ag(SO3)2]3-的浓度与溶液pH的关系如图2; SO
 及其与H+形成的微粒的浓度分数α随溶液pH变化的关系如图3。
及其与H+形成的微粒的浓度分数α随溶液pH变化的关系如图3。
“沉银”时的终点pH需控制在3.5-5.5范围内,不能过低的原因是
(5)“还原"时HCHO转化为HCOOH,其化学方程式为
(6)已如Ag+ +SCN- =AgSCN↓ (白色),实验室可通过如下过程测定所制银样品的纯度(杂质不参与反应):
①称取制备的银样品1.000g,加适量稀硝酸溶解,定容到100mL容量瓶中。
②准确称取25.00 mL溶液置于锥形瓶中,般化后滴入几滴铁铵矾[NH4Fe(SO4)2]溶液作指示剂,再用0.1000 mol / L NH4SCN标准溶液滴定,滴定终点的实验现象为溶液变为(血)红色。
③重复②的操作两次,所用NH4SCN标准溶液的平均体积为22. 00mL。则样品中银的质量分数为
您最近一年使用:0次



