解题方法
1 . 下列实验中,由实验现象不能得到正确结论的是
| 选项 | 实验 | 现象 | 结论 |
| A | 相同的铝片分别与同温同体积,且c(H+)=1mol·L-1的盐酸、硫酸反应 | 铝与盐酸反应产生气泡较快 | 可能是Cl-对该反应起到促进作用 |
| B | 在醋酸钠溶液中滴入酚酞溶液并加热 | 加热后红色加深 | 证明盐类水解是吸热反应 |
| C | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡 | 沉淀由白色变为红褐色 | Fe(OH)3的溶解度小于Mg(OH)2的溶解度 |
| D | 向5mL0.1mol/L的AgNO3溶液中先滴加5滴0.lmol/LNaCl溶液,再加5滴0.lmol/LKI溶液 | 白色沉淀转化为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列由实验操作及现象所得结论正确的是
| A.将同浓度同体积的KHSO3溶液与FeCl3溶液混合,充分反应后滴入KSCN溶液,溶液变红色,证明该反应存在一定限度 |
| B.向可能含有苯酚的苯中加入适量的浓溴水,若未出现白色沉淀,证明苯中不含有苯酚 |
| C.将饱和NaBr溶液滴入AgCl浊液中,沉淀颜色由白色变为淡黄色,证明Ksp(AgCl)>Ksp(AgBr) |
| D.常温下,用pH试纸分别测定浓度均为0.1mol•L-1CH3COONa溶液和Na2S溶液,后者pH大,证明酸性:H2S<CH3COOH |
您最近一年使用:0次
解题方法
3 . 某实验小组通过下图所示实验探究 与水的反应。已知:
与水的反应。已知: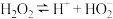 ;
; 。下列分析正确的是
。下列分析正确的是

 与水的反应。已知:
与水的反应。已知: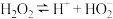 ;
; 。下列分析正确的是
。下列分析正确的是
A.实验②中 的主要作用是降低了水中 的主要作用是降低了水中 的溶解度 的溶解度 |
B.⑤酸性 溶液足量,则④⑤产生 溶液足量,则④⑤产生 的总量与②产生 的总量与②产生 的量相等 的量相等 |
C.实验④证明了同温下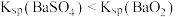 |
| D.实验②⑤均可证明实验①中有复分解反应发生 |
您最近一年使用:0次
名校
解题方法
4 . 根据下列操作和现象所得到的结论正确的是
| 选项 | 操作和现象 | 结论 |
| A | 向碳酸钙中加入盐酸,产生的气体经饱和碳酸氢钠溶液洗气后,再通入硅酸钠溶液,出现白色沉淀 | 利用该实验可以证明非金属性: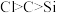 |
| B | 向大豆油和煤油中分别加入足量 溶液充分加热,一种液体仍然分层,另一种液体不再分层 溶液充分加热,一种液体仍然分层,另一种液体不再分层 | 分层的液体是大豆油,不再分层的是煤油 |
| C | 向等体积、等浓度的稀硫酸中分别加入少许等物质的量的ZnS和CuS固体,ZnS溶解而CuS不溶解 |  |
| D | 向 溶液中滴加 溶液中滴加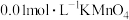 溶液,溶液褪色 溶液,溶液褪色 | H2O2具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 下列实验过程不能达到实验目的的是
| 实验目的 | 实验过程 | |
| A | 配制 溶液 溶液 | 将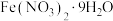 溶于较浓硝酸,然后加水稀释 溶于较浓硝酸,然后加水稀释 |
| B | 探究 的漂白性 的漂白性 | 向盛有2mL黄色氯化铁溶液的试管中通入 观察颜色变化 观察颜色变化 |
| C | 证明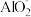 结合 结合 的能力强于 的能力强于 | 向 溶液中加入 溶液中加入 溶液,观察到有白色沉淀生成 溶液,观察到有白色沉淀生成 |
| D | 比较AgCl和AgI的 相对大小 相对大小 | 向等体积饱和AgCl溶液和饱和AgI溶液中分别滴加等量的 浓溶液 浓溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下列实验目的对应的方案设计、现象和结论都正确的是
选项 | 实验目的 | 方案设计 | 现象和结论 |
A | 比较 | 向 | 白色沉淀转化为红褐色沉淀,证明 |
B | 探究压强对平衡移动的影响 | 密闭容器中盛 | 气体颜色加深,说明平衡向生成 |
C | 比较 | 向等体积饱和 | 得到沉淀 |
D | 比较 | 用 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 用下列装置不能达到实验目的的是
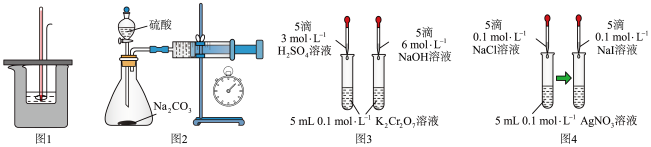

| A.图1:测量强酸强碱中和反应的反应热 |
B.图2:测定 和稀硫酸反应的速率 和稀硫酸反应的速率 |
| C.图3:验证浓度对化学平衡的影响 |
D.图4:证明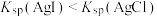 |
您最近一年使用:0次
2023-01-14更新
|
354次组卷
|
3卷引用:广东省佛山市2022~2023学年高二上学期期末考试化学试题
解题方法
8 . 根据下列实验操作和现象能推出相应结论的是
| 选项 | 实验操作和现象 | 实验目的或结论 |
| A | 向NaAlO2溶液中滴加NaHCO3溶液,产生白色沉淀 |  与 与 发生了相互促进的双水解反应 发生了相互促进的双水解反应 |
| B | 向2mL0.1 mol∙L−1硝酸银溶液中加入1mL 0.1 mol∙L−1NaCl溶液,出现白色沉淀,再加入几滴0.1 mol∙L−1的Na2S溶液,有黑色沉淀生成 | 证明氯化银的溶解度大于硫化银的溶解度 |
| C | 向2 mL 0.l mol∙L−1 MgCl2溶液中加入 l mL 0.1 mol∙L−1 NaOH溶液,再加入4滴0.l mol∙L−1FeCl3溶液 | 验证Mg(OH)2沉淀能转化为Fe(OH)3沉淀 |
| D | 常温下AgCl固体分别加到100mL水、0.1 mol∙L−1 NaCl溶液、0.1 mol∙L−1CaCl2溶液中,溶解的质量逐渐减小 | AgCl的溶解度、Ksp均受同离子效应的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 下列实验方案能达到实验目的的是
| 实验目的 | 实验操作 | |
| A | 检验酸雨中含有 | 取样,向样品中滴入 溶液,有白色沉淀生成 溶液,有白色沉淀生成 |
| B | 检验钢铁发生吸氧腐蚀 | 取钢铁电极附近溶液,向其中滴加 溶液,产生蓝色 溶液,产生蓝色 沉淀 沉淀 |
| C | 证明酸性: | 室温下,用 计分别测等浓度的 计分别测等浓度的 溶液和 溶液和 溶液的 溶液的 ,测得 ,测得 溶液的 溶液的 大 大 |
| D | 验证: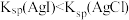 | 向 溶液中滴加2滴 溶液中滴加2滴 溶液,产生白色沉淀,再滴加2滴 溶液,产生白色沉淀,再滴加2滴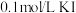 溶液,沉淀变成黄色 溶液,沉淀变成黄色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . Ⅰ、某小组同学用下列试剂研究将 转化为
转化为 。(已知:
。(已知: ,
, )
)
(1)实验操作:所用试剂: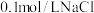 溶液,
溶液, 溶液,
溶液,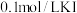 溶液;向盛有
溶液;向盛有 溶液的试管中滴加2滴
溶液的试管中滴加2滴 溶液,充分振荡后,
溶液,充分振荡后, ___________ (将操作补充完整)。
(2)实验现象:上述实验中,沉淀由白色变为___________ 色现象可证明 转化为
转化为 。
。
(3)分析及讨论
①该沉淀转化反应的离子方程式是___________ 。
②定量分析。由上述沉淀转化反应的化学平衡常数表达式可推导:
___________ (列式即可,不必计算结果)。
③同学们结合②中的分析方法,认为教材中的表述:“一般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实现”,可进一步表述为对于组成形式相同的沉淀,
___________ (填“小”或者“大”)的沉淀转化为
___________ (填“更小”或者“更大”)的沉淀容易实现。
Ⅱ、某同学设计如图实验装置研究 溶液和
溶液和 溶液间的反应(a、b均为石墨)。
溶液间的反应(a、b均为石墨)。
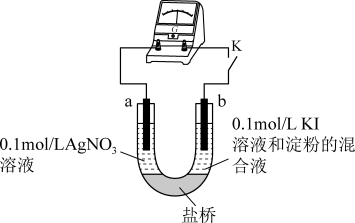
(4)当K闭合后,发现电流计指针偏转,b极附近溶液变蓝。
①b极发生的是___________ (填“氧化”或“还原”)反应。
②a极上的电极反应式是___________ 。
(5)事实证明: 溶液与
溶液与 的溶液混合只能得到
的溶液混合只能得到 沉淀,对比(4)中反应,从反应原理的角度解释产生该事实的可能原因是
沉淀,对比(4)中反应,从反应原理的角度解释产生该事实的可能原因是 与
与 之间发生沉淀反应比氧化还原反应的速率或限度
之间发生沉淀反应比氧化还原反应的速率或限度___________ (填“小”或者“大”)。
 转化为
转化为 。(已知:
。(已知: ,
, )
)(1)实验操作:所用试剂:
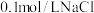 溶液,
溶液, 溶液,
溶液,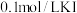 溶液;向盛有
溶液;向盛有 溶液的试管中滴加2滴
溶液的试管中滴加2滴 溶液,充分振荡后,
溶液,充分振荡后, (2)实验现象:上述实验中,沉淀由白色变为
 转化为
转化为 。
。(3)分析及讨论
①该沉淀转化反应的离子方程式是
②定量分析。由上述沉淀转化反应的化学平衡常数表达式可推导:

③同学们结合②中的分析方法,认为教材中的表述:“一般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实现”,可进一步表述为对于组成形式相同的沉淀,


Ⅱ、某同学设计如图实验装置研究
 溶液和
溶液和 溶液间的反应(a、b均为石墨)。
溶液间的反应(a、b均为石墨)。
(4)当K闭合后,发现电流计指针偏转,b极附近溶液变蓝。
①b极发生的是
②a极上的电极反应式是
(5)事实证明:
 溶液与
溶液与 的溶液混合只能得到
的溶液混合只能得到 沉淀,对比(4)中反应,从反应原理的角度解释产生该事实的可能原因是
沉淀,对比(4)中反应,从反应原理的角度解释产生该事实的可能原因是 与
与 之间发生沉淀反应比氧化还原反应的速率或限度
之间发生沉淀反应比氧化还原反应的速率或限度
您最近一年使用:0次

 和
和 的
的 相对大小
相对大小 的
的 的
的 溶液,再滴加
溶液,再滴加 溶液
溶液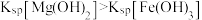
 ,一段时间后反应达平衡,压缩体积至原来的一半
,一段时间后反应达平衡,压缩体积至原来的一半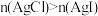 ,则
,则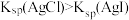
 与
与 的酸性
的酸性

