1 .  是一种具有强温室效应的分子,将其先转化为合成气
是一种具有强温室效应的分子,将其先转化为合成气 再合成液态链烃或芳香烃是实现碳中和的重要途径,请回答下列问题。
再合成液态链烃或芳香烃是实现碳中和的重要途径,请回答下列问题。
(1)已知H2、CO和C10H22(正癸烷, )的燃烧热依次是
)的燃烧热依次是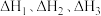 ,则反应
,则反应 的反应热
的反应热
_______ (用含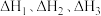 的代数式表示)。
的代数式表示)。
(2)氢气作为理想能源的原因_______ (写出一个原因即可)。
(3)甲烷转化为合成气主要是在催化剂的作用下发生如下反应:
 反应I
反应I
 反应Ⅱ
反应Ⅱ
①向一定温度下的 刚性容器中充入
刚性容器中充入 甲烷和
甲烷和 水蒸气,
水蒸气, 后体系达平衡状态,此时容器中含有
后体系达平衡状态,此时容器中含有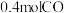 和
和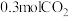 ,则
,则 内反应I的平均速率
内反应I的平均速率 =
=_______  ,写出该温度下反应Ⅱ的平衡常数为
,写出该温度下反应Ⅱ的平衡常数为_______ 。
②在起始投料比一定的密闭容器中,温度对 平衡转化率、
平衡转化率、 选择性、
选择性、 选择性的影响如图所示,其中表示
选择性的影响如图所示,其中表示 选择性的曲线是
选择性的曲线是_______ (填“ ”、“
”、“ ”或“
”或“ ”)。
”)。_______ 。
②若放电一段时间后,消耗氧气2.24L(标准状况),理论上外电路转移电子的物质的量为_______ 。
 是一种具有强温室效应的分子,将其先转化为合成气
是一种具有强温室效应的分子,将其先转化为合成气 再合成液态链烃或芳香烃是实现碳中和的重要途径,请回答下列问题。
再合成液态链烃或芳香烃是实现碳中和的重要途径,请回答下列问题。(1)已知H2、CO和C10H22(正癸烷,
 )的燃烧热依次是
)的燃烧热依次是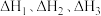 ,则反应
,则反应 的反应热
的反应热
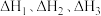 的代数式表示)。
的代数式表示)。(2)氢气作为理想能源的原因
(3)甲烷转化为合成气主要是在催化剂的作用下发生如下反应:
 反应I
反应I 反应Ⅱ
反应Ⅱ①向一定温度下的
 刚性容器中充入
刚性容器中充入 甲烷和
甲烷和 水蒸气,
水蒸气, 后体系达平衡状态,此时容器中含有
后体系达平衡状态,此时容器中含有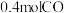 和
和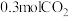 ,则
,则 内反应I的平均速率
内反应I的平均速率 =
= ,写出该温度下反应Ⅱ的平衡常数为
,写出该温度下反应Ⅱ的平衡常数为②在起始投料比一定的密闭容器中,温度对
 平衡转化率、
平衡转化率、 选择性、
选择性、 选择性的影响如图所示,其中表示
选择性的影响如图所示,其中表示 选择性的曲线是
选择性的曲线是 ”、“
”、“ ”或“
”或“ ”)。
”)。

②若放电一段时间后,消耗氧气2.24L(标准状况),理论上外电路转移电子的物质的量为
您最近一年使用:0次
2024-05-12更新
|
107次组卷
|
2卷引用:天津市河北区2023-2024学年高三下学期二模化学试卷
名校
解题方法
2 . 科学家称他们正在研制的铝电池未来有望取代锂电池。银铝电池具有能量密度高的优点,电池装置如图;电池放电时的反应为: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是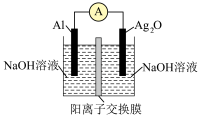
A. 电极发生还原反应 电极发生还原反应 |
| B.阳离子交换膜允许阳离子和电子通过 |
C.当导线中通过 电子时,负极区溶液质量减小 电子时,负极区溶液质量减小 |
D.正极电极反应式为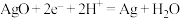 |
您最近一年使用:0次
2024-04-23更新
|
852次组卷
|
3卷引用:天津市河北区2024届高三总复习质量检测(一)化学试题
天津市河北区2024届高三总复习质量检测(一)化学试题(已下线)题型8 反应热 电化学的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届陕西省西安中学高三下学期第七次模拟考试理综试题-高中化学
3 . 中国杭州举行的第19届亚运会倡导:绿色能源引领科技与环保,氢气既是一种优质的能源,又是一种重要化工原料,高纯氢的制备是目前的研究热点。
(1)根据下图写出a极反应式___________________________ 。
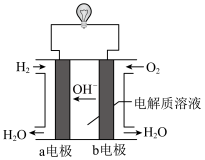
(2)利用氢气进行工业合成氨的反应压强一般控制在___________  ,反应方程式为
,反应方程式为____________________________ 。
甲烷水蒸气催化重整是制备高纯氢的方法之一,甲烷和水蒸气反应的热化学方程式是: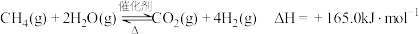
已知反应器中存在如下反应过程:
Ⅰ.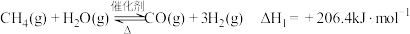
Ⅱ.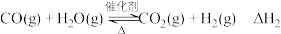
(3)根据上述信息计算:
_________ 、
________ 。
(4)某温度下,在体积为 的密闭容器内发生Ⅰ反应,当下列物理量不再发生变化时,可以说明该反应达到平衡的是________。(填序号)
的密闭容器内发生Ⅰ反应,当下列物理量不再发生变化时,可以说明该反应达到平衡的是________。(填序号)
(5)欲增大 转化为
转化为 的平衡转化率,可采取的措施有_________(填标号)。
的平衡转化率,可采取的措施有_________(填标号)。
(1)根据下图写出a极反应式

(2)利用氢气进行工业合成氨的反应压强一般控制在
 ,反应方程式为
,反应方程式为甲烷水蒸气催化重整是制备高纯氢的方法之一,甲烷和水蒸气反应的热化学方程式是:
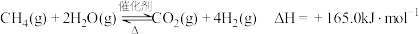
已知反应器中存在如下反应过程:
Ⅰ.
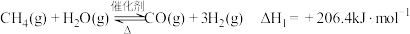
Ⅱ.
化学键 |
|
|
|
|
键能 | 436 | 465 | a | 1076 |
(3)根据上述信息计算:


(4)某温度下,在体积为
 的密闭容器内发生Ⅰ反应,当下列物理量不再发生变化时,可以说明该反应达到平衡的是________。(填序号)
的密闭容器内发生Ⅰ反应,当下列物理量不再发生变化时,可以说明该反应达到平衡的是________。(填序号)| A.混合气体的压强 | B.混合气体的密度 | C.混合气体的总物质的量 | D.混合气体的颜色 |
(5)欲增大
 转化为
转化为 的平衡转化率,可采取的措施有_________(填标号)。
的平衡转化率,可采取的措施有_________(填标号)。A.适当增大反应物投料比 | B.提高压强 | C.分离出 |
您最近一年使用:0次
名校
解题方法
4 . 锌铜原电池装置如图,下列说法不正确的是

| A.锌电极上发生氧化反应 | B.盐桥中的 移向 移向 溶液 溶液 |
| C.电子从锌片经电流计流向铜片 | D.铜电极上发生反应: |
您最近一年使用:0次
2023-12-03更新
|
524次组卷
|
15卷引用:天津市第二中学2022-2023学年高二上学期12月学情调查化学试题
天津市第二中学2022-2023学年高二上学期12月学情调查化学试题北京市朝阳区2021-2022学年高二上学期期末考试化学试题北京市房山区2022-2023学年高二上学期期中质量检测化学试题北京市丰台区2022-2023高二上学期期中考试化学(B卷)试题天津市河东区 2022-2023 学年高二上学期期末质量检测化学试题北京师范大学附属中学2022-2023学年上学期高二化学期末试题北京市昌平区第一中学2022-2023学年高二上学期期末考试化学试题北京市第二十中学2022-2023学年高二上学期期末考试化学试题河南省许昌市2022-2023学年高二上学期期末教学质量检测化学试题 北京市第一七一中学2023-2024学年高二上学期10月月考化学试题北京市丰台区2023-2024学年高二上学期期中联考(B卷)化学试题北京市第五十中学2023-2024学年高二上学期期中考试化学试题北京市清华大学附属中学朝阳学校2023-2024学年高二上学期期中考试化学试题北京市第十五中学2022-2023学年高二上学期期中考试 化学试题甘肃省武威第七中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
5 . 在如图装置中,观察到图1装置铜电极上产生大量无色气泡,而图2装置中铜电极上无气泡产生,铬电极上产生大量有色气泡。下列叙述不正确的是
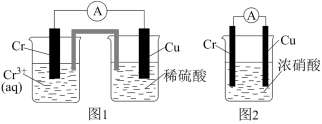
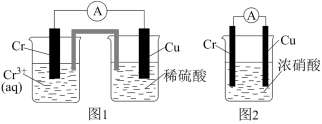
A.图1装置中 Cu 电极上电极反应式是 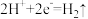 |
B.图2装置中 Cu 电极上发生的电极反应为 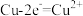 |
C.图2装置中 Cr电极上电极反应式为  |
| D.两个装置中,电子均由 Cr电极经导线流向 Cu 电极 |
您最近一年使用:0次
2023-10-24更新
|
485次组卷
|
10卷引用:天津市第二中学2022-2023学年高二上学期12月学情调查化学试题
天津市第二中学2022-2023学年高二上学期12月学情调查化学试题河南省顶尖名校联盟2021-2022学年高二上学期12月联考化学试题辽宁省沈阳市五校协作体2021-2022学年高二上学期期末联考化学试题黑龙江省佳木斯市第十二中学(佳木斯市建三江第一中学)2021-2022学年高一下学期期中考试化学试题湖北省部分省级示范高中(四校联考)2022-2023学年高二上学期期末测试化学试题河北省石家庄市第一中学东校区2023-2024学年高二上学期第一次月考化学试题河北省石家庄第一中学2023-2024学年高二上学期10月月考化学试题广东省普宁二中实验学校2023-2024学年高二上学期第三次月考化学试题新疆石河子第一中学2023-2024学年高二上学期12月月考化学试题四川省眉山市仁寿县铧强中学 眉山天府新区实验中学2023-2024学年高二上学期11月期中联考化学试题
解题方法
6 . 下列关于如图所示装置的叙述,正确的是


| A.铜片表面发生氧化反应 | B.电子从锌片经导线流向铜片 |
| C.电流从锌片经导线流向铜片 | D.锌片是正极,其质量逐渐减小 |
您最近一年使用:0次
解题方法
7 . 镍—镉电池是一种新型的封闭式体积小的可充电电池。其工作原理如下图所示,下列说法不正确的是
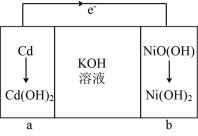

| A.放电时a极为负极 |
B.放电时a极的反应 |
| C.充电时b极接外接电源正极 |
D.用该电池电解足量的饱和食盐水,电路中通过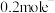 ,阴极生成 ,阴极生成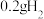 |
您最近一年使用:0次
解题方法
8 . 我国科研人员利用双极膜技术构造出一类具有高能量密度、优异的循环性能的新型水系电池,模拟装置如图所示。已知电极材料分别为Zn和MnO2,相应的产物为 和Mn2+。下列说法错误的是
和Mn2+。下列说法错误的是
 和Mn2+。下列说法错误的是
和Mn2+。下列说法错误的是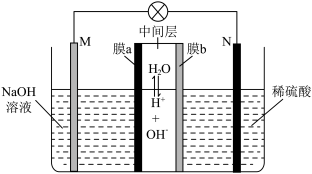
| A.双极膜中的OH-通过膜a移向M极 |
| B.电池工作一段时间后,NaOH溶液的pH不变 |
| C.N电极的反应式为MnO2 +4H+ +2e- =Mn2+ +2H2O |
| D.若电路中通过2 mol e-,则稀硫酸溶液质量增加89 g |
您最近一年使用:0次
2023-04-19更新
|
448次组卷
|
3卷引用:天津市河北区2023-2024学年高三下学期二模化学试卷
解题方法
9 . 利用所学知识完成下列问题。
Ⅰ. 和
和 均为重要的工业原料。已知:
均为重要的工业原料。已知:
 I
I

请回答下列问题
(1)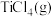 与
与 反应生成
反应生成 、C(s)和氯气的热化学方程式为
、C(s)和氯气的热化学方程式为_______ 。升高温度对该反应的影响为_______ 。
(2)若反应Ⅱ的逆反应的活化能为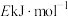 ,则E
,则E_______ (填“>”“<”或“=”)220.9。
(3)t℃时,向10L恒容密闭容器中充入 和
和 ,发生反应Ⅰ.5min时达到平衡,测得
,发生反应Ⅰ.5min时达到平衡,测得 的物质的量为0.2mol。
的物质的量为0.2mol。
①0~5min内,用 表示的反应速率
表示的反应速率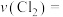
_______ 。
② 的平衡转化率为
的平衡转化率为_______ 。
③该反应的平衡常数为_______ 。
④下列措施,既能加快逆反应速率又能增大 平衡转化率的是
平衡转化率的是_______ (填字母)。
A.缩小容器容积 B.加入催化剂 C.分离出部分 D.增大
D.增大 浓度
浓度
Ⅱ.利用铜和石墨作电极,在盐酸介质中,铜与氢叠氮酸 构成原电池,总反应离子方程式为
构成原电池,总反应离子方程式为 。
。
(4)该电池的正极反应式为:_______ 。
Ⅰ.
 和
和 均为重要的工业原料。已知:
均为重要的工业原料。已知: I
I
请回答下列问题
(1)
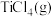 与
与 反应生成
反应生成 、C(s)和氯气的热化学方程式为
、C(s)和氯气的热化学方程式为(2)若反应Ⅱ的逆反应的活化能为
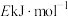 ,则E
,则E(3)t℃时,向10L恒容密闭容器中充入
 和
和 ,发生反应Ⅰ.5min时达到平衡,测得
,发生反应Ⅰ.5min时达到平衡,测得 的物质的量为0.2mol。
的物质的量为0.2mol。①0~5min内,用
 表示的反应速率
表示的反应速率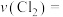
②
 的平衡转化率为
的平衡转化率为③该反应的平衡常数为
④下列措施,既能加快逆反应速率又能增大
 平衡转化率的是
平衡转化率的是A.缩小容器容积 B.加入催化剂 C.分离出部分
 D.增大
D.增大 浓度
浓度Ⅱ.利用铜和石墨作电极,在盐酸介质中,铜与氢叠氮酸
 构成原电池,总反应离子方程式为
构成原电池,总反应离子方程式为 。
。(4)该电池的正极反应式为:
您最近一年使用:0次
10 . 如图甲是一种利用微生物将废水中的尿素( ,氮元素显
,氮元素显 价)的化学能直接转化为电能,并生成对环境无害物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是
价)的化学能直接转化为电能,并生成对环境无害物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是

 ,氮元素显
,氮元素显 价)的化学能直接转化为电能,并生成对环境无害物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是
价)的化学能直接转化为电能,并生成对环境无害物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是
A. 透过质子交换膜由右向左移动 透过质子交换膜由右向左移动 |
| B.铜电极应与X相连接 |
C.M电极的反应式: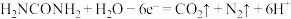 |
| D.当N电极消耗0.5mol气体时,则铁电极增重32g |
您最近一年使用:0次








