名校
1 . 根据化学能转化电能的相关知识,回答下列问题:
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是___________ ,发生___________ (填“氧化”或“还原”)反应,电解质溶液是___________ 。
(2)正极上出现的现象是___________ 。
(3)若导线上转移电子1mol,则生成银___________ g。___________ 。
(5)写出乙中负极的电极反应式:___________ 。
Ⅲ.电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。___________ (填“正极”或“负极”);
(7)①正极的电极反应式为___________ 。
②若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为___________ 。
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是
(2)正极上出现的现象是
(3)若导线上转移电子1mol,则生成银
II.有甲、乙两位同学均想利用原电池反应检测金属 活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol·L-1的H2SO4溶液中,乙同学将电极放入6mol·L-1的NaOH溶液中,如图所示。
活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol·L-1的H2SO4溶液中,乙同学将电极放入6mol·L-1的NaOH溶液中,如图所示。

(5)写出乙中负极的电极反应式:
Ⅲ.电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。
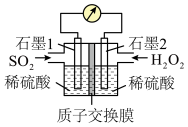
(7)①正极的电极反应式为
②若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为
您最近一年使用:0次
名校
解题方法
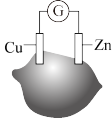
2 . Ⅰ.化学电池的发明,是贮能和供能技术的巨大进步。某同学用柠檬自制如图所示水果电池。_______ ,若导线中转移了 电子,则消耗锌的质量是
电子,则消耗锌的质量是_______ g。
Ⅱ.在恒温下,将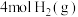 和
和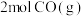 充入1L恒容的密闭容器中发生如下反应:
充入1L恒容的密闭容器中发生如下反应: 。下图是和
。下图是和 的浓度随时间变化的关系图,回答下列问题:
的浓度随时间变化的关系图,回答下列问题: 的平均反应速率是
的平均反应速率是_______  ;
; 的平衡转化率为
的平衡转化率为_______ 。
(3)设起始压强为 ,平衡时压强为
,平衡时压强为 ,则
,则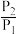 的值为
的值为_______ 。
Ⅲ.将一定量纯净的氨基甲酸铵( )置于特制的恒容密闭真空容器中(假设固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
)置于特制的恒容密闭真空容器中(假设固体试样体积忽略不计),在恒定温度下使其达到分解平衡: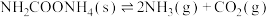 。
。
(4)下列不能 判断该分解反应已经达到最大限度的是_______(填选项)。
 电子,则消耗锌的质量是
电子,则消耗锌的质量是Ⅱ.在恒温下,将
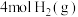 和
和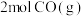 充入1L恒容的密闭容器中发生如下反应:
充入1L恒容的密闭容器中发生如下反应: 。下图是和
。下图是和 的浓度随时间变化的关系图,回答下列问题:
的浓度随时间变化的关系图,回答下列问题: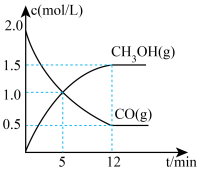
 的平均反应速率是
的平均反应速率是 ;
; 的平衡转化率为
的平衡转化率为(3)设起始压强为
 ,平衡时压强为
,平衡时压强为 ,则
,则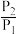 的值为
的值为Ⅲ.将一定量纯净的氨基甲酸铵(
 )置于特制的恒容密闭真空容器中(假设固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
)置于特制的恒容密闭真空容器中(假设固体试样体积忽略不计),在恒定温度下使其达到分解平衡: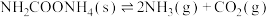 。
。(4)下列
A. |
| B.密闭容器中氨气的物质的量不变 |
C.容器中 与 与 的物质的量之比保持不变 的物质的量之比保持不变 |
| D.密闭容器中总压强保持不变 |
您最近一年使用:0次
名校
解题方法
3 . 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是
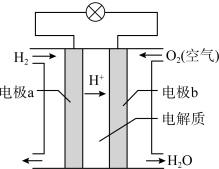
| A.该电池工作时化学能转化为电能 | B.电极b为正极,电极反应式为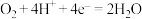 |
| C.外电路中电流由电极a通过导线流向电极b | D.该电池的总反应: |
您最近一年使用:0次
4 . 根据实验操作及现象,下列结论中正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 常温下将铁片分别插入稀硝酸和浓硝酸中 前者产生无色无味气体,后者无明显现象 | 稀硝酸的氧化性比浓硝酸的强 |
| B | 取一定量的 样品,溶解后加入 样品,溶解后加入 溶液 溶液产生白色沉淀。加入稀盐酸,仍有白色沉淀 | 此样品中含有 |
| C | 将Ag、Cu和 溶液组成原电池。连通后 溶液组成原电池。连通后Ag表面有银白色金属沉积,Cu电极附近溶液逐渐变蓝 | Cu的金属性比Ag强 |
| D | 向蔗糖中加入浓硫酸,蔗糖变黑,体积膨胀 放出有刺激性气味的气体 | 浓硫酸具有吸水性、强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 燃料电池是一种常见化学电源,如图是最常见的可以实现“零污染”的氢-氧燃料电池的简易工作示意图。下列说法正确的是

A.总反应是2H2+O2 2H2O 2H2O |
| B.通H2的一极是负极,得到电子 |
| C.b电极上发生还原反应,电极反应式为O2+4e-+2H2O=4OH- |
| D.该装置可以实现化学能转化为电能 |
您最近一年使用:0次
名校
解题方法
6 . 某原电池装置如图所示,下列说法正确的是
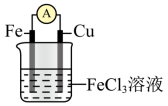
| A.Cu片上发生反应的电极反应式为Fe3++e-=Fe2+ |
| B.Fe电极消耗5.6g,则外电路转移0.3mole- |
| C.溶液中的Fe3+向Fe片移动 |
| D.电子由Cu片通过导线流向Fe片 |
您最近一年使用:0次
名校
解题方法
7 . 利用表中实验装置进行相应实验,能达到实验目的的是
选项 | A | B |
装置 |
|
|
目的 | 检验化合物中是否含钾元素 | 证明非金属性: |
选项 | C | D |
装置 |
|
|
目的 | 分离乙醇和水 | 将化学能转化为电能 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 研究化学能与热能、电能的转化具有重要价值。回答下列问题:
(1)下列化学反应过程中的能量变化符合如图所示的是___________ (填序号)。
③金属钠与水反应 ④酒精燃烧
⑤灼热的碳与二氧化碳反应 ⑥ 与
与 反应
反应
(2)若利用反应 设计一个原电池,请在如图内完善实验装置
设计一个原电池,请在如图内完善实验装置______ 。
 溶液中,乙同学将电极放入2
溶液中,乙同学将电极放入2 的
的 溶液中,如图所示。
溶液中,如图所示。___________ (填“氧化”或“还原”)反应。
②乙池中写出铝电极的电极反应式:___________ 。
(4)甲醇燃料电池具有很大的发展潜力,其工作原理如图所示。电极A为燃料电池的___________ (填“正”或“负”)极,正极的电极反应式为___________ 。
(1)下列化学反应过程中的能量变化符合如图所示的是
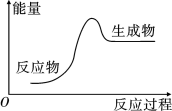
③金属钠与水反应 ④酒精燃烧
⑤灼热的碳与二氧化碳反应 ⑥
 与
与 反应
反应(2)若利用反应
 设计一个原电池,请在如图内完善实验装置
设计一个原电池,请在如图内完善实验装置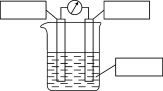

 溶液中,乙同学将电极放入2
溶液中,乙同学将电极放入2 的
的 溶液中,如图所示。
溶液中,如图所示。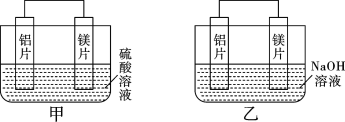
②乙池中写出铝电极的电极反应式:
(4)甲醇燃料电池具有很大的发展潜力,其工作原理如图所示。电极A为燃料电池的

您最近一年使用:0次
名校
9 . 下列关于反应与能量说法正确的是

| A.化学反应一定伴随物质变化与能量变化 |
B.由如图可知,向密闭容器中充入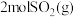 和 和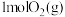 充分反应后放热 充分反应后放热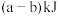 |
C. 溶于水释放出大量的热,可利用该反应设计成原电池,把化学能转化为电能 溶于水释放出大量的热,可利用该反应设计成原电池,把化学能转化为电能 |
D.由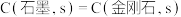 吸收的能量为 吸收的能量为 ,可知金刚石比石墨稳定 ,可知金刚石比石墨稳定 |
您最近一年使用:0次
名校
解题方法
10 . 到目前为止,由化学能转变的热能或电能仍然是人类使用的主要能源。现有反应①Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑②Zn+H2SO4=ZnSO4+H2↑。试回答下列问题:
(1)两反应中属于吸热反应的是_______ (填序号,下同),能设计成原电池的是_______ 。
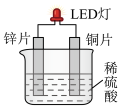
(2)化学课外活动小组设计的用铜-锌-稀硫酸原电池使LED灯发光的装置示意图。_______ (填“锌”或“铜”)电极方向移动。
②正极的电极方程式为_______ 。
③若反应过程中有0.2 mol电子的转移,则生成的氢气在标准状况下的体积为_______ L。
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:_______ 。(填“正极”或“负极”)
②电极b的电极反应式为_______ 。
(1)两反应中属于吸热反应的是
(2)化学课外活动小组设计的用铜-锌-稀硫酸原电池使LED灯发光的装置示意图。
②正极的电极方程式为
③若反应过程中有0.2 mol电子的转移,则生成的氢气在标准状况下的体积为
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
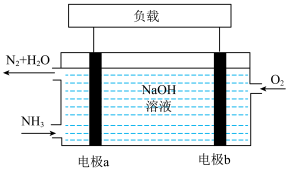
②电极b的电极反应式为
您最近一年使用:0次